அறிமுகம் - அணுக்களும் மூலக்கூறுகளும் | 10th Science : Chapter 7 : Atoms and Molecules
10வது அறிவியல் : அலகு 7 : அணுக்களும் மூலக்கூறுகளும்
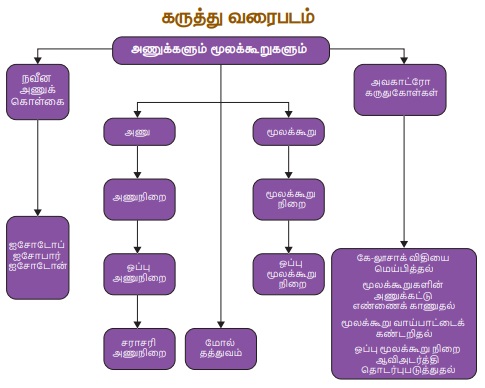
அணுக்களும் மூலக்கூறுகளும்
அலகு 7
அணுக்களும்
மூலக்கூறுகளும்

கற்றல் நோக்கங்கள்
இப்பாடத்தைக் கற்றபின், மாணவர்கள் பெறும்
திறன்களாவன:
* அணுக்கள் மற்றும் மூலக்கூறுகள்
பற்றிய அறிவைப் பெறுதல்.
* அணுநிறை மற்றும் மூலக்கூறு நிறையை
தொடர்புபடுத்துதல்.
* கிராம் அணு நிறை மற்றும் கிராம்
மூலக்கூறு நிறை பற்றிய தகவல்களை பெறுதல்.
* வாயுக்கள் பற்றிய அவகாட்ரோ
கருதுகோளின் உள்ளடங்கிய கருத்துக்களைப் புரிந்து கொள்ளுதல்.
* அவகாட்ரோ கருதுகோளினை வாழ்வியல்
சூழலுடன் தொடர்புபடுத்துதல்.
* மூலக்கூறுகளின் அணுக்கட்டு எண்ணைக்
கண்டறிதல்.
* ஆவி அடர்த்திக்கும் ஒப்பு மூலக்கூறு
நிறைக்கும் உள்ள தொடர்பினை வருவித்தல்.
* வாயுக்களின் பருமனுக்கும்
மூலக்கூறுகளின் எண்ணிக்கைக்கும் உள்ள தொடர்புகளைப் பெறுதல்.
* மோல் தத்துவத்தைப் பயன்படுத்தி
கணக்குகளைத் தீர்த்தல்.
* சதவீத இயைபினைக் கணக்கிடக் கற்றுக்
கொள்ளுதல்.
அறிமுகம்
நம்மைச் சுற்றியுள்ள பருப்பொருள்கள்
அனைத்தும் அணுக்களால் ஆனவை என்பதை நாம் முன் வகுப்புகளில் படித்துள்ளோம்.
முதன்முறையாக கி.மு (பொ.ஆ.மு) 5ம் நூற்றாண்டில் கிரேக்கத் தத்துவவியலாளர்கள் அணுவைப் பற்றிய தங்களது
கொள்கையை வெளியிட்டனர். அவர்களது கொள்கையானது முற்றிலும் தத்துவம் சார்ந்ததேயன்றி
அதற்கு எந்தவித அறிவியல் அடிப்படையும் இல்லை.
ஜான் டால்டன் அணுவைப் பற்றிய முதல்
அறிவியல் கோட்பாட்டினை வெளியிட்டார். டால்டனின் சில கோட்பாடுகள் ஜே.ஜே.தாம்சன், ரூதர்போர்டு,
நீல்ஸ்போர், ஷிரோடிஞ்சர் (Schrodinger)
போன்ற பிந்தைய அறிவியல் அறிஞர்களின் ஆய்வுகளால் தவறு என
கண்டறியப்பட்டது. அவர்களது ஆய்வு முடிவுகளின் அடிப்படையில் டால்டன் கோட்பாட்டின்
குறைகள் நீக்கப்பட்டு ‘நவீன அணுக்கொள்கை’ என்ற கோட்பாடு முன் மொழியப்பட்டது. நவீன அணுக் கொள்கைகளின் சில முக்கிய
கருத்துருக்கள் பின்வருமாறு.
· அணு என்பது பிளக்கக்கூடிய துகள் (எலக்ட்ரான், புரோட்டான்
நியூட்ரான் கண்டுபிடிப்புக்குப் பிறகு)
· ஒரே
தனிமத்தின் அணுக்கள் வெவ்வேறு அணு நிறைகளைப் பெற்றுள்ளன. (ஐசோடோப்புகளின்
கண்டுபிடிப்புகளுக்குப் பிறகு எ.கா. 17Cl35, 17Cl37)
· வெவ்வேறு
தனிமங்களின் அணுக்கள் ஒரே அணுநிறைகளைப் பெற்றுள்ளன. (ஐசோபார்களின்
கண்டுபிடிப்புகளுக்குப் பிறகு எகா 18Ar40, 20Ca40)
· அணுவை
ஆக்கவோ, அழிக்கவோ முடியாது.
ஒரு தனிமத்தின் அணுக்களை மற்றொரு தனிமத்தின் அணுக்களாக மாற்றமுடியும். (செயற்கை
மாற்று தனிமமாக்கல் முறை)
· அணுவானது
எளிய முழு எண்களின் விகிதத்தில் இருக்க வேண்டிய அவசியமில்லை. (எ.கா. குளுக்கோஸ் C6H12O6 C:H:O
= 6:12:6 அல்லது
1:2:1 மற்றும்
சுக்ரோஸ் C12H22O11
C : H : O = 12 : 22 : 11
· அணு என்பது வேதிவினையில் ஈடுபடும் மிகச்சிறிய
துகள்.
· ஒரு
அணுவின் நிறையிலிருந்து அதன் ஆற்றலை கணக்கிட முடியும் (E = mc2)
நவீன அணுக்கொள்கையானது அணுக்களின்
இயற்பியல் மற்றும் வேதியியல் பண்புகளுக்கு அடிப்படையானது. அணுவைப் பற்றிய
அடிப்படைக் கருத்துகளை நீங்கள் முன் வகுப்புகளில் படித்துள்ளீர்கள். தற்போது
அணுவைப் பற்றி விரிவாக பார்ப்போம்.