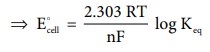மின் வேதியியல் - கலவினைகளின் வெப்ப இயக்கவியல் | 12th Chemistry : UNIT 9 : Electro Chemistry
12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 9 : மின் வேதியியல்
கலவினைகளின் வெப்ப இயக்கவியல்
கலவினைகளின் வெப்ப இயக்கவியல்
கால்வானிக் மின்கலத்தில் வேதி ஆற்றலானது மின்னாற்றலாக மாற்றப்படுகிறது என்பதை நாம் கற்றறிந்தோம். மின்கலத்தில் உருவாக்கப்பட்ட மின்னாற்றலானது, எலக்ட்ரான்களின் மொத்த மின்சுமை மற்றும், மின்முனைகளுக்கிடையே எலக்ட்ரான்களை இயக்க உதவும் மின்கலத்தின் emf மதிப்பு ஆகியவற்றின் பெருக்குத் தொகைக்கு சமமாக இருக்கும்.
ஒட்டுமொத்த கலவினைவில் ஆக்ஸிஜனேற்றி மற்றும் ஒடுக்கிகளுக்கிடையே பரிமாற்றம் செய்யப்பட்ட எலக்ட்ரான்களின் மோல் எண்ணிகையை 'n' எனக் கொண்டால், மின்கலத்தில் உருவாக்கப்பட்ட மின்னாற்றலின் அளவு கீழே கொடுக்கப்பட்டுள்ளது.
மின்னாற்றல் = n மோல் எலக்ட்ரான்களின் மின்னூட்டம் XEமின்கலம் .......(9.20)
1 மோல் எலக்ட்ரான்களின் மின்னூட்டம் = ஒரு ஃபாரடே (1F)
ஃ n மோல் எலக்ட்ரான்களின் மின்னூட்டம் = nF
சமன்பாடு (9.20) ⇒ மின்னாற்றல் = nF Eமின்கலம் .... (9.21)
1 எலக்ட்ரானின் மின்சுமை = 1.602 × 10-19 C
ஃ.1 மோல் எலக்ட்ரான்களின் மின்சுமை = 6.023 × 1023 × 1.602 × 10-19 C
= 96488 C
i.e., 1F = 96500 C
இந்த ஆற்றலானது, மின்னாற் வேலை செய்ய பயன்படுத்தப்படுகிறது. எனவே, ஒரு கால்வானிக் மின்கலத்திலிருந்து பெறக்கூடிய அதிகபட்ச வேலை
(W.max) cell = - nFEcell ...... (9.22)
அமைப்பானது சூழலின்மீது வேலையை செய்வதை குறிப்பிட (-) குறி புகுத்தப்பட்டுள்ளது.
வெப்ப இயக்கவியலின் இரண்டாம் விதிப்படி,அமைப்பினால் செய்யப்பட்ட வேலையானது, அமைப்பின் கட்டிலா ஆற்றலில் ஏற்பட்ட மாற்றத்திற்கு சமமாக இருக்கும் என்பதை நாம் அறிவோம்.
i.e., W.max = ∆G ......(9.23)
(9.22) மற்றும் (9.23) லிருந்து,
∆G = - nFEcell ... (9.24)
தன்னிச்சையான கலவினைகளுக்கு, ∆G மதிப்பு எதிர்குறி மதிப்பாக இருத்தல் அவசியம். எதிர்குறி ∆G மதிப்பை பெற Eமின்கலன் மதிப்பானது நேர்குறி கொண்டதாக இருத்தல் அவசியம் என்பதை சமன்பாடு (9.24) காட்டுகிறது.
மின்கலத்தின் அனைத்து உட்கூறுகளும் அவற்றின் திட்ட நிலைகளில் உள்ளபோது, சமன்பாடு (9.24) ஆனது பின்வருமாறு மாறுகிறது.
∆Go = - nFEocell ... (9.25)
திட்ட கட்டிலா ஆற்றல் மாற்றமானது சமநிலை மாறிலியுடன் பின்வரும் சமன்பாட்டினால் தொடர்பு படுத்தப்பட்டுள்ளதை நாம் அறிவோம்.
∆Go = RT InKeq .....(9.26)
(9.25) மற்றும் (9.26) ஆகியவற்றை ஒப்பிடும்போது,
nFEocell = RT InKeq
⇒ Eocell = [2.303 RT / nF] log Keq .....(9.27)