அணு அமைப்பு | வேதியியல் | அறிவியல் - பின்வரும் கேள்விகளுக்கு விடையளிக்க | 9th Science : Chemistry : Atomic Structure
9 ஆம் வகுப்பு அறிவியல் : அலகு 11 : அணு அமைப்பு
பின்வரும் கேள்விகளுக்கு விடையளிக்க
VI. மிகச் சுருக்கமாக
விடையளி
1.
முதல்
வட்டப்பாதையிலும்,
இரண்டாவது
வட்டப்
பாதையிலும்
ஒரே
மாதிரியான
எலக்ட்ரான்களின்
எண்ணிக்கையைப்
பெற்றுள்ள
தனிமத்தைக்
கூறுக.
விடை :
பெரிலியம் (2,2)
2.
K மற்றும்
CI ஆகியவற்றின்
எலக்ட்ரான்
பகிர்வை
எழுதுக.
விடை :
K+ ன் எலக்ட்ரான் அமைப்பு : (2,8,8,1)
Cl- ன் எலக்ட்ரான் அமைப்பு : (2,8,7)
3.
கீழே
கொடுக்கப்பட்டுள்ள
துகள்கள்
குறிக்கும்
குறியீட்டின்
பெயரினை
எழுதி
அவற்றின்
கீழ்
மற்றும்
மேலே
உள்ள
எண்கள்
எதனைக்
குறிக்கின்றன
என்பதனை
விளக்குக.
1H1, 0n1, -1e0
விடை :
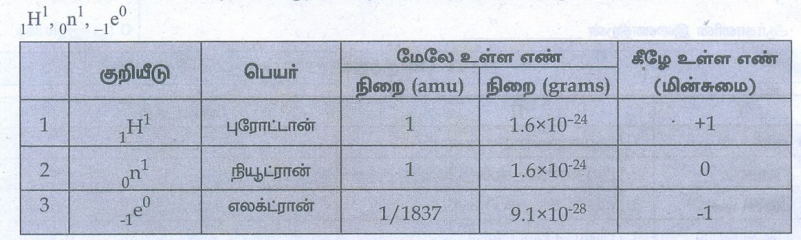
4. X என்ற
அணுவில்
K, L, M கூடுகள்
அனைத்தும்
நிரம்பியிருந்தால்,
அந்த
அணுவில்
உள்ள
மொத்த
எலக்ட்ரான்களின்
எண்ணிக்கை
என்ன?
விடை :
மொத்த எலக்ட்ரான்களின் எண்ணிக்கை
= K + L + M
= 2 + 8 + 8 = 18
5.
எலக்ட்ரான்
அமைப்பினைப்
பொறுத்து
இவற்றிற்கிடையே
உள்ள
ஒற்றுமை
யாது?
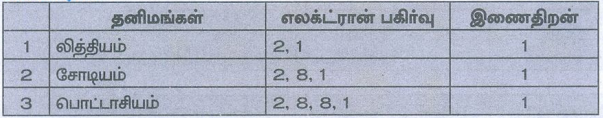
அ. லித்தியம், சோடியம் மற்றும் பொட்டாசியம்
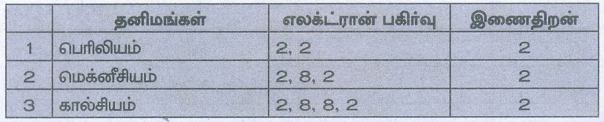
ஆ. பெரிலியம், மெக்னீசியம் மற்றும் கால்சியம்
விடை :
லித்தியம், சோடியம் மற்றும் பொட்டாசியம் அணுக்களின் இணைதிறன் கூட்டில் ஒரு எலக்ட்ரான் மட்டுமே உள்ளது. எனவே இவைகளின் இணைதிறன் 1
பெரிலியம், மெக்னீசியம் மற்றும் கால்சியம் அணுக்களின் இணைதிறன்
கூட்டில் இரு எலக்ட்ரான் மட்டுமே உள்ளது. எனவே
இவைகளின் இணைதிறன் 2
VII. சுருக்கமாக விடையளி
1.
அணுவில்
வெற்றிடம்
இருப்பது
எவ்வாறு
கண்டறியப்பட்டது?
விடை :
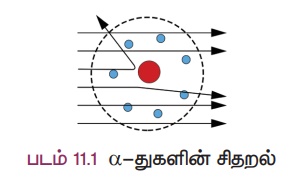
• ரூதர்போர்டு மெல்லிய தங்கத் தகட்டின் மீது மிகச்சிறிய நேர்மின் துகள்களானmஆல்பா கதிர்களை விழச் செய்தார்.
• பெரும்பாலான ஆல்பா துகள்கள் ஊடுருவி நேர்கோட்டுப் பாதையில் விலகல் அடையாமல் சென்றன.
• எனவே அணுவின் பெரும்பகுதி வெற்றிடமாக உள்ளது எனக் கண்டறிந்தார்.
2. 3517Cl மற்றும் 3717 Cl இவற்றின்
வேதியியல்
பண்புகள்
ஒன்றாக
இருப்பதற்கான
காரணம்
யாது?
விடை :
• ஒரு தனிமத்தின் வேதியியல் பண்புகள் அவை பெற்றுள்ள எலக்ட்ரான்களின் எண்ணிக்கையைப் பொறுத்து அமைகிறது.
• 3517Cl 3717Cl வேறுபட்ட அணு எடைகளைப் பெற்றிருந்தாலும், இரண்டு குளோரின் அணுக்களும் ஒத்த எலக்ட்ரான்களை பெற்றுள்ளது.
• எனவே இவற்றின் வேதிப்பண்புகள் ஒன்றாக உள்ளது.
3.
ஆக்சிஜன்
மற்றும்
சல்ஃபர்
அணுக்களின்
அணு
அமைப்பை
வரைக.
விடை :
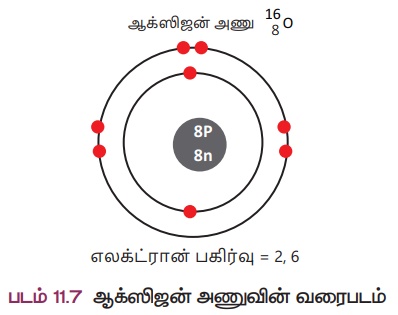
ஆக்சிஜன் (2,6)
அணு எண் = 8
நிறை எண் = 16
புரோட்டான் = 8
நியூட்ரான் = 8
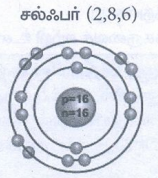
சல்ஃபர் (2,8,6)
அணு எண் = 16
நிறை எண் = 32
புரோட்டான் = 16
நியூட்ரான் = 16
4.
கீழே
கொடுக்கப்பட்டுள்ள
அணு
எண்
மற்றும்
நிறை
எண்களை
கொண்டு,
புரோட்டான்கள்,
நியூட்ரான்கள்
மற்றும்
எலக்ட்ரான்களின்
எண்ணிக்கையை
கணக்கிடுக.
1. அணு எண் 3 மற்றும் நிறை எண் 7
தீர்வு :
அணு எண் = 3
நிறை எண் = 7
அணு எண் = புரோட்டான்களின் எண்ணிக்கை (or) எலக்ட்ரான் எண்ணிக்கை ஃ புரோட்டான்களின் எண்ணிக்கை = 3 ;
எலக்ட்ரான்களின் எண்ணிக்கை = 3
ஃபுரோட்டான்களின் எண்ணிக்கை = எலக்ட்ரான்களின் எண்ணிக்கை
நிறை எண் = புரோட்டான்களின் எண்ணிக்கை + நியூட்ரான்களின் எண்ணிக்கை
நியூட்ரான்களின் எண்ணிக்கை = நிறை எண் - புரோட்டான்களின் எண்ணிக்கை = 7 – 3
நியூட்ரான்களின் எண்ணிக்கை = 4
ii. அணு எண் 92 மற்றும் நிறை எண் 238
தீர்வு :
அணு எண் = 92
நிறை எண் = 238
அணு எண் = புரோட்டான்களின் எண்ணிக்கை (or) எலக்ட்ரான் எண்ணிக்கை
ஃ புரோட்டான்களின் எண்ணிக்கை = 92 ;
எலக்ட்ரான்களின் எண்ணிக்கை = 92
நியூட்ரான்களின் எண்ணிக்கை = 238 - 92 = 146
நியூட்ரான்களின் எண்ணிக்கை = 146
5.
நியூக்ளியான்
என்றால்
என்ன?
பாஸ்பரசில்
எத்தனை
நியூக்ளியான்கள்
உள்ளன?
அதன்
அணு
அமைப்பை
வரைக.
விடை :
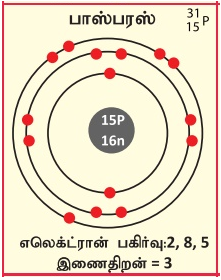
• நியூக்ளியான் என்பது ஒரு அணுவின் உட்கருவில் உள்ள புரோட்டான்கள் மற்றும் நியூட்ரான்களின் எண்ணிக்கை.
• பாஸ்பரஸ்சில் உள்ள நியூக்ளியான்கள்
புரோட்டான்கள் = 15
நியூட்ரான்கள் = 16
மொத்த நியுக்ளியான்கள் = புரோட்டான்கள் + நியூட்ரான்கள்
= 15 + 16
= 31
VIII. விரிவாக விடையளி
1.
தங்கத்
தகடு
சோதனையின்
மூலம்
நீ
என்ன
முடிவிற்கு
வருகிறாய்?
விடை :
• அணுவின் மையப்பகுதியில் மிக மிகச்சிறிய உட்கரு உள்ளது
• உட்கருவைச் சுற்றியுள்ள பெரும்பகுதி வெற்றிடமாக உள்ளது.
• அணுவின் மொத்த நிறையும் உட்கரு எனப்படும் சிறிய நேர்மின்சுமை கொண்ட பகுதிய பொதிந்துள்ளது. \
• அணுக்கருவைச் சுற்றி உள்ள எலக்ட்ரான்கள் வட்டவடிவப் பாதையில் சுற்றி வருகின்றன.
2.
போரின்
அணு
மாதிரியின்
கூற்றுக்களை
பற்றி
விளக்குக.
விடை :
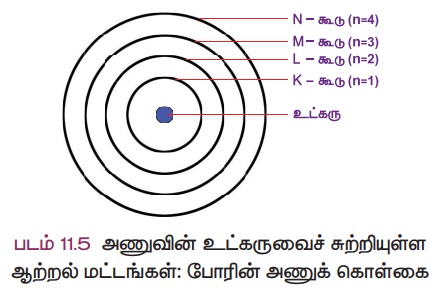
• ஓர் அணுவில் எலக்ட்ரான்கள் 'ஆர்பிட்' எனப்படும் நிலையான
வட்டப் பாதையில் அணுக்கருவைச் சுற்றி வருகின்றன.
• சுற்றி வரும் எலக்ட்ரான்கள் ஆற்றலை இழப்பதோ, ஏற்பதோ
இல்லை .
• வட்டப்பாதைகள் 1,2,3,4 அல்லது K,L,M,N என பெயரிடப்பட்டுள்ளன.
• ஆற்றல் மட்டத்தில் இடங்கொள்ளும் அதிகபட்ச எலக்ட்ரான்களின்
எண்ணிக்கை = 2N2
• எலக்ட்ரான் ஆற்றலை உறிஞ்சும் போது உயர் ஆற்றல் மட்டத்திற்கும், ஆற்றலை வெளியிடும்போது குறைந்த ஆற்றல் மட்டத்திற்கும் இடம் பெயருகின்றன.
3.
கேலூசாக்கின் பருமன் இணைப்பு விதியைக் கூறி உதாரணத்துடன் விளக்கு.
விடை :
"வாயுக்கள் வினைபுரியும் போது அவற்றின் பருமன்கள் அவ்வினையின் விளைபொருள்களி பருமனுக்கு எளிய முழுஎண் விகிதத்தில் இருக்கும்” . (உ.ம்) H2 + Cl2 →2HCl
(1 பருமன் + 1 பருமன் → 2 பருமன்)
1 : 1 : 2
பிற நூல்கள்
1.
Atomic Structure Rebecca L. Johnson Twenty First Century Books.
2.
Atomic structure and Periodicity Jack Barrett. Royal Society of Chemistry.
3.
Chemistry for Degree Students (B.Sc. Sem.-1, As per CBCS) R L Madan.
இணைய வளங்கள்
https://www.youtube.com/watch?v=t4xgvINFQ3c
https://www.youtube.com/watch?
v=P6DMEgE8CK8
https://www.youtube.com/watch?
v=YURRel6OJsg
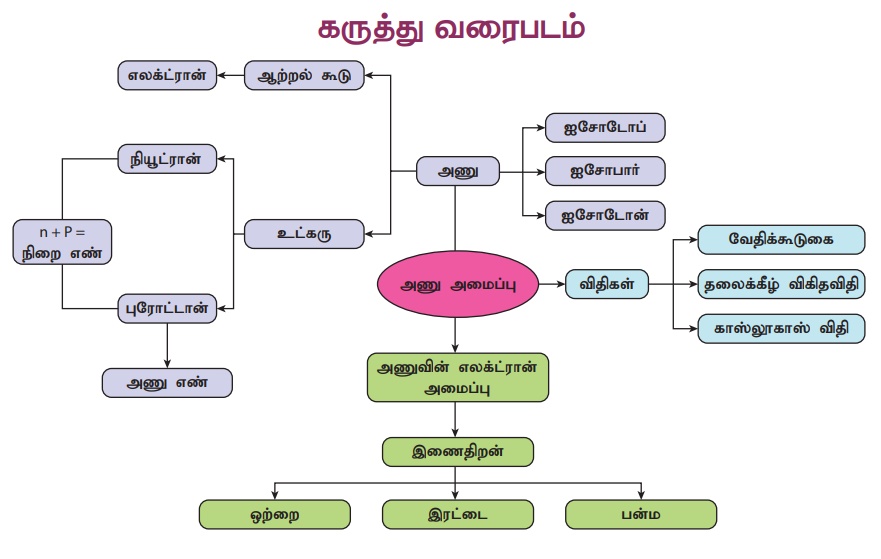
கருத்து வரைபடம்
இணையச்செயல்பாடு
அணு அமைப்பு
படி 1.
கீழ்க்காணும் உரலி /
விரைவுக் குறியீட்டைப் பயன்படுத்திச் செயல்பாட்டின் இணையப் பக்கத்திற்குச் செல்க.
படி 2.
முதலில் ATOM
என்பதைத் தேர்வு செய்தால் பல தேர்வுகளுடன் அணுப்பாதை திரையில் தோன்றும். புரோட்டான், எலக்ட்ரான் மற்றும் நியூட்ரான்களை இழுத்துக் கொண்டு அணு அமைப்பில் விடும்போது அவற்றின் எண்ணிக்கைக்கு ஏற்ப அருகில் உள்ள தனிம அட்டவணையில் தனிம பெயர் தோன்றும்.
படி 3.
அடுத்து குறியீடுக்குள் சென்றால் புரோட்டான், நியூட்ரான் மற்றும் எலக்ட்ரான்களின் எண்ணிக்கைக்கு ஏற்ப அருகில் உள்ள கட்டத்தில் தனிம பெயர் அவற்றின் அணு எண்,
அணு நிறை மற்றும் நியூட்ரான்களின் எண்ணிக்கைத் தோன்றும்.
படி 4.
மதிப்பீடாக GAMES
ஐ தேர்வு செய்து மாணவர்களின் புரிந்து கொள்ளலை இன்னும் மேம்படுத்தலாம்.
உரலி: https://phet.colorado.edu/sims/html/build-an-atom/latest/build-an-atom_en.html