குறைபாடுகள் - போரின் அணுக் கொள்கை | 9th Science : Atomic Structure
9 ஆம் வகுப்பு அறிவியல் : அலகு 11 : அணு அமைப்பு
போரின் அணுக் கொள்கை
போரின் அணுக் கொள்கை
1913-ஆம் ஆண்டில், டென்மார்க் நாட்டைச் சேர்ந்த நீல்ஸ்போர் எனும் இயற்பியலாளர், அணுவின் நிலைப்புத் தன்மையை நியாயப் படுத்துவதற்காக புதிய அணுக் கொள்கையினை உருவாக்கினார். அதன் முக்கியக் கருத்துக்கள்:
i. ஓர் அணுவில் எலக்ட்ரான்கள் நிலையான வட்டப்பாதையில் அணுக்கருவைச் சுற்றி வருகின்றன. இவ்வட்டப் பாதைகள் ஆர்பிட்டுகள் அல்லது ஆற்றல் மட்டங்கள் என அழைக்கப்படுகின்றன.
ii.
ஒரே வட்டப்பாதையில் எலக்ட்ரான்கள் சுற்றி வருகையில் ஆற்றலை இழப்பதோ அல்லது ஏற்பதோ இல்லை.
iii. ஒரு ஆற்றல் மட்டத்திலிருக்கும் எலக்ட்ரான் உயர் அல்லது குறைந்த ஆற்றல் மட்டத்திற்கு நகரும்போது ஆற்றலை ஏற்கவோ அல்லது
இழக்கவோ செய்யும்.
iv. இவ்வட்டப் பாதைகள் 1,2,3,4 அல்லது K, L, M ,N எனப் பெயரிடப்படுகின்றன.
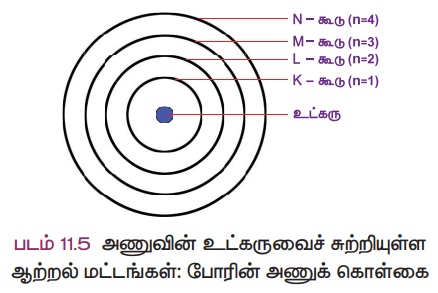
உட்கருவிற்கு அருகாமையில் இருக்கும் K
கூடு (n
= 1) குறைந்த ஆற்றலை உடையது. L, M, N ....... ஆகியன அடுத்தடுத்த உயர் ஆற்றல் மட்டங்கள் ஆகும். உட்கருவிலிருந்து தொலைவு அதிகரிக்கும் போது,
ஆர்பிட்டின் ஆற்றலும் அதிகரிக்கிறது. ஒவ்வொரு ஆர்பிட்டும் நிலையான ஆற்றல் அளவினைப் பெற்றிருப்பதால், அவற்றை ஆற்றல் நிலை அல்லது ஆற்றல் மட்டங்கள் என போர் அழைத்தார்.
1. போர் அணுக் கொள்கையின் குறைபாடுகள்
ஹைட்ரஜன் மற்றும் ஹைட்ரஜன் போன்ற (He+, Li2+, Be3+) அயனிகளுக்கு மட்டுமே போரின் அணுக்கொள்கை பொருந்தியது. இந்த அணுக்கொள்கை, பல எலக்ட்ரான்களை உடைய அணுக்களுக்கு விரிவாக்கம் செய்யப்படவில்லை.