Я«хЯ»ЄЯ«цЯ«┐Я«»Я«┐Я«»Я«▓Я»Ї - Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»Ђ Я«ЋЯ«БЯ»ЇЯ«ЪЯ»ЂЯ«фЯ«┐Я«ЪЯ«┐Я«фЯ»ЇЯ«фЯ»Ђ | 9th Science : Atomic Structure
9 Я«єЯ««Я»Ї Я«хЯ«ЋЯ»ЂЯ«фЯ»ЇЯ«фЯ»Ђ Я«ЁЯ«▒Я«┐Я«хЯ«┐Я«»Я«▓Я»Ї : Я«ЁЯ«▓Я«ЋЯ»Ђ 11 : Я«ЁЯ«БЯ»Ђ Я«ЁЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ»Ђ
Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»Ђ Я«ЋЯ«БЯ»ЇЯ«ЪЯ»ЂЯ«фЯ«┐Я«ЪЯ«┐Я«фЯ»ЇЯ«фЯ»Ђ
Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»Ђ Я«ЋЯ«БЯ»ЇЯ«ЪЯ»ЂЯ«фЯ«┐Я«ЪЯ«┐Я«фЯ»ЇЯ«фЯ»Ђ
1911 Я«єЯ««Я»Ї Я«єЯ«БЯ»ЇЯ«ЪЯ«┐Я«▓Я»Ї,
Я«еЯ«┐Я«»Я»ѓЯ«џЯ«┐Я«▓Я«ЙЯ«еЯ»ЇЯ«цЯ»Ђ Я«еЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«ЕЯ»Ї Я«ЁЯ«▒Я«┐Я«хЯ«┐Я«»Я«▓Я«ЙЯ«│Я«░Я»Ї Я«▓Я«ЙЯ«░Я»ЇЯ«ЪЯ»Ї Я«░Я»ѓЯ«цЯ«░Я»ЇЯ«фЯ»ІЯ«░Я»ЇЯ«ЪЯ»Ђ, Я«њЯ«░Я»Ђ Я««Я»єЯ«▓Я»ЇЯ«▓Я«┐Я«» Я«цЯ«ЎЯ»ЇЯ«ЋЯ«цЯ»Ї Я«цЯ«ЋЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«ЕЯ»Ї Я««Я»ђЯ«цЯ»Ђ Я««Я«┐Я«ЋЯ«џЯ»Ї Я«џЯ«┐Я«▒Я«┐Я«» Я«еЯ»ЄЯ«░Я»Ї Я««Я«┐Я«ЕЯ»Ї Я«цЯ»ЂЯ«ЋЯ«│Я»ЇЯ«ЋЯ«│Я«ЙЯ«Е Я«єЯ«▓Я»ЇЯ«фЯ«Й Я«ЋЯ«цЯ«┐Я«░Я»ЇЯ«ЋЯ«│Я»ѕ Я«хЯ«┐Я«┤Я«џЯ»ЇЯ«џЯ»єЯ«»Я»ЇЯ«цЯ»Ђ Я«цЯ«ЕЯ»ЇЯ«ЕЯ»ЂЯ«ЪЯ»ѕЯ«» Я«ЅЯ«▓Я«Ћ Я«фЯ«┐Я«░Я«џЯ«┐Я«цЯ»ЇЯ«цЯ«┐ Я«фЯ»єЯ«▒Я»ЇЯ«▒ Я«цЯ«ЎЯ»ЇЯ«ЋЯ«цЯ»ЇЯ«цЯ«ЋЯ«ЪЯ»Ђ Я«ЁЯ«БЯ»Ђ Я«єЯ«»Я»ЇЯ«хЯ»Ђ Я«џЯ»ІЯ«цЯ«ЕЯ»ѕЯ«»Я»ѕ Я«еЯ«┐Я«ЋЯ«┤Я»ЇЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ«ЙЯ«░Я»Ї. Я«цЯ«ЎЯ»ЇЯ«ЋЯ««Я»Ї Я«јЯ«│Я«┐Я«цЯ«┐Я«▓Я»Ї Я«цЯ«ЋЯ«ЪЯ«ЙЯ«ЋЯ«ЋЯ»Ї Я«ЋЯ»ѓЯ«ЪЯ«┐Я«»Я«цЯ«ЙЯ«Ћ Я«ЄЯ«░Я»ЂЯ«фЯ»ЇЯ«фЯ«цЯ«ЙЯ«▓Я»Ї Я«ЁЯ«хЯ«░Я»Ї Я«цЯ«ЎЯ»ЇЯ«ЋЯ«цЯ»Ї Я«цЯ«ЋЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«ЕЯ»ѕЯ«цЯ»Ї Я«цЯ»ЄЯ«░Я»ЇЯ«еЯ»ЇЯ«цЯ»єЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ«ЙЯ«░Я»Ї.
Я«ЄЯ«џЯ»ЇЯ«џЯ»ІЯ«цЯ«ЕЯ»ѕЯ«»Я«┐Я«ЕЯ»Ї Я«фЯ»ІЯ«цЯ»Ђ Я«ЋЯ»ђЯ«┤Я»ЇЯ«ЋЯ«БЯ»ЇЯ«ЪЯ«хЯ«▒Я»ЇЯ«▒Я»ѕ Я«ЁЯ«хЯ«░Я»Ї Я«ЋЯ«хЯ«ЕЯ«┐Я«цЯ»ЇЯ«цЯ«ЙЯ«░Я»Ї:
1.
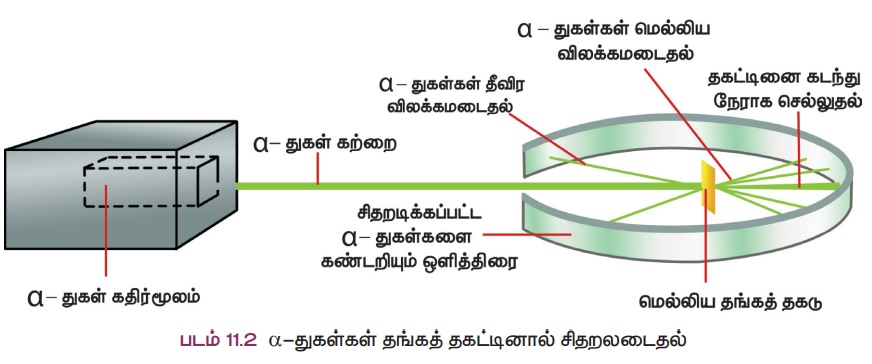
Я«фЯ»єЯ«░Я»ЂЯ««Я»ЇЯ«фЯ«ЙЯ«▓Я«ЙЯ«Е Я«єЯ«▓Я»ЇЯ«фЯ«Й Я«цЯ»ЂЯ«ЋЯ«│Я»ЇЯ«ЋЯ«│Я»Ї Я«цЯ«ЎЯ»ЇЯ«ЋЯ«цЯ»Ї Я«цЯ«ЋЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«ЕЯ»ЂЯ«│Я»Ї Я«іЯ«ЪЯ»ЂЯ«░Я»ЂЯ«хЯ«┐ Я«еЯ»ЄЯ«░Я»ЇЯ«ЋЯ»ІЯ«ЪЯ»ЇЯ«ЪЯ»ЂЯ«фЯ»Ї Я«фЯ«ЙЯ«цЯ»ѕЯ«»Я«┐Я«▓Я»Ї Я«џЯ»єЯ«ЕЯ»ЇЯ«▒Я«Е.
2.
Я«џЯ«┐Я«▓ Я«єЯ«▓Я»ЇЯ«фЯ«Й Я«цЯ»ЂЯ«ЋЯ«│Я»ЇЯ«ЋЯ«│Я»Ї Я«еЯ»ЄЯ«░Я»ЇЯ«ЋЯ»ІЯ«ЪЯ»ЇЯ«ЪЯ»ЂЯ«фЯ»Ї Я«фЯ«ЙЯ«цЯ»ѕЯ«»Я«┐Я«▓Я»Ї Я«ЄЯ«░Я»ЂЯ«еЯ»ЇЯ«цЯ»Ђ Я«џЯ«┐Я«▒Я»Ђ Я«ЋЯ»ІЯ«БЯ«цЯ»ЇЯ«цЯ«┐Я«▓Я»Ї Я«хЯ«┐Я«▓Я«ЋЯ»ЇЯ«ЋЯ««Я»Ї Я«ЁЯ«ЪЯ»ѕЯ«еЯ»ЇЯ«цЯ«Е.
3.
Я««Я«┐Я«ЋЯ«ЋЯ»Ї Я«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«єЯ«▓Я»ЇЯ«фЯ«Й Я«цЯ»ЂЯ«ЋЯ«│Я»ЇЯ«ЋЯ«│Я»Ї Я«хЯ«еЯ»ЇЯ«ц Я«фЯ«ЙЯ«цЯ»ѕЯ«»Я«┐Я«▓Я»ЄЯ«»Я»Є Я«цЯ«┐Я«░Я»ЂЯ«фЯ»ЇЯ«фЯ«┐ Я«ЁЯ«ЕЯ»ЂЯ«фЯ»ЇЯ«фЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«ЪЯ«Е.
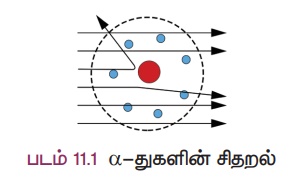
Я«ЄЯ«еЯ»ЇЯ«ц Я«єЯ«▓Я»ЇЯ«фЯ«Й Я«цЯ»ЂЯ«ЋЯ«│Я»ЇЯ«ЋЯ«│Я»Ї Я«џЯ«┐Я«цЯ«▒Я«▓Я«ЪЯ»ѕЯ«»Я»ЂЯ««Я»Ї Я«єЯ«»Я»ЇЯ«хЯ«┐Я«ЕЯ»Ї Я««Я»ЂЯ«ЪЯ«┐Я«хЯ»ЂЯ«ЋЯ«│Я»ѕ Я«фЯ»іЯ«цЯ»ЂЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐ Я«њЯ«░Я»Ђ Я«ЁЯ«БЯ»ЂЯ«ЋЯ»Ї Я«ЋЯ»іЯ«│Я»ЇЯ«ЋЯ»ѕЯ«»Я«┐Я«ЕЯ»ѕ Я«░Я»ѓЯ«цЯ«░Я»ЇЯ«фЯ»ІЯ«░Я»ЇЯ«ЪЯ»Ђ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ«┐Я«ЕЯ«ЙЯ«░Я»Ї,
Я«ЄЯ«цЯ»ЂЯ«хЯ»Є Я«░Я»ѓЯ«цЯ«░Я»ЇЯ«фЯ»ІЯ«░Я»ЇЯ«ЪЯ»Ђ Я«ЁЯ«БЯ»ЂЯ«ЋЯ»Ї Я«ЋЯ»іЯ«│Я»ЇЯ«ЋЯ»ѕ Я«јЯ«ЕЯ»ЇЯ«▒Я»Ђ Я«ЁЯ«┤Я»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
1. Я«░Я»ѓЯ«цЯ«░Я»ЇЯ«фЯ»ІЯ«░Я»ЇЯ«ЪЯ»Ђ Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ»іЯ«│Я»ЇЯ«ЋЯ»ѕ
Я«ЄЯ«еЯ»ЇЯ«ц Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ»іЯ«│Я»ЇЯ«ЋЯ»ѕЯ«»Я«┐Я«ЕЯ»Ї Я««Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«»Я«ЋЯ»Ї Я«ЋЯ«░Я»ЂЯ«цЯ»ЇЯ«цЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«│Я»Ї:
i.
Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«фЯ»єЯ«░Я»ЂЯ««Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ«┐ Я«хЯ»єЯ«▒Я»ЇЯ«▒Я«┐Я«ЪЯ««Я«ЙЯ«Ћ Я«ЅЯ«│Я»ЇЯ«│Я«цЯ»Ђ.
ii.
Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я««Я»ѕЯ«»Я«цЯ»ЇЯ«цЯ«┐Я«▓Я»ЂЯ«│Я»ЇЯ«│ Я«ЁЯ«цЯ«┐Я«Ћ Я«еЯ»ЄЯ«░Я»ЇЯ««Я«┐Я«ЕЯ»Ї Я«џЯ»ЂЯ««Я»ѕЯ«»Я»ЂЯ«ЪЯ»ѕЯ«» Я«фЯ«ЋЯ»ЂЯ«цЯ«┐ Я«ЅЯ«ЪЯ»ЇЯ«ЋЯ«░Я»Ђ Я«јЯ«ЕЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
iii. Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«ЁЯ«│Я«хЯ»ѕ Я«њЯ«фЯ»ЇЯ«фЯ«┐Я«ЪЯ»ЂЯ««Я»ЇЯ«фЯ»ІЯ«цЯ»Ђ Я«ЅЯ«ЪЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«ЁЯ«│Я«хЯ»Ђ Я««Я«┐Я«ЋЯ«џЯ»ЇЯ«џЯ«┐Я«▒Я«┐Я«»Я«цЯ«ЙЯ«Ћ Я«ЅЯ«│Я»ЇЯ«│Я«цЯ»Ђ.
iv.
Я«јЯ«▓Я«ЋЯ»ЇЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я»Ї Я«ЅЯ«ЪЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ»ѕЯ«џЯ»Ї Я«џЯ»ЂЯ«▒Я»ЇЯ«▒Я«┐ Я«хЯ«░Я»ЂЯ««Я»Ї Я«хЯ«ЪЯ»ЇЯ«ЪЯ«фЯ»Ї Я«фЯ«ЙЯ«цЯ»ѕ Я«єЯ«░Я»ЇЯ«фЯ«┐Я«ЪЯ»Ї Я«јЯ«ЕЯ»ЇЯ«▒Я«┤Я»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
v.
Я«њЯ«ЪЯ»ЇЯ«ЪЯ»Ђ Я««Я»іЯ«цЯ»ЇЯ«цЯ««Я«ЙЯ«Ћ Я«њЯ«░Я»Ђ Я«ЁЯ«БЯ»Ђ Я«еЯ«ЪЯ»ЂЯ«еЯ«┐Я«▓Я»ѕ Я«хЯ«ЙЯ«»Я»ЇЯ«еЯ»ЇЯ«цЯ«цЯ»Ђ Я«єЯ«ЋЯ»ЂЯ««Я»Ї. Я«ЁЯ«цЯ«ЙЯ«хЯ«цЯ»Ђ, Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«▓Я»ЂЯ«│Я»ЇЯ«│ Я«фЯ»ЂЯ«░Я»ІЯ«ЪЯ»ЇЯ«ЪЯ«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«јЯ«▓Я«ЋЯ»ЇЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«јЯ«БЯ»ЇЯ«БЯ«┐Я«ЋЯ»ЇЯ«ЋЯ»ѕ Я«џЯ««Я««Я«ЙЯ«Ћ Я«ЄЯ«░Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї.

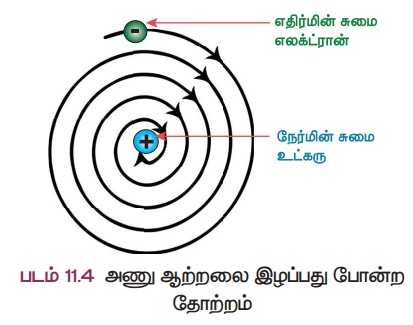
Я«░Я»ѓЯ«цЯ«░Я»ЇЯ«фЯ»ІЯ«░Я»ЇЯ«ЪЯ«┐Я«ЕЯ»Ї Я«ЁЯ«БЯ»Ђ Я«ЁЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«џЯ»ѓЯ«░Я«┐Я«» Я«ЋЯ»ЂЯ«ЪЯ»ЂЯ««Я»ЇЯ«фЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЁЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ»ІЯ«ЪЯ»Ђ Я«њЯ«цЯ»ЇЯ«цЯ»ЂЯ«│Я»ЇЯ«│Я«цЯ»Ђ. Я«џЯ»ѓЯ«░Я«┐Я«» Я«ЋЯ»ЂЯ«ЪЯ»ЂЯ««Я»ЇЯ«фЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я««Я»ѕЯ«»Я«цЯ»ЇЯ«цЯ«┐Я«▓Я«┐Я«░Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«џЯ»ѓЯ«░Я«┐Я«»Я«ЕЯ»ѕЯ«џЯ»Ї Я«џЯ»ЂЯ«▒Я»ЇЯ«▒Я«┐ Я«ЁЯ«цЯ«ЕЯ»Ї Я«ЋЯ»ІЯ«│Я»ЇЯ«ЋЯ«│Я»Ї Я«џЯ»ЂЯ«┤Я«▓Я»ЇЯ«хЯ«цЯ»ѕЯ«фЯ»ЇЯ«фЯ»ІЯ«▓ Я«њЯ«░Я»Ђ Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я««Я»ѕЯ«»Я«цЯ»ЇЯ«цЯ«┐Я«▓Я«┐Я«░Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«ЅЯ«ЪЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ«┐Я«ЕЯ»ѕЯ«џЯ»Ї Я«џЯ»ЂЯ«▒Я»ЇЯ«▒Я«┐Я«»Я»ЂЯ«│Я»ЇЯ«│ Я«єЯ«░Я»ЇЯ«фЯ«┐Я«ЪЯ»ЇЯ«ЪЯ»ЂЯ«ЋЯ«│Я«┐Я«▓Я»Ї Я«ЁЯ«цЯ«ЕЯ»Ї Я«јЯ«▓Я«ЋЯ»ЇЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я»Ї Я«џЯ»ЂЯ«┤Я«▓Я»ЇЯ«ЋЯ«┐Я«ЕЯ»ЇЯ«▒Я«Е.
2. Я«░Я»ѓЯ«цЯ«░Я»ЇЯ«фЯ»ІЯ«░Я»ЇЯ«ЪЯ»Ђ Я«ЁЯ«БЯ»ЂЯ«ЋЯ»Ї Я«ЋЯ»іЯ«│Я»ЇЯ«ЋЯ»ѕЯ«»Я«┐Я«ЕЯ»Ї Я«хЯ«░Я««Я»ЇЯ«фЯ»ЂЯ«ЋЯ«│Я»Ї
Я««Я«┐Я«ЕЯ»ЇЯ«ЋЯ«ЙЯ«еЯ»ЇЯ«цЯ«ЋЯ»Ї Я«ЋЯ»іЯ«│Я»ЇЯ«ЋЯ»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ«┐, Я«хЯ»ЄЯ«ЋЯ««Я«ЙЯ«Ћ Я«ЄЯ«»Я«ЎЯ»ЇЯ«ЋЯ«┐Я«ЋЯ»Ї Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ«┐Я«░Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«јЯ«▓Я«ЋЯ»ЇЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»Ї Я«цЯ»іЯ«ЪЯ«░Я»ЇЯ«еЯ»ЇЯ«цЯ»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ѕ Я«ЄЯ«┤Я«ЋЯ»ЇЯ«Ћ Я«хЯ»ЄЯ«БЯ»ЇЯ«ЪЯ»ЂЯ««Я»Ї. Я«ЄЯ«хЯ»ЇЯ«хЯ«ЙЯ«▒Я»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ѕ Я«ЄЯ«┤Я«фЯ»ЇЯ«фЯ«цЯ«ЙЯ«▓Я»Ї, Я«јЯ«▓Я«ЋЯ»ЇЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»Ї Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ»ѕЯ«џЯ»ЇЯ«џЯ»ЂЯ«▒Я»ЇЯ«▒Я«┐Я«хЯ«░Я»ЂЯ««Я»Ї Я«фЯ«ЙЯ«цЯ»ѕ Я«џЯ»ЂЯ«░Я»ЂЯ«ЎЯ»ЇЯ«ЋЯ«┐ Я«ЄЯ«▒Я»ЂЯ«цЯ«┐Я«»Я«┐Я«▓Я»Ї Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ«┐Я«ЕЯ»ЂЯ«│Я»Ї Я«хЯ«┐Я«┤ Я«хЯ»ЄЯ«БЯ»ЇЯ«ЪЯ»ЂЯ««Я»Ї. Я«ЄЯ«хЯ»ЇЯ«хЯ«ЙЯ«▒Я»Ђ Я«еЯ«┐Я«ЋЯ«┤Я»ЇЯ«еЯ»ЇЯ«цЯ«ЙЯ«▓Я»Ї Я«ЁЯ«БЯ»Ђ Я«ЁЯ«цЯ«ЕЯ»Ї Я«еЯ«┐Я«▓Я»ѕЯ«фЯ»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ««Я»ѕЯ«»Я»ѕ Я«ЄЯ«┤Я«ЋЯ»ЇЯ«Ћ Я«еЯ»ЄЯ«░Я«┐Я«ЪЯ»ЂЯ««Я»Ї. Я«єЯ«ЕЯ«ЙЯ«▓Я»Ї Я«ЁЯ«БЯ»Ђ Я«еЯ«┐Я«▓Я»ѕЯ«фЯ»ЇЯ«фЯ»ЂЯ«цЯ»Ї Я«цЯ«ЕЯ»ЇЯ««Я»ѕ Я«ЅЯ«ЪЯ»ѕЯ«»Я«цЯ»Ђ. Я«ЄЯ«цЯ«ЕЯ«ЙЯ«▓Я»Ї Я«░Я»ѓЯ«цЯ«░Я»ЇЯ«фЯ»ІЯ«░Я»ЇЯ«ЪЯ»Ђ Я«ЋЯ»іЯ«│Я»ЇЯ«ЋЯ»ѕ Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▓Я»ѕЯ«фЯ»ЇЯ«фЯ»ЂЯ«цЯ»Ї Я«цЯ«ЕЯ»ЇЯ««Я»ѕЯ«»Я»ѕ Я«хЯ«┐Я«│Я«ЋЯ»ЇЯ«Ћ Я«ЄЯ«»Я«▓Я«хЯ«┐Я«▓Я»ЇЯ«▓Я»ѕ.