வகைகள், பண்புகள், பயன்கள், இராஜதிராவகம் - காரங்கள் | 9th Science : Acids, Bases and Salts
9 ஆம் வகுப்பு அறிவியல் : அலகு 14 : அமிலங்கள், காரங்கள் மற்றும் உப்புகள்
காரங்கள்
காரங்கள்
அர்ஹீனியஸ் கொள்கையின்படி, காரங்கள் நீரில் கரையும்போது ஹைட்ராக்சைடு (OH-)
அயனிகளைத் தருவனவாகும். சில உலோக ஆக்சைடுகள் அமிலங்களுடன் வினைபுரிந்து உப்பையும், நீரையும் தருகின்றன. இவை காரங்கள் என்று அழைக்கப்படுகின்றன. நீரில் கரையும் காரங்கள் எரிகாரங்கள் (Alkali) என்றழைக்கப்படுகின்றன. ஒரு காரம் அமிலத்துடன் வினை புரிந்து உப்பையும்,
நீரையும் மட்டும் தரும்.
காரம் +
அமிலம் →
உப்பு +
நீர்
எடுத்துக்காட்டாக, ஜிங்க் ஆக்சைடு (ZnO),
HCl உடன் வினைபுரிந்து ஜிங்க் குளோரைடு உப்பு மற்றும் நீரைத் தருகிறது.
ZnO(s)
+ 2HCl(aq) → ZnCl(aq) +H2O(2)
இதேபோல் சோடியம் ஹைட்ராக்சைடு நீரில் அயனியுற்று, ஹைட்ராக்சைடு அயனிகளைத் தருகிறது. ஆகவே, இது நீரில் கரைகிறது. எனவே இது ஒரு எரிகாரம் ஆகும்.
NaOH(aq)
→ Na+ (aq) + OH-(aq)
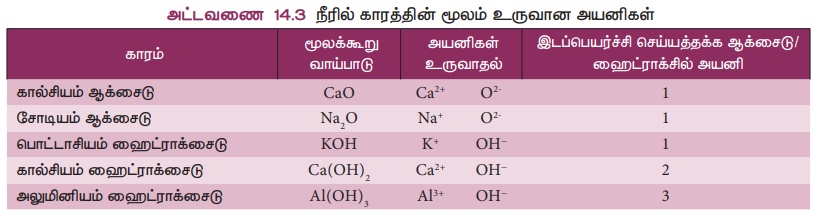
காரங்கள் ஒன்று அல்லது அதற்கு மேற்பட்ட இடப்பெயர்ச்சி செய்யத்தக்க ஆக்சைடு மற்றும் ஹைட்ராக்சைடு அயனிகளைக் கொண்டுள்ளன.
அட்டவணை 14.3 காரங்கள் நீரில் கரைந்து அயனிகளை உருவாக்குவதைக் காட்டுகிறது.
உங்களுக்குத் . தெரியுமா?
அனைத்து எரிகாரங்களும் காரங்கள் ஆகும். ஆனால் அனைத்துக் காரங்களும் எரிகாரங்கள் அல்ல. எ.கா NaOH
மற்றும் KOH
எரிகாரங்கள் ஆகும். Al(OH)3
, மற்றும் Zn(OH) 3 காரங்கள் ஆகும்
1. காரங்களின் வகைகள்
அ. அமிலத்துவத்தின் அடிப்படையில் காரங்கள்
ஒற்றை அமிலத்துவ காரம்: இவை நீரில் அயனியுற்று ஒரு மூலக்கூறு காரத்திற்கு ஒரு ஹைட்ராக்சைடு அயனியைத் தருபவை. எ.கா: NaOH, KOH
இரட்டை அமிலத்துவக் காரம்: இவை நீரில் அயனியுற்று,
ஒரு மூலக்கூறு காரத்திற்கு இரு ஹைட்ராக்சைடு அயனிகளைத் தருபவை. எ.கா: Ca(OH)2,
Mg(OH) 2
மும்மை அமிலத்துவக் காரம்: இவை நீரில் அயனியுற்று,
ஒரு மூலக்கூறு காரத்திற்கு மூன்று ஹைட்ராக்சைடு அயனிகளைத் தருபவை.
எ.கா: Al(OH)3
Fe(OH)3
ஆ. செறிவின் அடிப்படையில் காரங்கள்
செறிவு மிகு காரங்கள்: இவை நீர்க் கரைசலில்,
அதிக சதவீதம் காரத்தைக் கொண்டுள்ளன.
நீர்த்த காரங்கள்: இவை நீர்க் கரைசலில்,
குறைந்த சதவீதம் காரத்தைக் கொண்டுள்ளன.
இ. அயனியாதல் அடிப்படையில் காரங்கள்
வலிமை மிகு காரங்கள்: இவை நீர்த்த கரைசலில் முழுவதுமாக அயனியுறுகின்றன. எ.கா: NaOH, KOH
வலிமை குறைந்த காரங்கள்: இவை நீர்த்த கரைசலில் பகுதியளவே அயனியுறுகின்றன. எ.கா: NH4OH, Ca(OH)2
உங்களுக்குத் தெரியுமா?
அமிலத்துவம் என்பது ஒரு கார மூலக்கூறிலுள்ள இடப்பெயர்ச்சி செய்யக்கூடிய ஹைட்ராக்சில் தொகுதிகளின் எண்ணிக்கையாகும்.
2. காரங்களின் பண்புகள்
அ) காரங்கள் கசப்புச் சுவை கொண்டவை.
ஆ) நீர்த்த கரைசலில் சோப்பு போன்ற வழவழப்புத் தன்மையைக் கொண்டவை.
இ) சிவப்பு லிட்மஸ் தாளை நீல நிறமாக மாற்றுபவை.
ஈ) இவற்றின் நீர்த்த கரைசல்கள் மின்சாரத்தைக் கடத்தும் திறன் உடையவை.
உ) காரங்கள், உலோகங்களுடன் வினைபுரிந்து உப்பையும், ஹைட்ரஜனையும் தருகின்றன.
Zn
+ 2 NaOH → Na2ZnO2 + H2 ↑
ஊ) காரங்கள், அலோக ஆக்சைடுகளுடன் வினைபுரிந்து உப்பையும், நீரையும் தருகின்றன. இந்த வினையானது அமிலத்திற்கும், காரத்திற்கும் இடையே உள்ள வினை போல உள்ளதால், அலோக ஆக்சைடுகள் அமிலத் தன்மையுடையது என்ற முடிவுக்கு வரலாம்.
Ca(OH)
2 + CO2 → CaCO3 + H2O
எ) காரங்கள், அமிலங்களுடன் வினைபுரிந்து உப்பையும், நீரையும் தருகின்றன.
KOH
+ HCl → KCl + H2O
மேலே குறிப்பிட்ட வினை, காரத்திற்கும் அமிலத்திற்கும் இடையே ஏற்படும் நடுநிலையாக்கல் வினை எனப்படும்.
ஏ) அம்மோனியம் உப்புகளுடன், காரங்களை வெப்பப்படுத்தும்போது, அம்மோனியா வாயு உருவாகிறது.
NaOH
+ NH4Cl → NaCl + H2O + NH3 ↑
உங்களுக்குத் தெரியுமா?
சில உலோகங்கள் சோடியம் ஹைட்ராக்சைடுடன் வினைபுரிவதில்லை . Cu, Ag, Cr.
செயல்பாடு 2
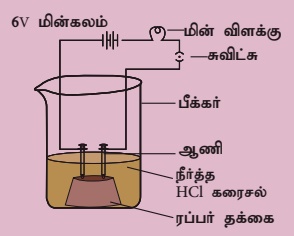
ஹைட்ரோ குளோரிக் அமிலம் (அ) சல்பியூரிக் அமிலத்தை எடுத்துக் கொள்ளவும். ஒரு தக்கையில் இரண்டு ஆணிகளைப் பொருத்தி, அதை 100 மிலி பீக்கரில் வைக்கவும். ஆணிகளை 6V மின்கலத்துடனும், மின் விளக்குடனும் பொருத்த வேண்டும். இப்பொழுது நீர்த்த ஹைட்ரோ குளோரிக் அமிலத்தை பீக்கரில் ஊற்றி, சுவிட்சை அழுத்தவும். மின் விளக்கு ஒளிர்கிறதா? எப்படி? இதே சோதனையை நீர்த்த சல்பியூரிக் அமிலம், குளுக்கோஸ் மற்றும் ஆல்கஹால் கொண்டு செய்யவும். மேற்கண்ட அனைத்து சோதனைகளிலும் மின்விளக்கு எரிகிறதா? ஏன்?
மேற்கண்ட சோதனைகளில் மின் விளக்கானது, அமிலத்தில் மட்டும் ஒளிரும். ஆனால், குளுக்கோஸ் மற்றும் ஆல்கஹால் மின்சாரத்தைக் கடத்தாது. மின்விளக்கு ஒளிர்வது கரைசலின் வழியே மின்சாரம் பாய்கிறது என்பதை உணர்த்துகிறது. மின்சாரமானது அயனிகளின் மூலமாக கரைசலில் எடுத்துச் செல்லப்படுகிறது. இதே சோதனையை காரங்களான சோடியம் ஹைட்ராக்சைடு மற்றும் கால்சியம் ஹைட்ராக்சைடுடன் செய்து பார்க்கவும்.
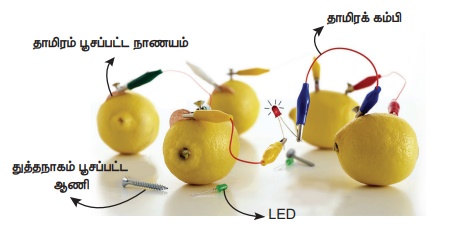
நீங்களாகவே செய்து பார்க்கவும்: படத்தில் காட்டியுள்ளவாறு எலுமிச்சை மின்கலம் அமைக்கவும்.
3. காரங்களின் பயன்கள்
i.
சோப்பு தயாரிக்க சோடியம் ஹைட்ராக்சைடு பயன்படுகிறது.
ii.
கட்டிடங்களுக்கு சுண்ணாம்பு பூச கால்சியம் ஹைட்ராக்சைடு பயன்படுகிறது.
iii.
வயிற்றுக் கோளாறுக்கு மருந்தாக மெக்னீசியம் ஹைட்ராக்சைடு பயன்படுகிறது.
iv. துணிகளில் உள்ள எண்ணெய்க் கறைகளை நீக்குவதற்கு அம்மோனியம் ஹைட்ராக்சைடு பயன்படுகிறது.