செய்முறை, கணக்கீடு, எடுத்துக்காட்டு - டுமாஸ்முறை - நைட்ரஜனை அளந்தறிதல் | 11th Chemistry : UNIT 11 : Fundamentals of Organic Chemistry
11 வது வேதியியல் : அலகு 11 : கரிம வேதியியலின் அடிப்படைகள்
டுமாஸ்முறை - நைட்ரஜனை அளந்தறிதல்
நைட்ரஜனை அளந்தறிதல்:
நைட்ரஜனை அளந்தறிய இருமுறைகள் உள்ளன. அவையாவன 1. டுமாஸ் முறை 2. கெல்டால் முறை.
டுமாஸ்முறை
இம்முறையானது நைட்ரஜனின் சேர்மங்களை, குப்ரிக் ஆக்சைடுடன்,CO2 சூழலில் வெப்படுத்தும்போது தனித்த நைட்ரஜன் வெளிவிடப்படுகிறது என்பதனை அடிப்படையாகக் கொண்டது.
Cx Hy Nz + (2x+y/2) CuO → x CO2 + y/2 H2O + (2x+y/2) Cu + z/2 N2
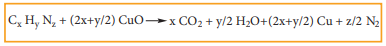
சில நேர்வுகளில் உருவாக வாய்ப்புள்ள சிறிய அளவிலான நைட்ரஜனின் ஆக்சைடுகளை வெப்படுத்தப்பட்ட காப்பர் சுருளின் வழியே செலுத்தி தனிம நிலை நைட்ரஜனாக ஒடுக்கப்படுகிறது.
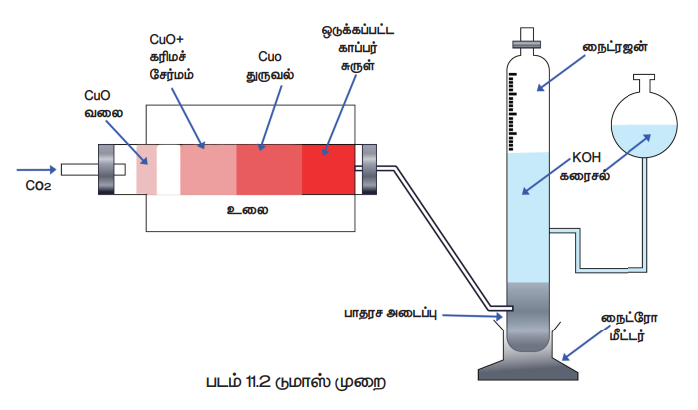
டுமாஸ் முறையில் பயன்படும் உபகரணமானது, CO2 உருவாக்கி, எரிகுழாய், ஷிப்ஸ் நைட்ரோமீட்டர் ஆகியவற்றைக் கொண்டுள்ளது.
CO2 உருவாக்கி:
இம்முறைக்கு தேவைப்படும் கார்பன் டை ஆக்சைடானது மாக்னடைட் அல்லது சோடியம் பை கார்பனேட்டை கடினமான கண்ணாடி குழாயில் வெப்பப்படுத்துவதன் மூலமோ அல்லது கிப்ஸ் உபகரணத்தில் உள்ள சுண்ணாம்பு கல்லின் மீது நீர்த்த HCl ஐ வினைபுரிய செய்வதன் மூலமாகவோ, பெறப்படுகிறது. இந்த CO2 வாயுவானது அடர் H2SO4 வழியே செலுத்தி உலரவைக்கப்பட்டு பின் எரிக்குழாயினுள் செலுத்தப்படுகிறது.
எரிகுழாய்: இக்குழாய் உலையினுள் வைத்து வெப்பபடுத்தப்படுகிறது. இது i) ஆக்ஸிஜனேற்றம் செய்யப்பட்ட காப்பர் சுருளால் நிரப்பப்பட்டுள்ளது. இது எரிதலால் உருவாகும் விளை பொருட்கள் பின்னோக்கி மீளவும் விரவுதலை தடுக்க பயன்படுகிறது. மேலும் கதிர்வீச்சின் மூலம் CuO உடன் சேர்த்து வெப்பப்படுத்த பயன்படுகிறது. ii) எடை அறிந்த கரிமச் சேர்மம் அதிக அளவு CuO உடன் கலக்கப்பட்டு வைக்கப்பட்டுள்ளது. iii) சொரசொரப்பான காப்பர் ஆக்சைடானது குழாயின் நீளத்தில் மூன்றில் இருபங்கு முழுநீளத்திற்கு தளர்வான கல்நாருடன் இருபுறமும் பொதியப்பட்டுள்ளது. இதன் வழி கடந்து செல்லும் கரிம சேர்ம ஆவிகளை இது ஆக்ஸிஜனேற்றம் செய்கிறது. iv) நைட்ரஜன், எரிக்கப்படும்போது ஏதேனும் நைட்ரஜன் ஆக்சைடுகள் உருவானால் அதனை ஒடுக்க ஒடுக்கப்பட்ட காப்பர் சுருள் உள்ளது.
ஷிப்ஸ் நைட்ரோமீட்டர்: எரிகுழாயில் சிதைவுற்ற கரிம சேர்மத்திலிருந்து நைட்ரஜனுடன் குறிப்பிட தகுந்த அதிக அளவு CO2 உடன் கலக்கப்படுகிறது. பின் நைட்ரோ மீட்டரில் செலுத்தும் போது, CO2 ஆனது KOHஆல் உறிஞ்சப்படும். மேற்புறத்திலுள்ள அளவீடுகள் உடைய குழாயில் நைட்ரஜனானது சேகரிக்கப்படுகிறது. (படம்: 11.2)
செய்முறை: முதலில் நைட்ரோ மீட்டர் உள்ளகுழாய் திறக்கப்பட்டு, எரிகுழாயினுள் உள்ள காற்றை நீக்க CO2 செலுத்தப்படுகிறது. வெளியேறும் CO2 ஆனது பொட்டாஷ் கரைசலின் வழியே செல்லும்போது முழுவதும் உறிஞ்சப்படுகிறது. எனவே மேற்பகுதியினை அடைவதில்லை. இதிலிருந்து எரிகுழாயில் உள்ள காற்று முழுவதும் வெளியேறியுள்ளது என அறியலாம். பின் நைட்ரோமீட்டரின் சேமிப்புக்கலன் கீழ் இறக்கப்பட்டு KOH கரைசலால் நிரப்பப்பட்டு குழாய் அடைக்கப்படுகிறது. எரிகுழாய் உலையில் வைத்து சூடுபடுத்தப்பட்டு வெப்பநிலை சீராக உயர்த்தப்படுகிறது. சேர்மத்திலுள்ள வெளியேறும் தனித்த நைட்ரஜன் நைட்ரோ மீட்டரில் சேகரிக்கப்படுகிறது. எரிதல் நிறைவுற்ற பின் குழாயினுள் ஏதேனும் சிறிதளவு நைட்ரஜன் இருப்பின் அதனை நீக்கும் பொருட்டு விரைவாக CO2 செலுத்தப்படுகிறது. அளவீட்டுக் குழாயில் உள்ள அளவீடும், கலவைகள் அளவீடும் சமமாக இருக்கும் வகையில் சேமிப்புக்கலனை சரிசெய்து சேகரிக்கப்பட்ட வாயுவின் கன அளவு குறித்துக்கொள்ளப்படுகிறது.
கணக்கீடு:
கரிமச் சேர்மத்தின் எடை = wg
ஈரமான நைட்ரஜனின் கன அளவு= V1L
அறை வெப்பநிலை = T1 K
வளிமண்டல அழுத்தம் = P mm Hg
அறைவெப்பநிலையில் நீராவி அழுத்தம் = P1 mm Hg
உலர் நைட்ரஜனின் அழுத்தம் = (P-P1) = P1 mm Hg.
STP, உலர் நைட்ரஜனின் அழுத்தம், கனஅளவு மற்றும் வெப்பநிலை முறையே P0 V0 மற்றும் T0 என்க.
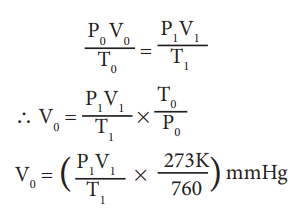
நைட்ரஜனின் சதவீதம் கணக்கிடுதல்
STP ல் 22.4L N2 ன் நிறை 28g
ஃ STP ல் V0 L N2 ன் நிறை 28/22.4 × V0
Wg கரிமச்சேர்மத்தில் (28/22.4 × V0/W)g நைட்ரஜன் உள்ளது
ஃ நைட்ரஜனின் % = (28/22.4 × V0/W) × 100

எடுத்துக்காட்டு: 0.1688g எடையுள்ள சேர்மம் டுமாஸ் முறையில் பகுப்பிற்கு உட்படும்போது 140C, 758 mm Hg யில் 31.7ml ஈரமான நைட்ரஜனை தருகிறது, எனில் அச்சேர்மத்தில் உள்ள நைட்ரஜனின் சதவீதத்தினை கணக்கிடுக.
கரிமச் சேர்மத்தின் எடை = 0.168g
ஈரமான நைட்ரஜனின் கன அளவு (V1) = 31.7mL
= 31.7 × 10-3 L
வெப்பநிலை (T1) = 14°C
= 14 + 273
= 287K
ஈரமான நைட்ரஜனின் அழுத்தம் = 758 mm Hg
14°C யில் நீர்ம அழுத்தம் = 12 mm of Hg
ஃ உலர் நைட்ரஜனின் அழுத்தம் = (P-P1)
= 758 – 12
= 746 mm Hg

= 21.90%