செய்முறை, கணக்கீடு, எடுத்துக்காட்டு - சல்பரை அளந்தறிதல் | 11th Chemistry : UNIT 11 : Fundamentals of Organic Chemistry
11 வது வேதியியல் : அலகு 11 : கரிம வேதியியலின் அடிப்படைகள்
சல்பரை அளந்தறிதல்
சல்பரை அளந்தறிதல்:
காரியஸ்முறை: எடை அறிந்த கரிமச்சேர்மம் புகையும் HNO3 - உடன் நன்கு வெப்பப்படுத்தப்படுகிறது. C மற்றும் H ஆகியன முறையே CO2 மற்றும் H2O ஆக ஆக்ஸிஜனேற்றம் அடைகின்றன. அதே நேரத்தில் சல்பர் பின்வரும் வினையின் குறிப்பிட்டுள்ளவாறு சல்பியூரிக் அமிலமாக ஆக்ஸிஜனேற்றம் அடைகிறது.
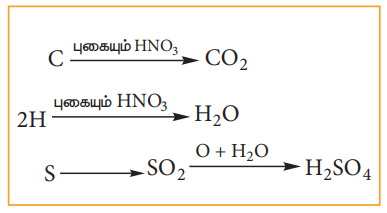
உருவான கரைசலுடன் அதிகளவு BaCl2 கரைசல் சேர்க்கப்படுகிறது. கரைசலில் உள்ள H2SO4 ஆனது BaSO4, ஆக மாற்றப்படுகிறது. BaSO4 - ன் எடையிலிருந்து, சல்பரின் எடை மற்றும் அதன் சதவீதம் கணக்கிடப்படுகிறது.
செய்முறை எடை தெரிந்த கரிமச்சேர்மத்துடன் சில துளிகள் புகையும் HNO3 சேர்க்கப்பட்டு தூய காரியஸ் குழாயில் எடுத்து கொள்ளப்படுகிறது. குழாய் மூடப்பட்டு பின்னர் இரும்பு குழாயில் வைக்கப்பட்டு 5 மணி நேரம் வரை வெப்பபப்படுத்தப்படுகிறது. பிறகு, காரியஸ் குழாய் குளிர்விக்கப்பட்டு சிறு துளையிடப்படுகிறது. இத்துளையின் வழியே குழாயின் உள்ளே உருவான வாயுக்கள் வெளியேற்றப்படுகின்றன. பின்பு காரியஸ் குழாய் உடைக்கப்பட்டு அதில் உள்ள விளைபொருட்கள் பீக்கரில் சேகரிக்கப்படுகின்றது. இவ்வினையில் உருவான H2SO4 உள்ள பீக்கரில் BaCl2 கரைசல் சேர்க்கப்படுகிறது. BaSO4 ஆனது வீழ்படிவாகிறது. வீழ்படிவான BaSO4 ஆனது வடிகட்டப்பட்டு, கழுவப்பட்டு உலர்த்தி பின் எடையறிப்படுகிறது. BaSO4 ன் எடையிலிருந்து, கந்தகத்தின் (S) சதவீதம் கணக்கிடப்படுகிறது.
கரிம சேர்மத்தின் எடை = w g
உருவான BaSO4 ன் எடை = x g
233g BaSO4 ல் உள்ள சல்பரின் எடை = 32 g
x g BaSO4 ல் (32/233 × x) g S உள்ளது
எனவே w g கரிம சேர்மத்திலுள்ள சல்பரின் (S) %
= (32/233 × x/w × 100)%
எடுத்துக்காட்டு – 2
காரியஸ் முறைப்படி அளந்தறிதலில், 0.2175 g நிறையுள்ள சல்பரைக் கொண்டுள்ள கரிமச் சேர்மம் ஆனது 0.5825g BaSO4 யைக் கொடுக்கிறது எனில் அச்சேர்மத்தில் உள்ள S ன் சதவீதத்தினை கணக்கிடுக.
கரிம சேர்மத்தின் எடை= 0.2175 g
BaSO4 ன் எடை = 0.5825 g
233 g BaSO4 ல் உள்ள S ன் எடை = 32 g
0.5825 g BaSO4 ல் உள்ள
S ன் எடை = (32/233) × 0.5825
S ன்% = (32/233) × ( 0.5825/0.2175) × 100
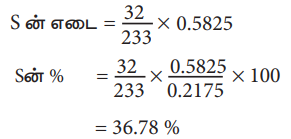
= 36.78 %