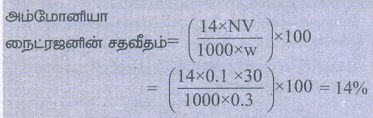கணக்குகளுக்கான தீர்வுகள் - தன் மதிப்பீடு - வேதியியல்: இயற் மற்றும் வேதிச்சமநிலை | 11th Chemistry : UNIT 11 : Fundamentals of Organic Chemistry
11 வது வேதியியல் : அலகு 11 : கரிம வேதியியலின் அடிப்படைகள்
தன் மதிப்பீடு - வேதியியல்: இயற் மற்றும் வேதிச்சமநிலை
தன் மதிப்பீடு
1. பின்வரும் கரிமச் சேர்ம வகைகளுக்கு ஒவ்வொன்றிற்கும் இரு எடுத்துக்காட்டுகள் தருக.
i. பென்சீன் வளைய அமைப்பை பெற்றிருக்காத அரோமேட்டிக் சேர்மம்.
தீர்வு:
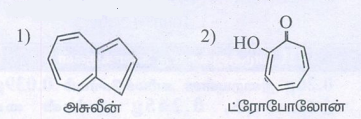
ii. அரோமேட்டிக் பல்லின வளையச் சேர்மம்
தீர்வு:
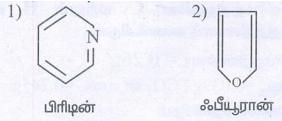
iii. திறந்த அமைப்புடைய அலிசைக்ளிக் மற்றும் அலிபாட்டிக் சேர்மங்கள்
தீர்வு:
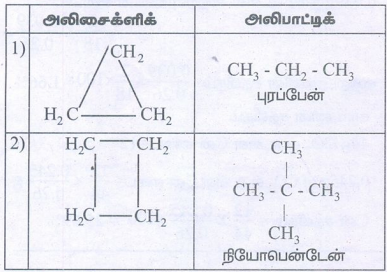
தன்மதிப்பீடு
2. பின்வரும் சேர்மங்களுக்கு வடிவ வாய்ப்பாடுகளை எழுதுக.
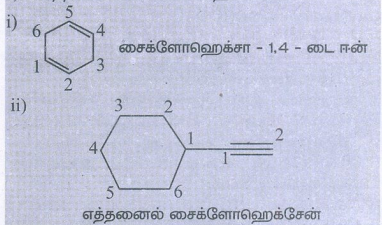
i. சைக்ளோ ஹெக்ஸா-1, 4-டையீன்
ii. எத்தைனைல் சைக்ளோ ஹெக்ஸேன்
தீர்வு:
தன்மதிப்பீடு
3) பின்வரும் சேர்மங்களுக்கு வடிவ வாய்பாடுகளை எழுதுக.
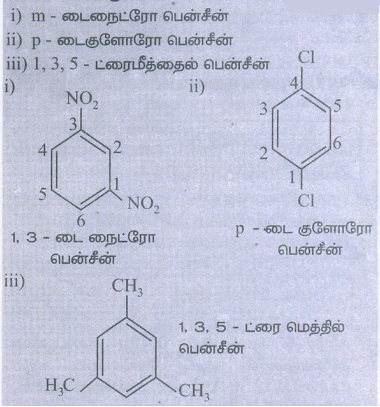
i. m-டைநைட்ரோ பென்சீன்
ii. P-டைகுளோரோ பென்சீன்
iii. 1,3,5-ட்ரைமீத்தைல் பென்சீன்
தீர்வு:
தன் மதிப்பீடு
4. C4H10O என்ற மூலக்கூறு வாய்ப்பாட்டினைப் பெற்றுள்ள சாத்தியமான மாற்றியங்கள் அனைத்தையும் எழுதுக அவைகளில் காணப்படும் மாற்றியங்களைக் கண்டறிக.
தன்மதிப்பீடு
5. C H மற்றும் O ஆகியனவற்றை கொண்டுள்ள 0.2346g எடையுள்ள கரிமச்சேர்மம் எரிக்கப்படும்போது, 0.2754g நீர் மற்றும் 0.4488g CO2 யை ஆகியவற்றை தருகிறது எனில் அச்சேர்மத்திலுள்ள CH மற்றும் O ன் % இயைபினைக் காண்க.
தீர்வு:
கரிம சேர்மத்தின் நிறை (w) = 0.2346g
நீரின் நிறை (x) = 0.2754g CO2 ன் நிறை (y) = 0.4488g
கார்பனின் சதவிகிதம் = 12/44 × y/w × 100
= 12/44 × 0.4488/0.2346 × 100 = 52.17%
நைட்ரஜனின் சதவிகிதம் = 2/18 × x/w × 100
= 2/18 × 0.2754/0.2346 × 100 = 13.04%
ஆக்ஸிஜனின் சதவிகிதம் = [100-(52.17 + 13.04)]
= 100 - 65.21 = 34.79%
தன்மதிப்பீடு
6. 0.16g எடையுள்ள கரிமச் சேர்மம், காரியஸ் குழாயில் சூடுபடுத்தப்படுகிறது. உருவான H2SO4 ஆனது BaCl2 உடன் சேர்த்து வீழ்படிவாக்கப்படுகிறது. வீழ்படிவான BaSO4 ன் நிறை 0.35g. சல்பரின் நிறை சதவீதத்தை காண்க.
தீர்வு:
கரிம சேர்மத்தின் நிறை (W) = 0.16g
பேரியம் சல்பேட்டின் நிறை (x) = 0.35g
சல்பரின் சதவீதம் = 32/233 × x/w × 100
= 32/233 × 0.35/0.16 × 100 = 30.04%
தன்மதிப்பீடு
1) 0.185g எடையுள்ள கரிமச்சேர்மம், அடர் HNO3 மற்றும் சில்வர் நைட்ரேட்டுன் சேர்ந்து 0.320g வெள்ளி புரோமைடை தந்தது எனில், அதில் உள்ள புரோமினின் % காண்க (Ag = 108, Br = 80)
தீர்வு:
கரிம சேர்மத்தின் நிறை (w) = 0.185g
சில்வர் புரோமைடின் நிறை (x) = 0.320g
புரோமினின் சதவீதம் =
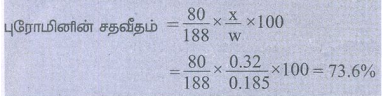
2) காரியஸ் முறையில் 0.40g எடையுள்ள அயோடினால் பதிலீடு செய்யப்பட்ட கரிம சேர்மம் 0.125g AgI யை தருகிறது எனில், அயோடினின் நிறை சதவீதத்தைக் காண்க.
தீர்வு:
கரிம சேர்மத்தின் நிறை (w) = 0.40g
சில்வர் அயோடைடின் நிறை (x) = 0.235g
அயோடினின் சதவீதம் = 127/235 × x/w × 100
= 127/235 × 0.235/0.40 × 100 = 31.75%
தன்மதிப்பீடு
9. பாஸ்பரஸை கொண்டுள்ள 0.33g எடையுள்ள கரிமச் சேர்மம் 0.397g Mg2P2O7 வீழ்படிவைத் தந்தது எனில், அச்சேர்மத்தில் உள்ள P இன் சதவீதத்தினைக் கணக்கிடுக.
தீர்வு:
கரிம சேர்மத்தின் நிறை (w) = 0.33g
Mg2P2O7ன் நிறை (x) = 0.397g
பாஸ்பரஸின் சதவீதம் =
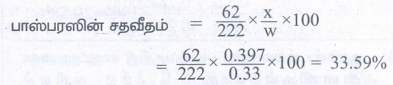
தன்மதிப்பீடு
0.3g எடையுள்ள கரிமச் சேர்மம், கெல்டால் முறையில் தந்த அமோனியா வாயுவை நடுநிலையாக்க 30ml 0.1 N H2SO4 தேவைப்பட்டது எனில் அச்சேர்மத்திலுள்ள நைட்ஜனின் சதவீதத்தினைக் காண்க
தீர்வு:
கரிமச் சேர்மத்தின் நிறை (w) = 0.3 g
சல்ஃபியூரிக் அமிலத்தின் நிறை (N) = 0.1N
சல்ஃபியூரிக் அமிலத்தின் கனஅளவு (V) = 30 mL
30ml 0.1 N சல்ஃபியூரிக் அமிலம் = 30ml 0.1 N அம்மோனியா
அம்மோனியா நைட்ரஜனின் சதவீதம் = (14 × NV/1000 × w) × 100
= (14 × 0.1 × 30/1000 × 0.3) × 100 = 14%