11 வது வேதியியல் : அலகு 9 : கரைசல்கள்
பாடச்சுருக்கம்: கரைசல்கள்
பாடச்சுருக்கம்
● இரண்டு அல்லது அதற்கு மேற்பட்ட வேதிவினை புரியாத ஒன்றோடொன்று சீராக கலந்துள்ள பொருள்களின் ஒருபடித்தான கலவை கரைசல் எனப்படுகிறது. கரைசலில் அதிக அளவுள்ள பகுதிப்பொருள் கரைப்பான் எனவும், குறைவாக உள்ள பகுதிப்பொருள் கரைபொருள் எனவும் அழைக்கப்படுகின்றன.
● கரைசலின் செறிவை குறிப்பிட பல்வேறு செறிவு அலகுகள் பயன்படுத்தப்படுகின்றன. அவையாவன மோலாலிட்டி, மோலாரிட்டி, நார்மாலிட்டி, மோல்பின்னம், பார்மாலிடி, நிறை/நிறை கரைசல் (w/w%), நிறை/ கனஅளவு கரைசல் (w/v%), கனஅளவு/ கனஅளவு கரைசல் (v/v%), கரைபொருளின் அளவானது மிகவும் குறைவாக இருப்பின் செறிவினை குறிப்பிட மில்லியனில் ஒரு பகுதி (ppm) என்ற அலகு பயன்படுத்தப்படுகிறது.
● திட்டக் கரைசல் தயாரிக்கப்பட்டு, அதனை நீர்த்தல் செய்து தேவையான செறிவுள்ள பயன்பாட்டுக் கரைசலைத் தயாரிக்கலாம். எடையிடுதலால் ஏற்படும் பிழைகளை இதன் மூலம் தவிர்க்கலாம்.
● ஒரு தெவிட்டிய கரைசலில் 100g கரைப்பானில் கரைந்துள்ள கரைபொருளின் அளவானது கரைதிறன் எனப்படும். இது கரைபொருள், கரைப்பான் மற்றும் வெப்பநிலை ஆகியனவற்றினைப் பொறுத்து அமைகிறது.
● ஒரு நீர்மத்தில் ஒரு வாயுவின் கரையும் திறனானது அவ்வாயுவின் அழுத்தம். திரவத்தின் தன்மை மற்றும் அமைப்பின் வெப்பநிலை ஆகியனவற்றைப் பொறுத்து அமையும்.
● ஒரு திரவத்தில் ஒரு வாயுவின் கரைதிறன் மீதான அழுத்தத்தால் ஏற்படும் விளைவினை ஹென்றி விதி தருகிறது. இவ்விதிப்படி "ஆவி நிலைமையிலுள்ள வாயுவின் பகுதி அழுத்தமானது (கரைபொருளின் ஆவி அழுத்தம்) கரைசலிலுள்ள வாயுநிலைக் கரைபொருளின் மோல்பின்னத்திற்கு(x), நேர் விகிதத்திலிருக்கும்".
● ஒரு நீர்மத்தின் ஆவிஅழுத்தம் என்பது அந்த நீர்மமானது அதன் ஆவியுடன் இயங்குச் சமநிலையின் ஒரு மூடிய அமைப்பில் உள்ள போது அதன் ஆவியினால் ஏற்படுத்தப்படும் அழுத்தம் எனப்படுகிறது.
● ரௌல்ட் விதிப்படி "எளிதில் ஆவியாகும் திரவங்களைக் கொண்ட கரைசல்களில், கரைசலிலுள்ள ஒவ்வொரு கூறின் ஆவி அழுத்தமும், அதன் மோல் பின்னத்துடன் நேர் விகிதத்திலிருக்கும்" ரௌல்ட் விதியினால் தீர்மானிக்கப்பட்ட ஆவி அழுத்தத்தை விட குறைவான ஆவி அழுத்தத்தைப் பெற்றுள்ள கரைசல்கள் எதிர் விலகலை கொண்டுள்ளன. எடுத்துக்காட்டு: (அசிட்டோன் + குளோரோபார்ம் கரைசல்).
● ரௌல்ட் விதியினால் தீர்மானிக்கப்பட்ட ஆவி அழுத்தத்தை விட அதிகமான ஆவி அழுத்தத்தைப் பெற்றுள்ள கரைசல்கள் நேர் விலகலை கொண்டுள்ளன. எடுத்துக்காட்டு : (அசிட்டோன் + பென்சீன்)
● கரைசலில் காணப்படும் துகள்களின் எண்ணிக்கையினை மட்டுமே பொருத்து அமைந்து, அத்துகள்களின் தன்மையினைப் பொருத்து அமையாத பண்புகள் தொகைசார் பண்புகள் எனப்படும்
(அ) ஒப்பு ஆவி அழுத்தக்குறைவு
● எளிதில் ஆவியாகாத ஒரு கரைபொருளை ஒரு தூய கரைப்பானில், கரைக்கும்போது, தூயகரைப்பானின் ஆவிஅழுத்தம் குறையும்
● “ஒரு குறிப்பிட்ட வெப்பநிலையில், எளிதில் ஆவியாகாத கரைபொருளைக் கொண்டுள்ள ஒரு நல்லியல்பு கரைசலின் ஒப்பு ஆவிஅழுத்தக்குறைவானது, கரைபொருளின் மோல் பின்னத்திற்கு சமம்"
(ஆ) கொதி நிலை ஏற்றம்
● எந்த ஒரு வெப்பநிலையில் திரவத்தின் ஆவி அழுத்தமானது வளிமண்டல அழுத்தத்திற்கு சமமாகிறதோ அவ்வெப்பநிலையானது, அத்திரவத்தின் கொதிநிலை எனப்படும். எளிதில் ஆவியாகாத கரைபொருளை தூய கரைப்பானுடன், அதன் கொதிநிலையில் சேர்க்கும்போது அதன் ஆவிஅழுத்தம் 1 atm க்கு கீழாக குறைகிறது. மீண்டும் ஆவிஅழுத்தத்தை 1 atm க்கு கொண்டுவரவேண்டுமானால், கரைசலின் வெப்பநிலை உயர்த்தப்படவேண்டும். இதன் விளைவாக, கரைசலானது, தூய கரைப்பானின் கொதிநிலையைவிட (Tbo) அதிக கொதிநிலையில் (Tb) கொதிக்கிறது.
(இ) உறை நிலை தாழ்வு
● எளிதில் ஆவியாகாத கரைபொருளை கரைப்பானுடன் அதன் உறைநிலையில் சேர்க்கும்போது, கரைசலின் உறைநிலையானது குறைகிறது. உறைநிலையில், பொருளின், திட மற்றும் திரவ நிலைமைகள் சமநிலையில் உள்ளன.
(ஈ) சவ்வூடுபரவுதல்
● சவ்வூடு பரவல் என்பது ஒரு கூறு புகவிடும் சவ்வின் வழியாக, கரைப்பான் மூலக்கூறுகள் செறிவு குறைந்த கரைசலிலிருந்து, செறிவு மிகுந்த கரைசலுக்கு விரவிச் செல்லும் தன்னிச்சையான நிகழ்வு ஆகும்.
(உ) சவ்வூடு பரவுதல் அழுத்தம்
● சவ்வூடு பரவல் அழுத்தத்தை, “ஒருகூறுபுகவிடும் சவ்வின் வழியே, கரைப்பான் புகுதலை தடுப்பதற்காக, (சவ்வூடுபரவலை தடுக்க) கரைசலின் மீது செலுத்தப்படவேண்டிய அழுத்தம்” என வரையறுக்க முடியும்.
அசாதரண பண்புகள்
கரைபொருள்கள் கரைசல்களில் பிரிகையடைந்தாலோ அல்லது இணைந்தாலோ அசாதரண தொகைசார் பண்புகளை பெற்றுவிளங்கும் வாண்ட் ஹாஃப் காரணியினை கொண்டு பிரிகை மற்றும் இணையும் காரணிகளை அளவிடமுடியும்.
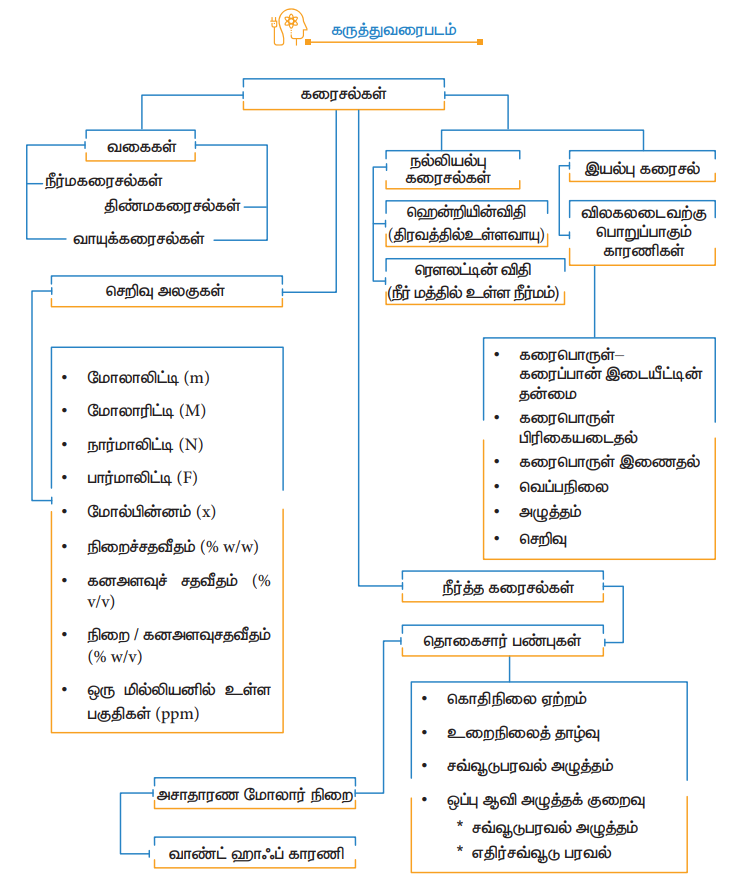
கருத்துவரைபடம்
இணையச் செயல்பாடு
சவ்வூடு பரவல்
இச்செயல்முறையை பயன்படுத்துவதன் மூலம் சவ்வூடு பரவல் மாதிரி செயல்முறையை நீங்கள் காணலாம். இது செயல்முறை குறித்த தெளிவான புரிதலை அளிக்கும்.
https://pbs1m=contrib.s3.amazonaws.com/WGBH/arct15/ SimBucket/Simulations/osmosis/ content/index.html
உரலிக்குச் செல்க அல்லது வலது புறத்தில் உள்ள விரைவுத் துலக்கக் குறியீட்டினை (QR code) ஸ்கேன் செய்க.
நிலைகள்:
● இணையப் பக்கத்தினை திறந்து, கொடுக்கப்பட்ட உரலியை (URL) தட்டச்சு செய்க (அல்லது) விரைவுத் துலக்கக் குறியீட்டினை (QR code) ஸ்கேன் செய்க.
● நீங்கள், தற்போது கீழே காட்டப்பட்டுள்ளவாறு வலைப்பக்கத்தினை காண்பீர்கள்.
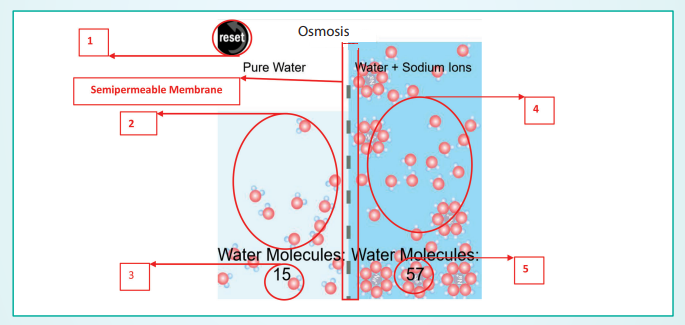
● இரண்டு பகுதிகள் ஒருகூறுபுகவிடும் சவ்வினால் பிரிக்கப்பட்டுள்ளன.
● இடப்புறபகுதியானது (பெட்டி 2) தூய கரைப்பானைக் கொண்டுள்ளது, மேலும் வலப்புறப் பகுதியானது கரைசலை (கரைபொருள் +நீர்) கொண்டுள்ளது.
● ஒவ்வொரு பகுதியிலும் உள்ள கரைப்பான் (நீர்) மூலக்கூறுகளின் எண்ணிக்கையானது பெட்டி 3 மற்றும் பெட்டி 5 என குறிப்பிடப்பட்டுள்ள பரப்புகளில் காட்டப்பட்டுள்ளது.
● நீங்கள் இப்போது, நீர் மூலக்கூறுகள் கரைப்பான் பகுதியிலிருந்து ஒருகூறுபுகவிடும் சவ்வின்வழியாக கரைசல் பகுதிக்கு நகர்வதைக் காண முடியும்.
● நீங்கள் பெட்டி 1ல் உள்ள reset பொத்தானை அழுத்துவதன்மூலம், உருவகப்படுத்துதலை மீண்டும் தொடங்க முடியும்