11 வது வேதியியல் : அலகு 9 : கரைசல்கள்
திரவத்தில் திண்மம் கரைந்துள்ள இருகூறுக் கரைசலின் ஆவிஅழுத்தம்
திரவத்தில் திண்மம் கரைந்துள்ள இருகூறுக் கரைசலின் ஆவிஅழுத்தம்
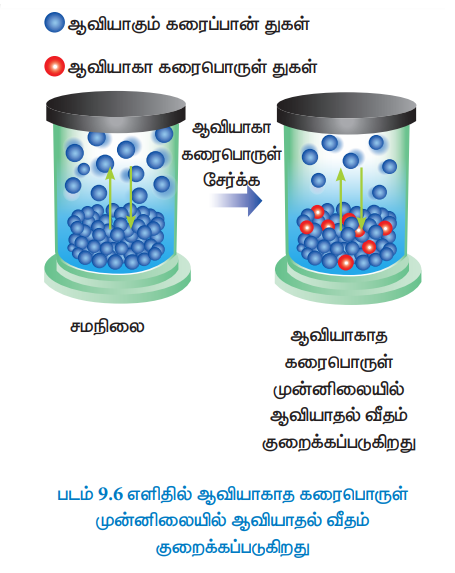
ஒரு தூய கரைப்பானில், எளிதில் ஆவியாகாத கரைபொருளைக் கரைக்கும் போது, தூய கரைப்பானின் ஆவி அழுத்தம் குறையும். இத்தகைய கரைசல்களில், கரைபொருள் எளிதில் ஆவியாகாததால், கரைசலின் ஆவிஅழுத்தமானது, கரைப்பான் மூலக்கூறுகளை மட்டுமே பொறுத்து அமையும்.
எடுத்துக்காட்டாக, சோடியம் குளோரைடை நீரில் கரைக்கும்போது, உப்புக் கரைசலின் ஆவிஅழுத்தம் குறைகிறது. எந்தஒரு நேரத்திலும் கரைசலின் மேற்பரப்பில் காணப்படும் கரைப்பான் மூலக்கூறுகளின் எண்ணிக்கை ஆனது கரைசலின் ஆவி அழுத்தத்தினை நிர்ணயிக்கிறது மேலும் கரைசலின் ஆவி அழுத்தம் கரைப்பானின் மோல் பின்னத்திற்கு நேர் விகிதத்தில் அமையும்.
இங்கு XB என்பது கரைபொருளின் மோல் பின்னம்
(∵ XA + XB = 1, XB = 1 – XA)
மேற்கண்ட சமன்பாடானது, ஒப்பு ஆவிஅழுத்தக் குறைவைத் தருகிறது. இச்சமன்பாட்டை அடிப்படையாகக் கொண்டு, “ஒரு குறிப்பிட்ட வெப்பநிலையில், எளிதில் ஆவியாகாத கரைபொருளைக் கொண்டுள்ள ஒரு நல்லியல்பு கரைசலின் ஒப்பு ஆவிஅழுத்தக்குறைவானது, கரைபொருளின் மோல் பின்னத்திற்கு சமம்” எனவும் ரௌல்ட் விதியைக் கூறலாம்.
ரௌல்ட் விதி மற்றும் ஹென்றி விதி ஆகியவற்றை ஒப்பிடுதல்
ரௌல்ட் விதிப்படி, எளிதில் ஆவியாகாத கரைபொருளைக் கொண்டுள்ள கரைசலுக்கு
Pகரைபொருள் = P°கரைபொருள் Xகரைபொருள் ---- (9.17)
ஹென்றி விதிப்படி:
Pகரைபொருள் = KHXகரைசலில் உள்ள கரைபொருள். ----- (9.18)
மேற்காண் இரண்டு சமன்பாடுகளுக்கு இடையே உள்ள வேறுபாடு, விகித மாறிலி (ரௌல்ட் விதி) மற்றும் KH (ஹென்றி விதி) மட்டுமே ஆகும். திரவ கரைப்பானில், வாயுநிலை கரைபொருளை கொண்டுள்ள கரைசல்களுக்கு ஹென்றி விதி பொருந்தும், அதேசமயம் திரவ கரைப்பானில், எளிதில் ஆவியாகாத திண்ம கரைபொருளை கொண்டுள்ள கரைசல்களுக்கு ரௌல்ட் விதி பொருந்தும். கரைபொருளானாது எளிதில் ஆவியாகாததாக இருந்தால், ஹென்றி விதி மாறிலியானது. தூய கரைப்பானின் ஆவிஅழுத்தத்திற்கு (PAo) சமமாகிறது. அதாவது, ரௌல்ட் விதியானது ஹென்றி விதியின் சிறப்பு நிகழ்வாகிறது. மிக நீர்த்த கரைசல்களில், கரைப்பான் ஆனது ரௌல்ட் விதிக்கு உட்படுகிறது. மேலும் கரைபொருளானாது ஹென்றி விதிக்கு உட்படுகிறது.