இயற்பியல் பண்புகள், வேதியியல் பண்புகள்,அமிலங்களின் பயன்கள் - அமிலங்கள் | 8th Science : Chapter 14 : Acids and Bases
8 ஆம் வகுப்பு அறிவியல் : அலகு 14 : அமிலங்கள் மற்றும் காரங்கள்
அமிலங்கள்
அமிலங்கள்
அமிலம் என்ற சொல்லானது புளிப்பு எனப் பொருள்படும் 'அசிடஸ்' என்ற
இலத்தீன் மொழிச் சொல்லில் இருந்து வருவிக்கப்பட்டது. எனவே, புளிப்புச்சுவை பொதுவாக
அமிலங்கள் எனப்படுகின்றன. அனைத்து அமிலங்களும் ஒன்று அல்லது அதற்கு மேற்பட்ட இடப்பெயர்ச்சி
செய்யத்தக்க ஹைட்ரஜன் அணுக்களைப் பெற்றுள்ளன. மேலும், அவற்றை நீரில் கரைக்கும்பொழுது
ஹைட்ரஜன் அயனிகளை (H+)அவை வெளியிடுகின்றன. எடுத்துக்காட்டாக, ஹைட்ரோகுளோரிக் அமிலம்
(HCI), சல்பியூரிக் அமிலம் (H,SO) மற்றும் நைட்ரிக் அமிலம் (HNO ). ஆகியவற்றை நீரில்
கரைக்கும் பொழுது ஹைட்ரஜன் அயனிகளை (H+) அவை கொடுக்கின்றன.
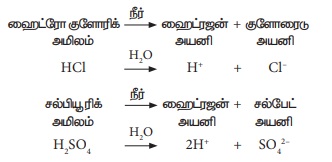
எனவே, நீரில் கரையும்போது ஹைட்ரஜன் அயனிகளை வெளியிடும் வேதிச்சேர்மங்கள்
அமிலங்கள் என வரையறுக்கப்படுகின்றன.
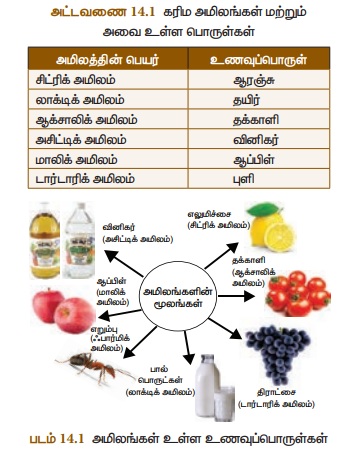
அமிலங்களை அவற்றின் மூலங்களைப் பொருத்து கரிம மற்றும் கனிம அமிலங்கள்
என வகைப்படுத்தலாம். சில அமிலங்கள் பழங்கள் மற்றும்
ஸ்வீடன்
நாட்டு வேதியியலாளர் அர்ஹீனியஸ் அமிலங்கள் பற்றிய ஒரு கொள்கையை முன் வைத்தார். அவரின்
கூற்றுப்படி அமிலம் என்பது நீர்க்கரைசலில் H+ அயனிகள் அல்லது H3Oஅயனிகளைத்
தரும் வேதிப்பொருளாகும்.

மாறாக, தொழிற்சாலைகளில் அமிலங்கள் செயற்கையாக உற்பத்தி செய்யப்படுகின்றன.
இந்த அமிலங்கள் கனிம அமிலங்கள் எனப்படும். எ.கா. ஹைட்ரோகுளோரிக் அமிலம் (HCI), சல்பியூரிக்
அமிலம் (H,SO) நைட்ரிக் அமிலம் (HNO ) அமிலங்களை மேலும் பலவகையாக வகைப்படுத்த இயலும்.
அவற்றைப் பற்றி நீங்கள் உயர் வகுப்புகளில் கற்க இருக்கிறீர்கள்.
1. அமிலங்களின்
பண்புகள்
அ. இயற்பியல் பண்புகள்
• அமிலங்கள் புளிப்புச்சுவை கொண்டவை.
• அமிலங்கள் நிறமற்றவை.
• அமிலங்கள் அரிக்கும் தன்மை கொண்டவை. மேலும், வலிமையான அமிலங்கள்
மனிதர்களின் தோல், துணி மற்றும் காகிதத்தைப் பாதிக்கின்றன.
• பொதுவாக அமிலங்கள் திரவ நிலையில் காணப்படும். ஒருசில அமிலங்கள்
திண்ம நிலையிலும் உள்ளன. எ.கா. பென்சாயிக் அமிலம்.
• அமிலங்கள், நிறங்காட்டிகளின் நிறத்தை மாற்றுகின்றன. நீல லிட்மஸ்
தாளை சிவப்பாகவும், மெத்தில் ஆரஞ்சு கரைசலை சிவப்பாகவும் மாற்றுகின்றன.
• அமிலங்கள் நீரில் நன்கு கரைகின்றன.
• அமிலங்களின் நீர்க் கரைசல் மின்சாரத்தைக் கடத்துகிறது.

நமது
வயிற்றில் சுரக்கும் நமக்கு ஹைட்ரோகுளோரிக் அமிலம் நமது வயிற்றின் உட்புறத்தை அரிப்பதால்
பசியுணர்வு ஏற்படுகிறது. ஹைட்ரோகுளாரிக் அமிலத்தின் சுரக்கும் அளவு அதிகரித்தால் வயிற்றுப்புண்
தோன்றக்கூடும்.
ஆ. வேதியியல் பண்புகள்
i. உலோகங்களுடன்
வினை
துத்தநாகம், மெக்னீசியம், அலுமினியம் மற்றும் இரும்பு போன்ற
உலோகங்கள் ஹைட்ரோகுளோரிக் அமிலம் மற்றும் சல்பியூரிக் அமிலத்துடன் (கந்தக அமிலம்) வினைபுரிந்து
உலோக உப்புகளையும் ஹைட்ரஜன் வாயுவையும் தருகின்றன.

செயல்பாடு 1
தாங்கியுடன்
கூடிய ஒரு சோதனைக் குழாயினை எடுத்துக்கொண்டு அதில் சிறிதளவு ஹைட்ரோ குளோரிக் அமிலத்தை
ஊற்றவும். சில மெக்னீசியம் நாடாத்துண்டுகளை மெதுவாகச் சேர்க்கவும். நீ என்ன காண்கிறாய்?
இப்பொழுது ஒரு எரியும் தீக்குச்சியை சோதனைக்குழாயின் வாய்ப்பகுதியில் காட்டவும். ஏதாவது
ஒலியைக் கேட்கிறாயா? இவ்வினையில் உருவாகும் ஒரு வாயு 'பாப்' என்ற ஒலியுடன் எரிவதைக்
காண்கிறாய் அல்லவா? இதிலிருந்து, ஒரு அமிலமும் உலோகமும் விணைபுரியும்போது ஹைட்ரஜன்
வாயு வெளிப்படுவதை அறியலாம். (இந்த சோதனையை ஆசிரியரின்முன்னிலையில் செய்யவும்)
காப்பர்
அல்லது பித்தளைப் பாத்திரங்களின் மீது வெள்ளீயம் என்ற உலோகம் (FFWILD) பூசப்படுகிறது.
அவ்வாறு பூசவில்லையெனில் உணவுப்பொருள்களிலுள்ள கரிம அமிலங்கள் பாத்திரங்களிலுள்ள தாமிரத்துடன்
வினைபுரிந்து உணவை நஞ்சாக்கிவிடும். வெள்ளீயம், பாத்திரங்களை அமிலங்களின் செயல்பாட்டிலிருந்து
தனித்துப் பிரித்து உணவு நஞ்சாவதைத் தடுக்கின்றது.
ii. உலோக
கார்பனேட்டுகள் மற்றும் பைகார்பனேட்டுகளுடன் வினை
நீர்த்த அமிலங்களுடன் உலோக கார்பனேட்டுகள் மற்றும் பைகார்பனேட்டுகள்
வினைபுரியும்போது கார்பன் டைஆக்சைடு வாயுவும், நீரும் உருவாகின்றன. எடுத்துக்காட்டாக,
கால்சியம் கார்பனேட்டானது சல்பியூரிக் அமிலத்துடன் வினைபுரிந்து கால்சியம் சல்பேட்,
கார்பன் டைஆக்சைடு மற்றும் நீரைக் கொடுக்கிறது.
நீர்த்த
கால்சியம் + சல்பியூரிக் → கால்சியம்
+ கார்பன் +நீர் கார்பனேட் அமிலம் சல்பேட் டைஆக்சைடு
CaCO3 + H2SO4 →
CaSO4 + CO2 +H2O
செயல்பாடு 2
ஒரு
முகவையில் எலுமிச்சைச் சாற்றை எடுத்துக்கொண்டு அதனுடன் சிறிதளவு சமையல் சோடாவை மெதுவாகச்
சேர்க்கவும். என்ன காண்கிறாய்? இதிலிருந்து நீ என்ன அறிகிறாய்?
iii.
உலோக ஆக்சைடுகளுடன் வினை
பல்வேறு உலோக ஆக்சைடுகள் நீர்த்த அமிலங்களுடன் வினைபுரிந்து
அவற்றின் உலோக உப்புகள் மற்றும் நீரைத் தருகின்றன.
உலோக + நீர்த்த → உலோக
+ நீர் ஆக்சைடுகள் அமிலம் உப்புகள்
எடுத்துக்காட்டு
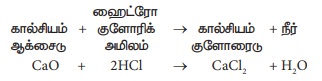
2. அமிலங்களின்
பயன்கள்
• நமது வயிற்றில் சுரக்கும் ஹைட்ரோ குளோரிக் அமிலம் உணவுப்பொருள்களின்
செரிமானத்திற்கு உதவுகிறது.
• உணவுப் பொருள்கள் கெட்டுப்போகாமல் இருக்க வினிகர்(அசிட்டிக்அமிலம்)பயன்படுத்தப்படுகிறது.
ஊறுகாய் போன்ற உணவுப் பொருள்கள் கெட்டுப்போகாமல் இருக்க பென்சாயிக் அமிலம் பயன்படுத்தப்படுகிறது.
• குளியல் சோப்புகள் மற்றும் சலவை சோப்புகள் தயாரிக்க உயர் கொழுப்பு
அமிலங்களின் சோடியம் உப்புகள் அல்லது பொட்டாசியம் உப்புகள் பயன்படுகின்றன.
• சல்பியூரிக் அமிலம் வேதிப்பொருள்களின் அரசன் என்று அழைக்கப்படுகிறது.
இது மிகச் சிறந்த நீர் நீக்கியாகச் செயல்படுகிறது. இது பல்வேறு சோப்புகள், வண்ணப்பூச்சுகள்
(பெயிண்ட்கள்), உரங்கள் மற்றும் பல வேதிப்பொருள்கள் தயாரிக்கும் தொழிற்சாலைகளில் பயன்படுத்தப்படுகிறது.
• ஹைட்ரோகுளோரிக் அமிலம், நைட்ரிக் அமிலம் மற்றும் சல்பியூரிக்
அமிலம் போன்றவை முக்கியமான ஆய்வகக் காரணிகளாகச் செயல்படுகின்றன.
• அனைத்து உயிரினங்களின் நியூக்ளிக் அமிலங்களை பொருளாகக் கொண்டுள்ளன.
செல்களும் அடிப்படைப் விலங்குகள் டி-ஆக்ஸிரிபோ நியூக்ளிக் அமிலத்தையும் (DNA) தாவரங்கள்
ரிபோ நியூக்ளிக் அமிலத்தையும் (RNA) கொண்டுள்ளன.

