11 வது வேதியியல் : அலகு 1 : வேதியியலின் அடிப்படைக் கருத்துக்கள் மற்றும் வேதிக் கணக்கீடுகள்
எளிய விகித வாய்ப்பாட்டிலிருந்து மூலக்கூறு வாய்பாட்டினைக் கணக்கிடுதல்
2. எளிய விகித வாய்ப்பாட்டிலிருந்து மூலக்கூறு வாய்பாட்டினைக் கணக்கிடுதல்:
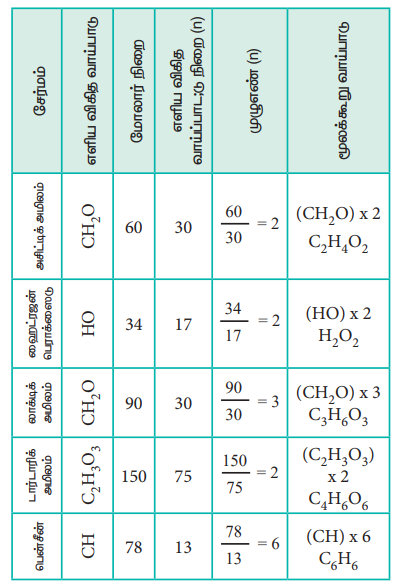
மூலக்கூறு வாய்ப்பாட்டினை கண்டறிவதை பின்வரும் எடுத்துக்காட்டின் மூலம் நாம் புரிந்து கொள்வோம்.
C-40%, H-6.6% ; O-53.4% நிறை சதவீத இயைபுடைய இரு கரிமச்சேர்மங்களில் ஒன்று வினிகரில் காணப்படுகிறது (மோலார்நிறை 60g mol-1), மற்றொன்று புளித்த பாலில் காணப்படுகிறது (மோலார்நிறை 90g mol-1) அவைகளின் மூலக்கூறு வாய்பாடுகளைக் கண்டறிக.
இரண்டு சேர்மங்களும் ஒரே சதவீத இயைபைக் கொண்டுள்ளன. எடுத்துக்காட்டு (2)ல் தீர்வு காணப்பட்ட எளிய விகித வாய்பாடும், இவ்விரண்டு சேர்மங்களின் எளிய விகித வாய்பாடுகளும் ஒன்றே. அதாவது எளிய விகித வாய்பாடு CH2O ஆகும். எளிய விகித வாய்ப்பாட்டினைக் கொண்டு கணக்கிடப்படும் நிறை
(CH2O) = 12 + (2 × 1) + 16 = 30 g mol-1
வினிகரில் காணப்படும் சேர்மத்தின் வாய்பாடு
n = மோலார் நிறை / கணக்கிடப்பட்ட எளிய விகித வாய்ப்பாட்டு நிறை = 60 / 30 = 2
ஃ மூலக்கூறு வாய்பாடு = (CH2 O)2
= C2 H4 O2 (அசிட்டிக் அமிலம்)
தன்மதிப்பீடு
6) x, y, z ஆகிய தனிமங்களைக் கொண்டுள்ள ஒரு சேர்மத்தின் பகுப்பாய்வு முடிவுகளிலிருந்து பின்வரும் தரவுகள் பெறப்பட்டுள்ளது. x = 32%, y = 24%, z = 44% x, y மற்றும் z ன் ஒப்பு அணுக்களின் எண்ணிக்கை முறையே 2, 1 மற்றும் 0.5 ஆகும். (சேர்மத்தின் மூலக்கூறு நிறை 400g)
i) தனிமங்கள் x, y மற்றும் z ன் அணு நிறைகளைக் காண்க.
ii) சேர்மத்தின் எளிய விகித வாய்பாடு மற்றும்
iii) சேர்மத்தின் மூலக்கூறு வாய்ப்பாட்டினைக் கண்டறிக.
தீர்வு
கணக்கிடப்பட்ட எளிய விகித வாய்ப்பாட்டு முறை = (16 × 14) + (24 × 2) + 88
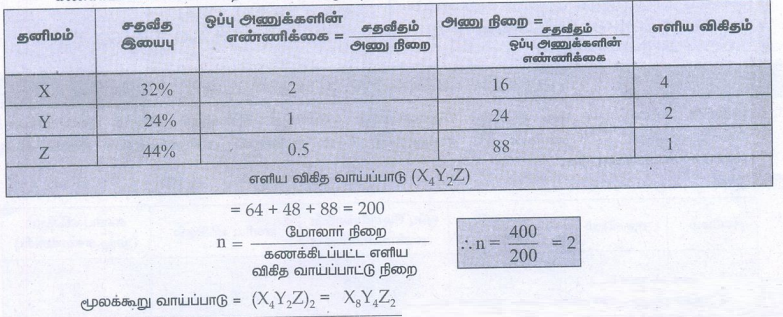
= 64 + 48 + 88 = 200
n = மோலார் நிறை / கணக்கிடப்பட்ட எளிய விகித வாய்ப்பாட்டு நிறை
மூலக்கூறு வாய்ப்பாடு = (X4Y2Z) 2 = X8Y4Z2
∴ n = 400 / 200 = 2
புளித்த பாலில் காணப்படும் சேர்மத்தின் மூலக்கூறு வாய்பாடு
n = மோலார் நிறை / 30 = 90 / 30 = 3
மூலக்கூறு வாய்பாடு = (CH2 O)3
= C3 H6 O3 (லாக்டிக் அமிலம்)