11 வது வேதியியல் : அலகு 5 : கார மற்றும் காரமண் உலோகங்கள்
காரமண் உலோகங்களின் வேதிப்பண்புகள்
காரமண் உலோகங்களின் வேதிப்பண்புகள்
கார உலோகங்களைக் காட்டிலும், காரமண் உலோகங்கள் குறைவான வினைத்திறனைப் பெற்றுள்ளன. தொகுதியில் கீழே வரும் போது இவற்றின் வினைத்திறன் அதிகரிக்கின்றது.
ஹாலஜன்களுடன் வினை
அதிக வெப்ப நிலையில், அனைத்து காரமண் உலோகங்களும், ஹாலஜன்களுடன் இணைந்து, அவைகளின் ஹாலைடுகளை உருவாக்குகின்றன.
M + X2 → MX2
(M = Be, Mg, Ca, Sr, Ba, Ra,
X = F, Cl, Br, l )
(NH4)2 BeF4 வெப்பச் சிதைவடையச் செய்தல் வினையானது BeF2 தயாரிக்க சிறந்த முறையாகும். BeCl2 வை அதன் ஆக்சைடிலிருந்து எளிதாக தயாரிக்கலாம்.
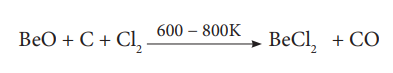
ஹைட்ரஜனுடன் வினை
பெரிலியத்தினைத் தவிர்த்து பிற தனிமங்கள் வெப்பப்படுத்தும் போது, ஹைட்ரஜனுடன் இணைந்து MH2 என்ற பொது வாய்ப்பாடுடைய ஹைட்ரைடுகளைத் தருகிறது. BeCl2 மற்றும் LiAlH4 ஆகியவற்றை வினைப்படுத்துவதன் மூலம் BeH2 ஐத் தயாரிக்கலாம்.
2 BeCl2 + LiAlH4 → 2 BeH2 + LiCl + AlCl3