வேதியியல் - பருப்பொருட்களை வகைப்படுத்துதல் | 11th Chemistry : UNIT 1 : Basic Concepts of Chemistry and Chemical Calculations
11 வது வேதியியல் : அலகு 1 : வேதியியலின் அடிப்படைக் கருத்துக்கள் மற்றும் வேதிக் கணக்கீடுகள்
பருப்பொருட்களை வகைப்படுத்துதல்
பருப்பொருட்களை வகைப்படுத்துதல்
உனது வகுப்பறை சூழலை உற்றுநோக்கு. நீ எதைக் காண்கிறாய்? உனது இருக்கை, மேசை, கரும்பலகை ஜன்னல் போன்றவற்றை நீ கண்டிருப்பாய். இவை அனைத்தும் எதனால் ஆக்கப்பட்டவை? இவை அனைத்தும் பருப்பொருள்களால் ஆக்கப்பட்டவை.
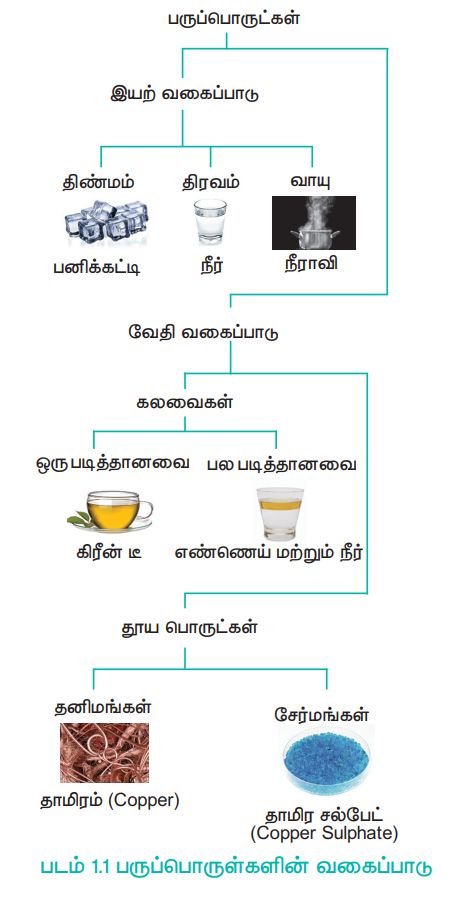
நிறையுள்ள, இடத்தை அடைத்துக்கொள்ளும் தன்மையுடைய அனைத்தும், பருப்பொருட்கள் என வரையறுக்கப்படுகின்றன. அனைத்து பருப்பொருட்களும் அணுக்களால் ஆக்கப்பட்டவை. பருப்பொருள் பற்றிய இந்த அறிவானது, நமது சூழலில் இருந்து நாம் பெறும் அனுபவங்களை விளக்குவதற்கு பயனுள்ளதாக அமையும். பருப்பொருட்களின் பண்புகளை புரிந்து கொள்ளும் பொருட்டு, நாம் அதனை வகைப்படுத்த வேண்டும். பருப்பொருட்களை வகைப்படுத்துதலில் பல்வேறு முறைகள் உள்ளன. பொதுவாக, பருப்பொருள்களை அதன் இயற்நிலைமை மற்றும் வேதிஇயைபு ஆகியவற்றின் அடிப்படையில், விளக்கப் படத்தில் காட்டியுள்ளவாறு வகைப்படுத்தலாம்.
1. இயற்நிலைமையின் அடிப்படையில் பருப்பொருட்களின் வகைப்பாடு
பருப்பொருட்களை அவற்றின் இயற் நிலைமையின் அடிப்படையில் திண்மம், திரவம் மற்றும் வாயு என வகைப்படுத்தலாம். அழுத்தம் மற்றும் வெப்பநிலையினை தகுந்தவாறு மாற்றியமைப்பதன் மூலம் பருப்பொருள்களை அதன் ஒரு இயற் நிலைமையிலிருந்து மற்றொரு நிலைமைக்கு மாற்ற இயலும்.
2. வேதித்தன்மையின் அடிப்படையில் வகைப்பாடு
பருப்பொருட்களை அவற்றின் வேதித்தன்மையின் அடிப்படையில், தூய பொருட்கள் மற்றும் கலவைகள் என வகைப்படுத்தலாம். கலவையில் ஒன்றிற்கும் மேற்பட்ட வேதி உட்பொருட்கள், அவற்றிற்கிடையே எத்தகைய இடைவினைகளுமின்றி காணப்படுகின்றன. இவற்றின் தோற்றத்தின் அடிப்படையில் ஒரு படித்தான அல்லது பல படித்தான கலவை என மேலும் வகைப்படுத்தப்படுகின்றன.
தூய பொருட்கள் என்பவை எளிய அணுக்கள் அல்லது மூலக்கூறுகளால் ஆக்கப்பட்டவை. இவை தனிமங்கள் மற்றும் சேர்மங்கள் என வகைப்படுத்தப்படுகின்றன.
தனிமம் :
ஒரே ஒரு வகை அணுக்களை மட்டுமே உள்ளடக்கியவை தனிமம் எனப்படும். அணுக்கள் என்பவை, புரோட்டான்கள், எலக்ட்ரான்கள், நியூட்ரான்கள் போன்ற அடிப்படைத் துகள்களைக் கொண்ட மின் நடு நிலைத்தன்மை உடையது என்பதனை நாம் அறிவோம்.
தனிமம் ஆனது ஓரணு அல்லது பல்லணு அலகுகளை உள்ளடக்கியதாக காணப்படுகிறது.
எடுத்துக்காட்டு : ஓரணு அலகு – தங்கம் (Au), தாமிரம் (Cu), பல்லணு அலகு - ஹைட்ரஜன் வாயு (H2), பாஸ்பரஸ் (P4) மற்றும் சல்பர் (S8).
சேர்மம் :
இரண்டு அல்லது அதற்கு மேற்பட்ட வெவ்வேறு தனிம அணுக்களைக் கொண்ட மூலக்கூறுகளை உள்ளடக்கியது சேர்மங்களாகும்.
எடுத்துக்காட்டு : கார்பன் டை ஆக்ஸைடு (CO2), குளுக்கோஸ் (C6H12O6), ஹைட்ரஜன் சல்பைடு (H2S), சோடியம் குளோரைடு (NaCl)
சேர்மங்களின் பண்புகள், அவற்றில் அடங்கியுள்ள தனிமங்களின் பண்புகளிலிருந்து மாறுபட்டிருக்கும். எடுத்துக்காட்டாக சோடியம் ஒரு பளபளப்பான உலோகம், குளோரின் ஓர் எரிச்சலூட்டும் வாயு, ஆனால் இந்த இரண்டு தனிமங்களில் இருந்து உருவாகும் சேர்மமான சோடியம் குளோரைடு, படிகத்தன்மையுடைய திண்மமாகும். மேலும், இச்சேர்மம் உயிரியல் செயல்பாடுகளுக்கு முக்கியமானதாகும்.
தன்மதிப்பீடு
1. வேதித்தன்மை அடிப்படையிலான வகைப்பாட்டு அறிவினை பயன்படுத்தி, பின்வரும் ஒவ்வொன்றையும், தனிமம், சேர்மம் அல்லது கலவை என வகைப்படுத்துக.
(i) சர்க்கரை
(ii) கடல்நீர்
(iii) வாலைவடிநீர்
(iv) கார்பன் டை ஆக்ஸைடு
(v) தாமிர கம்பி (Copper wire)
(vi) சாதாரண உப்பு
(vii) வெள்ளித் தட்டு (Silver plate)
(viii) நாப்தலீன் உருண்டைகள்.
தீர்வு:
(i) தனிமம் - காப்பர் கம்பி, வெள்ளித்தட்டு
(ii) சேர்மம் - சர்க்கரை, வாலை வடிநீர், கார்பன் டை ஆக்ஸைடு, சாதாரண உப்பு, நாஃப்தலீன் உருண்டைகள்.
(iii) கலவை - கடல் நீர்