11 வது வேதியியல் : அலகு 5 : கார மற்றும் காரமண் உலோகங்கள்
காரமண் உலோகங்களின் பொதுப் பண்புகள்
காரமண் உலோகங்களின் பொதுப் பண்புகள்
இயற்நிலைமை
பெரிலியம் அரிதானது. மேலும் ரேடியம் மிகவும் அரிதானதாகும். வெப்பப் பாறைகளில் 10 சதவீதம் மட்டும் காணப்படுகிறது. புவி மேலடுக்கில் பொதுவாகக் காணப்படும் தனிமங்களாக மெக்னீசியம் மற்றும் கால்சியம் உள்ளன.
அதிக அளவு கிடைக்கப்பெறும் தனிமங்களில் கால்சியம் ஐந்தாவதாகவும், மெக்னீசியம் எட்டாவதாகவும் உள்ளன. மேலும் பல பாறைகள் மற்றும் தாதுக்களில் மெக்னீசியம் மற்றும் கால்சியம் காணப்படுகின்றது. கார்னலைட், டோலமைட், மேக்னசைட் ஆகியவற்றில் மெக்னீசியமும், சுண்ணாம்புக்கல், ஜிப்சம் ஆகியவற்றில் கால்சியமும் காணப்படுகின்றன. பெரும்பாலான ஸ்ட்ரான்சியம் ஆனது செலிசைட் மற்றும் ஸ்ட்ரான்சியோனைட்டில் காணப்படுகிறது. பேரியம் பெரும்பாலும் பேரைட் தாதுவில் உள்ளது. யுரேனியத்தின் கதிரியக்கத் தன்மையின் விளைவாக உருவாகும் பொருள் ரேடியம். ஆதலால் யுரேனியத்தைக் கொண்டுள்ள தாதுக்களில்ரேடியம் காணப்படுகின்றது.
உங்களுக்குத் தெரியுமா?
வான வேடிக்கை

பெரும்பாலான கார மற்றும் காரமண் உலோகங்கள் வண்ணங்களை உருவாக்க பயன்படுகின்றன. ஸ்ட்ரான்சியம் மற்றும் பேரியம் போன்றவை வான வேடிக்கை நிகழ்வுகளில் வண்ணம் உருவாக்கப் பயன்படுகின்றன. குளோரின் தனிமத்துடன் சேர்ந்து பேரியம் பச்சை நிற தீப்பொறிகளை உருவாக்குகிறது. கால்சியம் ஆரஞ்சு நிறத்தையும், லித்தியம் ஓரளவு சிவப்பு நிறத்தையும் தருகிறது. ஸ்ட்ரான்சியம் கார்பனேட் பிரகாசமான சிவப்பு நிறத்தையும், சோடியத்தின் நைட்ரேட்டுகள் ஆரஞ்சு நிறத்தையும் தருகிறது. பொட்டாசியம் மற்றும் ருபீடியம் கருஊதா நிறத்தையும், சீசியம் இண்டிகோ நிறத்தையும் தருகிறது. எரிதலால், எலக்ட்ரான்கள் கிளர்வுறுகின்றன. வழக்கமான ஆற்றல் மட்டதை விட, அதிக ஆற்றல் மட்டத்திற்குச் செல்கிறது. அவற்றின் அதிகப்படியான ஆற்றலை அவைகள் நிறமுள்ள வெடிப்பு ஒளியாக வெளியிடுகின்றன.
வெப்பச்சுடரில் காப்பர் கார்பனேட்டானது சிதைவடையும் என்பதால் நீல நிறமுள்ள வான வேடிக்கையினை உருவாக்குவது கடினமானதாகும். சமீப காலங்களில் வான வேடிக்கை வல்லுநர்கள் காரமண் உலோகமான மெக்னீசியம் மற்றும் அலுமினியத்தின் உலோகக்கலவை மெக்னாலியத்தினை வான வேடிக்கை நிறங்களை வலுப்படுத்த பயன்படுத்துகின்றனர். மெக்னாலியம் நீல நிறத்தினை மேலும் வலுப்படுத்துகிறது. எனினும், சிவப்பு, பச்சை, மஞ்சள் நிறங்களைப் போன்று பிரகாசமான நீல நிறத்தினைப் பெற வெப்ப நுட்பவியலாளர்கள் தொடர்ந்து முயன்று வருகின்றனர்.
எலக்ட்ரான் அமைப்பு
இத்தனிமங்கள் அவற்றின் அணுக்களில், மந்த வாயு எலக்ட்ரான் அமைப்பினைத் தொடர்ந்து இணைதிறக் கூட்டில் இரண்டு எலக்ட்ரான்களைப் பெற்றுள்ளன. இவைகளின் பொதுவான எலக்ட்ரான் அமைப்பு (மந்தவாயு) ns2. இங்கு 'n' என்பது இணைதிறன் கூட்டைக் குறிப்பிடுகிறது.
அட்டவணை 5.8 காரமண் உலோகங்களின் எலக்ட்ரான் அமைப்பு
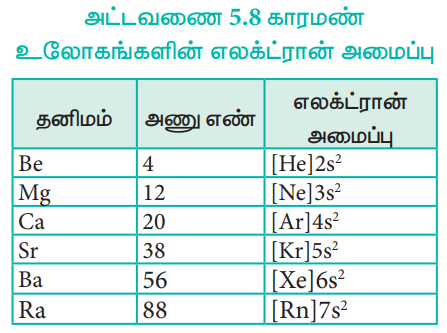
அணு மற்றும் அயனி ஆரம்
காரமண் உலோகங்களின் அணு மற்றும் அயனி ஆரங்களின் மதிப்புகள் அவற்றிற்கு இணையான கார உலோகங்களைக் காட்டிலும் குறைவானதாகும். ஏனெனில் இரண்டாம் தொகுதி தனிமங்கள் அதிக அணுக்கரு மின் சுமையைப் பெற்றிருப்பதால் அவைகளின் எலக்ட்ரான்கள் அணுக்கருவினை நோக்கி வலிமையாகக் கவரப்படுகின்றன. தொகுதியில் மேலிருந்து கீழே வரும் போது, கூடுகளின் எண்ணிக்கை மற்றும் திரை மறைப்பு விளைவு அதிகரிப்பதால் அணு ஆரம் அதிகரிக்கின்றது.
பொதுவான ஆக்ஸிஜனேற்ற நிலை
இரண்டாம் தொகுதி தனிமங்கள், அவைகளின் இணைதிற கூட்டில் இரண்டு எலக்ட்ரான்களைக் கொண்டுள்ளன. அவைகளை இழப்பதன் மூலம் மந்தவாயுவின் எலக்ட்ரான் அமைப்பினைப் பெறுகின்றன. எனவே இவற்றின் சேர்மங்களில் +2 ஆக்சிஜனேற்ற நிலையில் காணப்படுகின்றது.
அயனியாக்கும் ஆற்றல்
‘p' தொகுதி தனிமங்களோடு ஒப்பிடும் போது, காரமண் உலோகங்கள் ஓரளவிற்கு பெரிய உருவளவினைப் பெற்றிருப்பதாலும், தொகுதியில் கீழாக, அணுவின் உருவளவு அதிகரிப்பதாலும், அயனியாக்கும் ஆற்றல் குறைகிறது. புதிய கூடுகள் உருவாக்கப்படுதல் மற்றும் உட்கூட்டில் உள்ள எலக்ட்ரான்களின் திரைமறைப்பு விளைவு அதிகமாதல் ஆகியவை இதற்குக் காரணமாக அமைகின்றன. முதல் தொகுதி தனிமங்களைக் காட்டிலும், இரண்டாம் தொகுதி தனிமங்களின் அயனியாக்கும் ஆற்றல் அதிகம். ஏனெனில் அவைகள் சிறிய உருவளவினைப் பெற்றிருக்கின்றன. மேலும் எலக்ட்ரான்கள் அணுக்கருவினை நோக்கி ஈர்க்கப்படுகின்றன. இவை கார உலோகங்களைக் காட்டிலும் குறைவான நேர்மின் தன்மையினைக் கொண்டுள்ளன.
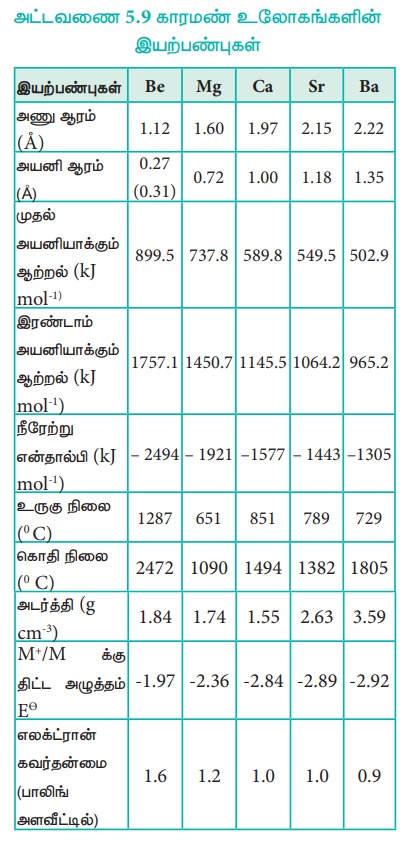
அட்டவணை 5.9 காரமண் உலோகங்களின் இயற்பண்புகள்
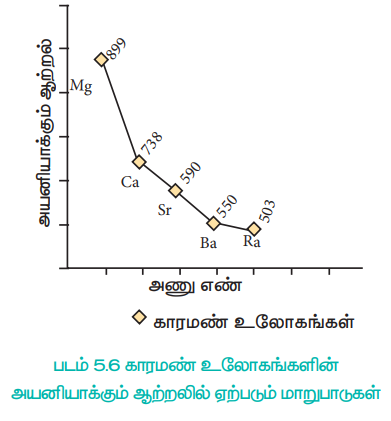
படம் 5.6 காரமண் உலோகங்களின் அயனியாக்கும் ஆற்றலில் ஏற்படும் மாறுபாடுகள்
காரஉலோகங்களைக் காட்டிலும், காரமண் உலோகங்களின் முதல் அயனியாக்கும் ஆற்றல் (IE1) அதிகமாக இருந்தபோதிலும், இரண்டாம் அயனியாக்கும் ஆற்றல் மதிப்பு (IE2) ஆனது, கார உலோகங்களைக் காட்டிலும் மிக குறைவாக உள்ளது.
ஏனெனில் காரஉலோகங்களில், இரண்டாவது எலக்ட்ரானானது, ஏற்கெனவே நிலையான மந்த வாயுவின் எலக்ட்ரான் அமைப்பினைப் பெற்றுள்ள ஒற்றை நேர்மின் சுமையுடைய அயனியிலிருந்து நீக்கப்பட வேண்டும். காரமண் உலோகங்களைப் பொறுத்த வரையில், அவற்றின் ஒற்றை நேர்மின் சுமையுடைய அயனியானது அவைகளின் இணைதிறன் கூட்டில் இன்னும் ஒரு எலக்ட்ரானைப் பெற்றிருப்பதால் அவைகளை எளிதாக நீக்க இயலும்.
நீரேற்று என்தால்பி
கார உலோகங்களைக்காட்டிலும், காரமண் உலோகங்கள் அதிக அளவில் நீரேற்றமடைகின்றன. ஏனெனில் காரமண் உலோக அயனிகளின் நீரேற்று ஆற்றலானது கார உலோக அயனிகளின் நீரேற்று ஆற்றலை விட அதிகம். கார உலோகங்களைப் போன்றே, காரமண் உலோக அயனிகளின் ஆரம் தொகுதியில் அதிகரிக்கும்போது, அவற்றின் நீரேற்று ஆற்றல் குறைகிறது.
Be > Mg > Ca > Sr > Ba
எடுத்துக்காட்டு: மெக்னீஷியம் குளோரைடு மற்றும் கால்சியம் குளோரைடு ஆகியவை முறையே MgCl2.6H2O மற்றும் CaCl2.6H2O ஆகிய நீரேற்ற சேர்மங்களாகக் காணப்படுகின்றன. ஆனால் NaCl மற்றும் KCl போன்றவை இத்தகைய ஹைட்ரேட்டுகளைத் தருவதில்லை.
எலக்ட்ரான் கவர் தன்மை
கார உலோகங்களைப் போன்றே, காரமண் உலோகங்களிலும் தொகுதியில் மேலிருந்து கீழே எலக்ட்ரான் கவர்தன்மை மதிப்பு குறைகிறது.
சுடரில் நிறம் தருதல் மற்றும் நிறமாலை
ஹைட்ரோ குளோரிக் அமிலத்தை சேர்த்து ஈரமாக்கப்பட்ட காரமண் உலோக உப்புகள் பிளாட்டினக் கம்பி மூலம் சுடரில் காட்டப்படும்போது, அவைகள் கீழே கண்டுள்ளவாறு குறிப்பிட்ட நிறச்சுடரைத் தருகின்றன.
அட்டவணை 5.10 சுடர் நிறம் மற்றும் அலைநீளம்
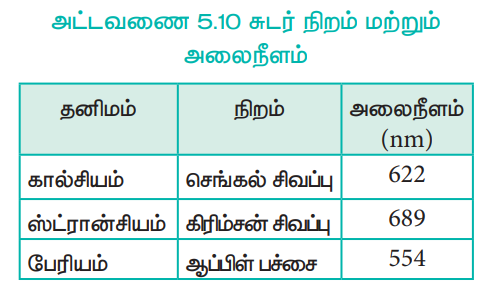
சுடரின் வெப்பத்தால் இணைதிற எலக்ட்ரான்கள் கிளர்வுற்று அதிக ஆற்றல் நிலைக்குச் செல்கின்றன. இவை அவற்றின் உண்மையான ஆற்றல் நிலைக்குத் திரும்பும்போது, கூடுதல் ஆற்றலை ஒளியாக உமிழ்கிறது. இந்த ஒளியின் அலைநீளம் கட்புலனாகும் பகுதியில் மேற்கண்டுள்ள அட்டவணையில் குறிப்பிட்டுள்ளவாறு அமைந்துள்ளது.

படம் 5.7 காரமண் உலோகங்களின் நிறச்சுடர்கள்