தயாரித்தல், பண்புகள், பயன்கள் | வேதியியல் - கால்சியத்தின் முக்கியமானச் சேர்மங்கள் | 11th Chemistry : UNIT 5 : Alkali and Alkaline Earth Metals
11 வது வேதியியல் : அலகு 5 : கார மற்றும் காரமண் உலோகங்கள்
கால்சியத்தின் முக்கியமானச் சேர்மங்கள்
1. கால்சியத்தின் முக்கியமானச் சேர்மங்கள்
சுட்ட சுண்ணாம்பு (CaO)
தயாரித்தல்
வணிக ரீதியில் சுண்ணாம்புக் கல்லை, சுண்ணாம்புக் களவாயில் 1070 - 1270K வெப்பநிலை எல்லையில் வெப்பப்படுத்துவதன் மூலம் இது தயாரிக்கப்படுகிறது.
CaCO3 ⇌ CaO + CO2
இவ்வினை ஒரு மீள் வினையாதலால், வினையினை முற்றிலும் நிகழ்த்த ஏதுவாக, வினையில் உருவாகும் கார்பன்டையாக்சைடு உடனுக்குடன் நீக்கப்படுகிறது.
பண்புகள்
கால்சியம் ஆக்சைடு வெண்மைநிற படிக உருவமற்ற திண்மம்.
1. இதன் உருகு நிலை 2870 K. காற்றில் வைக்கப்படும் போது, கார்பன்டையாக்சைடு மற்றும் ஈரப்பதத்தினை உறிஞ்சுகிறது.
CaO + H2O → Ca(OH)2
CaO + CO2 → CaCO3
2. குறைந்தளவு நீரினைச் சேர்க்கும்போது, கால்சியம் ஆக்சைடு கட்டிகள் உடைக்கப்படுகின்றன. இச்செயல் சுண்ணாம்பை நீர்க்கச் செய்தல் என்றும் உருவாகும் வினைபொருள் நீற்றுச் சுண்ணாம்பு எனவும் அழைக்கப்படுகிறது.
CaO + H2O → Ca(OH)2
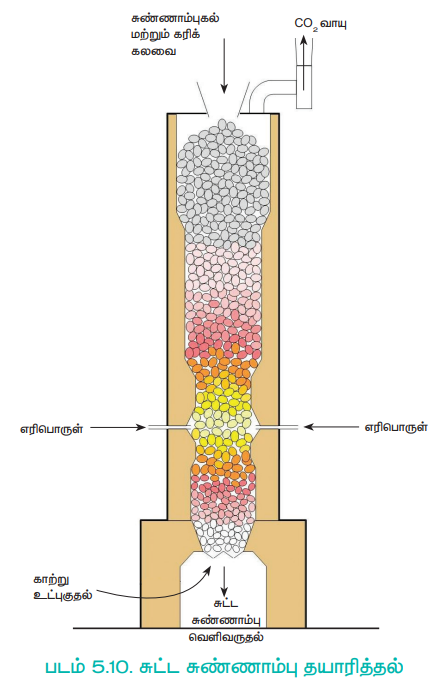
படம் 5.10. சுட்ட சுண்ணாம்பு தயாரித்தல்
3. சுட்ட சுண்ணாம்பு, மற்றும் சோடியம் ஹைட்ராக்சைடு சேர்ந்த கலவை சோடாச் சுண்ணாம்பு எனப்படுகிறது
4. இது SiO2 மற்றும் P4O10 ஆகிய அமில ஆக்ஸைடுகளுடன் சேர்ந்து முறையே CaSiO3 மற்றும் Ca3 (PO4)2 ஆகியவற்றைத் தருகின்றது.
CaO + SiO2 → CaSiO3
6 CaO + P4O10 → 2 Ca3 (PO4)2
பயன்கள்
கால்சியம் ஆக்சைடானது,
1. சிமெண்ட், கட்டுமான பூச்சுகள் மற்றும் கண்ணாடித் தயாரிப்பில் பயன்படுகிறது.
2. சோடியம் கார்பனேட் மற்றும் நீற்றுச் சுண்ணாம்பு தயாரித்தலில் பயன்படுகிறது.
3. சர்க்கரை தூய்மையாக்கலில் பயன்படுகிறது.
4. உலர்த்தும் வினைபொருளாகப் பயன்படுகிறது.
2. கால்சியம் ஹைட்ராக்சைடு தயாரித்தல்
கால்சியம் ஆக்ஸைடுடன் நீர் சேர்க்கப்பட்டு கால்சியம் ஹைட்ராக்சைடு தயாரிக்கப்படுகிறது.
பண்புகள்
இது ஒரு வெண்மை நிற படிக உருவமற்ற படிகமாகும். இது நீரில் பகுதியளவே கரையும். இதன் நீர்க்கரைசல் நீற்றுச்சுண்ணாம்பு (சுண்ணாம்பு நீர்) எனவும், நீற்றுச் சுண்ணாம்பின் தொங்கல் நீர்க்கரைசல் சுண்ணாம்புப் பால் எனவும் அறியப்படுகிறது.
கார்பன் டை ஆக்சைடை நீற்றுச் சுண்ணாம்பின் வழியே செலுத்தும்போது, அது பால்போல மாறுகிறது. இதற்கு காரணம் இந்நிகழ்வில், கால்சியம் கார்பனேட் உருவாகிறது.
Ca(OH)2 + CO2 → CaCO3 + H2O
கூடுதலாக அதிக அளவு CO2 செலுத்தப்படும்போது, வீழ்படிவு கரைந்து கால்சியம் ஹைட்ரஜன் கார்பனேட்டைத் தருகிறது.
CaCO3 + CO2 + H2O → Ca(HCO3)2
நீர்த்த சுண்ணாம்பு, குளோரினுடன் வினைபுரிந்து, சலவைத்தூளின் ஒரு பகுதிப் பொருளான, ஹைப்போ குளோரைட்டைத் தருகிறது.
2 Ca (OH)2 + 2Cl2 → CaCl2 + Ca(OCl)2 + 2 H2O
பயன்கள்
கால்சியம் ஹைட்ராக்சைடு கட்டுமானப் சுண்ணாம்பு கலவைகல்.
நுண்ணுயிர் எதிர்ப்பு இயல்பினைப் பெற்றிருப்பதால் சுண்ணாம்பு அடித்தலில் பயன்படுகிறது.
கண்ணாடி உற்பத்தி செய்தல், தோல் பதனிடும் தொழில்கள், சலவைத்தூள் தயாரிப்பதில் மற்றும் சர்க்கரை தயாரித்தலில் பயன்படுகிறது.
3. ஜிப்சம் (CaSO4.2H2O)
வரலாற்றுக்கு முந்தைய பெரிய கடல் வடிநில பரப்பில் இருந்த நீர் ஆவியாவதால் ஜிப்சப்படுகைகள் உருவாகின்றன. நீர் ஆவியாக மாறும் போது அதில் அடங்கியுள்ள தாதுப்பொருட்களின் செறிவு அதிகரிப்பதுடன் அவை படிகமாகின்றன.

படம் 5.11 ஒரு ஜிப்சக் குவாரி
ஜிப்சத்தின் பண்புகள்
∙ ஜிப்சம் ஒரு மிருதுவான தாதுப்பொருள், நீரில் ஒரளவிற்கு கரையும், வெப்பநிலை இதன் கரைதிறன் மீது தாக்கத்தினை ஏற்படுத்துகிறது. வெப்பநிலை அதிகரிக்கும் போது, மற்ற உப்புகளைப் போல் அல்லாமல் இதன் கரைதிறன் குறைகிறது. இப்பண்பு எதிர்க்கரைதிறன் (retrograde solubility) என அறியப்படுகிறது. இது ஜிப்சத்தின் தனித்துவமான பண்பாகும்.
∙ ஜிப்சம் பொதுவாக நிறமற்றதாகவோ அல்லது வெளிர்ந்த நிறத்தையோ கொண்டிருக்கும். சில நேரங்களில், மாசுகள் காணப்படும் காரணத்தால் இளஞ்சிகப்பு, மஞ்சள், பழுப்பு மற்றும் வெளிர் பச்சை ஆகிய நிறங்களின் சாயல்களைப் பெற்றிருக்கும்.
∙ சில நேரங்களில், ஜிப்சம் மலர்களின் இதழ்களை ஒத்த வடிவமைப்பில் கிடைக்கப் பெறுகிறது. இவ்வகை ‘பாலைவன ரோஜா' என அழைக்கப்படுகிறது. இது பெரும்பாலும் பாலைவனப் பகுதிகளில் உண்டாகிறது.
∙ ஜிப்சம் குறைவான வெப்பக் கடத்தும் திறனைப் பெற்றுள்ளது. இதன் காரணமாக உலர் சுவர்கள் மற்றும் சுவர்ப்பலகைகள் தயாரித்திட பயன்படுகிறது. ஜிப்சம் இயற்கை மின்காப்புப் பொருள் எனவும் அறியப்படுகிறது.

படம் 5.12 ஜிப்சத்தின் ஒரு வகையான அலபாஸ்டர்
∙ அலபாஸ்டர் எனும் ஜிப்சத்தின் ஒரு வகையானது, அணிகல கற்கள் போன்று விலைமதிப்புமிக்கது. இது சிற்பிகளால் பல நூற்றாண்டுகளாக பயன்படுத்தப்பட்டு வருகிறது.
∙ இது துகள் வடிவமுடைய, ஒளி ஊடுருவ இயலாத்தன்மை உடையது. "மோ" கடினத்தன்மை அளவீட்டில் (moh's scale) ஜிப்சத்தின் கடினத்தன்மை 1.5 முதல் 2 வரை. இதன் அடர்த்தி எண் 2.3 முதல் 2.4 வரை.
ஜிப்சத்தின் பயன்கள்
∙ பண்டைய எகிப்து மற்றும் மெசபடோமியாவில் ஜிப்சத்தின் ஒரு வகையான அலபாஸ்டர் சிற்பிகளால் பயன்படுத்தப்பட்டுள்ளது. ஜிப்சத்தினை, எவ்வாறு பாரீஸ்சாந்தாக மாற்றுவது என்பதை சுமார் 5000 ஆண்டுகளுக்கு முன்பே எகிப்தியர்களால் அறியப்பட்டுள்ளது. தற்போது மனித சமுதாயத்தில் ஜிப்சம் பல பயன்பாடுகளைக் கொண்டுள்ளது. அவற்றின் சில பயன்கள் கீழே கொடுக்கப்பட்டுள்ளது.
∙ உலர் பலகைகள், பூச்சுப் பலகைகள் தயாரிப்பதில் ஜிப்சம் பயன்படுகிறது. சுவர்களுக்கு இறுதி வடிவம் கொடுக்கவும், மேற்கூரைகள் மற்றும் அறைகளை பகுதிகளாக பிரிக்கவும் பூச்சுப் பலகைகள் பயன்படுகின்றது.
∙ ஜிப்சத்தின் மற்றுமொரு பயன்பாடு பாரீஸ்சாந்து தயாரிப்பதாகும். ஜிப்சத்தினை 300 டிகிரி பாரன்ஹீட்டில் சூடுபடுத்தி பாரீஸ்சாந்து தயாரிக்கப்படுகிறது. இது ஜிப்சம் பூச்சு எனவும் அழைக்கப்படுகிறது. முக்கியமாக இது சிற்பங்களை வடிப்பதில் பயன்படுகிறது.
∙ ஜிப்சம் எலும்பியல் துறையில் எலும்பு முறிவு சரிசெய்யும் கட்டுகள் மற்றும் அச்சுகள் தயாரிக்க பயன்படுகிறது.
∙ வேளாண்மைத் துறையில், மண்ணுடன் சேர்க்கப்படும் பொருளாகவும், கட்டுப்படுத்தியாகவும், உரமாகவும் பயன்படுகிறது. களிமண் மற்றும் இறுக்கமான மண்ணை நெகிழச் செய்வதுடன், தாவர வளர்ச்சிக்கு முக்கியமாக பயன்படும் கால்சியம் மற்றும் சல்பரை தரும் பொருளாக உள்ளது. மண்ணிற்கு அதிக உப்புத் தன்மையைத் தரும் Na+ அயனிகளை நீக்கவும் பயன்படுகிறது.
∙ ஜிப்சம் முக்கியமாக இணைத்தல் மற்றும் கெட்டியாக்கும் பண்புகளைப் பெற்றுள்ளதால் பற்பசை, ஷாம்புகள் மற்றும் முடித் தொடர்பான பொருட்களில் பயன்படுகிறது.
∙ போர்ட்லாண்டு சிமெண்டுகளில், ஜிப்சம் ஒரு முக்கியப் பகுதிப் பொருளாகும். இது கடினமாதலை தாமதப்படுத்தும் காரணியாக செயல்படும் தன்மையைப் பெற்றிருப்பதால் கான்கிரீட்டுகள் கடினமாகும் வேகத்தினைக் கட்டுப்படுத்துகிறது.
∙ அதிக அளவில் கிடைக்கும் தாதுப்பொருட்களின் முக்கியமானது ஜிப்சமாகும். இது கணக்கற்ற பயன்பாடுகளைக் கொண்டுள்ளது. இத் தாதுவானது புவி மேற்பரப்பிற்கருகில் அதிக அளவில் கிடைப்பதால் இதனை வெட்டி எடுப்பது எளிதாகும் எனினும் அதிக அளவு ஜிப்சம் வெட்டி எடுத்தால் சுற்றுச் சூழலில் குறிப்பிடத்தக்க பாதிப்புகளை ஏற்படுத்தும். ஜிப்சத்தினை மறுசுழற்ச்சி செய்ய முடியும். ஆனால் இத்தாது அதிக அளவில் கிடைப்பதால், இதன் மறுசுழற்ச்சிக்கு அதிக முக்கியத்துவம் தரப்படுவதில்லை.

படம் 5.13 ஜிப்சத்தின் பயன்கள்
4. பாரீஸ்சாந்து (Plaster of Paris), (CaSO4.1/2H2O) கால்சியம் சல்பேட் ஹெமிஹைட்ரேட்
இது கால்சியம் சல்பேட்டின் ஹெமிஹைட்ரேட்டாகும். ஜிப்சத்தை, (CaSO4.2H2O) 393K வெப்பநிலைக்கு வெப்பப்படுத்தி பாரீஸ்சாந்து பெறப்படுகிறது.
2 CaSO4.2H2O (s) → 2 CaSO4.1/2H2O + 3 H2O
393Kக்கு மேல், எவ்வித படிக நீர் மூலக்கூறும் காணப்படுவதில்லை மேலும் நீரற்ற கால்சியம் சல்பேட் CaSO4 உருவாகிறது. இது முற்றும் எரிக்கப்பட்ட சாந்து (dead burnt plaster) என அறியப்படுகிறது.
இது நீருடன் சேர்ந்து கடினமாகும் பண்பினைப் பெற்றுள்ளது போதுமான அளவு நீருடன் இதனைச் சேர்க்கும் போது இது நெகிழியைப் போன்ற பொருளாக மாறி 5 முதல் 15 நிமிடங்களில் கடினமான பொருளாக மாறுகிறது.
பயன்கள்
1. கட்டுமானத் தொழிலில் இது அதிக அளவில் பூச்சாக பயன்படுகிறது.
2. ஒரு உறுப்பில் எலும்பு முறிவு அல்லது சுளுக்கு பாதிக்கப்பட்டுள்ள இடங்களை நகராமல் இருத்தி வைக்க பயன்படுகிறது.
3. பற்சீராக்கும் துறை, அணிகலன்கள், சிலைகள் மற்றும் வார்ப்புகள் உருவாக்குவதில் இது பயன்படுகிறது.
