11 வது வேதியியல் : அலகு 1 : வேதியியலின் அடிப்படைக் கருத்துக்கள் மற்றும் வேதிக் கணக்கீடுகள்
வினைக்கட்டுப்பாட்டுக் காரணி
2. வினைக்கட்டுப்பாட்டுக் காரணி
கொடுக்கப்பட்ட வேதி வினையில், உருவாகும் வினைவிளை பொருட்களின் அளவினைத் தீர்மானிப்பதில் வேதிவினைக்கூறு விகித கோட்பாடு பயன்படுவதை முந்தையப் பாடப் பகுதியில் நாம் கற்றோம். வேதிவினைக் கூறு விகித அடிப்படையிலான அளவினைக் கொண்ட வினைபடுபொருட்களைக் கொண்டு ஒரு வினையானது நிகழ்த்தப்படும் போது, அனைத்து வினைபடுபொருட்களும், வினைவிளை பொருட்களாக மாற்றப்படுகிறது. மாறாக, வேதிவினைக் கூறு விகித அடிப்படையில் அமையாத அளவினைக் கொண்ட வினைபடு பொருட்களைக் கொண்டு, வினை நிகழ்த்தப்படும் போது, உருவாகும் விளை பொருளின் அளவானது, எந்த வினைபடுபொருள் முதலில் முழுவதும் வினைபடுகிறதோ, அந்த வினைபடுபொருளைச் சார்ந்து அமையும். இவ்வினைபடு பொருள் வினை தொடர்ந்து நிகழ்வதைக் கட்டுப்படுத்துகிறது, இது வினை கட்டுப்பாட்டுக் காரணி என அழைக்கப்படுகிறது. மற்ற வினைப் பொருட்கள், மிகுதியான வினைப் பொருட்கள் எனப்படுகின்றன.
வேதிவினைக் கூறு விகித கோட்பாட்டினை புரிந்து கொள்ள பயன்படுத்திய ஒப்புமையான கேசரி தயாரித்தலை நினைவுகூர்க.
அதில் குறிப்பிடப்பட்ட தயாரிப்பு முறையின் படி, ஒவ்வொரு கப் ரவாவிற்கும் இரண்டு கப் சர்க்கரை தேவைப்படும். 8 கப் சர்க்கரையும், 3 கப் ரவாவும் உள்ள ஒரு நிலையைக் கருதுக. (பிற தேவையான அனைத்துப் பொருட்களும் கூடுதலாக உள்ளது) சமையல் குறிப்பின்படி, 3 கப் ரவா மற்றும் 6 கப் சர்க்கரையினைப் பயன்படுத்தி 18 கப் கேசரியினைத் தயாரிக்க இயலும். நம்மிடம் கூடுதலாக 2 கப் சர்க்கரை இருந்த போதிலும் நம்மால் கூடுதலாக கேசரியினை தயாரிக்க இயலாது. ஏனெனில், தேவையான ரவா நம்மிடம் இல்லை. எனவே, இந்நிகழ்வில் தயாரிக்கப்படும் கேசரியின் அளவினை ரவா கட்டுப்படுத்துகிறது. இந்த ஒப்புமையினை, பின்வரும் வேதிவினைக்கு நீட்டிப்போம். மூன்று மோல் சல்பரானது பன்னிரெண்டு மோல் புளூரினுடன் வினைபுரிந்து சல்பர்ஹெக்சா புளுரைடை உருவாக்க அனுமதிக்கப்படுகிறது.
இவ்வினைக்கான சமன்படுத்தப்பட்ட சமன்பாடானது
S + 3F2 → SF6
வேதிவினைக் கூறு விகித அடிப்படையில்,
1 மோல் சல்பர், 3 மோல் புளூரினுடன் வினைபுரிந்து. 1 மோல் சல்பர்ஹெக்சா புளூரைடைத் தருகிறது. எனவே மூன்று மோல் சல்பர், 9 மோல் புளூரினுடன் வினைபுரிந்து, மூன்று மோல் சல்பர் ஹெக்சா புளூரைடைத் தரும். இந் நேர்வில், எடுத்துக் கொள்ளப்பட்ட அனைத்து சல்பர் மூலக்கூறுகளும் வினைபுரிந்து விட்டதால், இவ்வினை தொடர்ந்து நிகழ்வதை சல்பர் கட்டுப்படுத்துகிறது எனவே சல்பர் ஆனது வினைக் கட்டுப்படுத்தும் காரணி மற்றும் புளூரின் ஆனது மிகுதியான காரணி ஆகும். இந்நேர்வில் மூன்று மோல் புளூரின் மிகுதியாக எஞ்சியுள்ளது. மேலும் இவை வினைபுரிவதில்லை.
தன்மதிப்பீடு
7) ஒரு வினையின் சமன்படுத்தப்பட்ட சமன்பாடு கீழே கொடுக்கப்பட்டுள்ளது
2x + 3y → 4l + m
8 மோல் x ஆனது 15 மோல் y உடன் வினைபுரிய அனுமதிக்கப்படும் போது,
i) வினைக்கட்டுப்பாட்டு காரணி எது?
ii) உருவாகும் வினைவிளை பொருட்களின் அளவினைக் கணக்கிடுக.
iii) வினையின் இறுதியில், மிகுதியாக எஞ்சியிருக்கும் வினைபடுபொருளின் அளவினைக் கணக்கிடுக.
தீர்வு
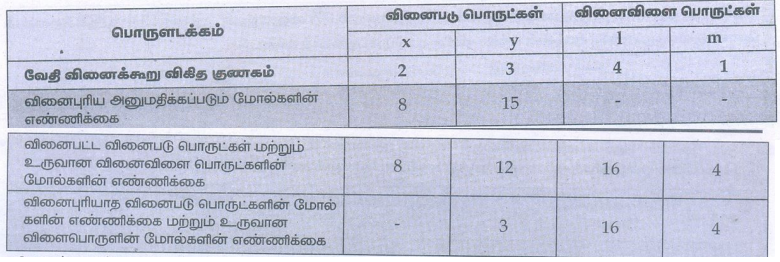
வினைக் கட்டுப்பாட்டுக் காரணி : x
உருவான விளைபொருள் : 16 மோல்கள் 1 மற்றும் 4 மோல்கள் m
கூடுதலாக எஞ்சியுள்ள வினைபடு பொருள் : 3 மோல்கள் y
யூரியாவானது நைட்ரஜனை அடிப்படையாகக் கொண்ட பொதுவாக பயன்படுத்தப்படும் ஒரு உரம் ஆகும். இது அம்மோனியா மற்றும் கார்பன் டை ஆக்ஸைடு ஆகிய வினை பொருட்களுக்கு இடையே நிகழும் பின்வரும் வேதிவினையின் மூலம் தயாரிக்கப்படுகிறது.
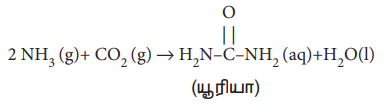
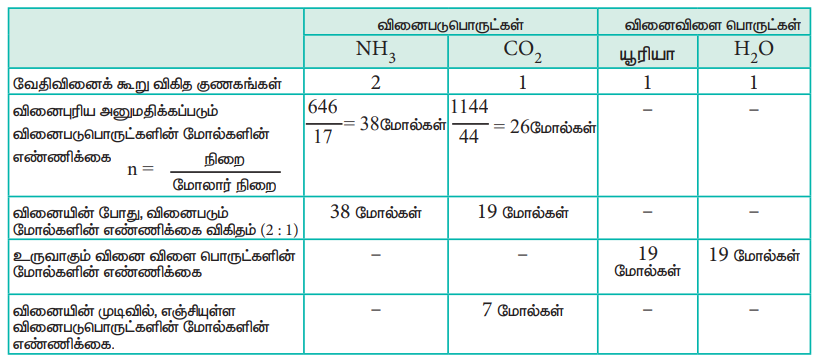
ஒரு செயல்முறையில், 646 g அம்மோனியாவானது, 1.144 kg CO2 உடன் வினையுரிய அனுமதிக்கப்பட்டு, யூரியா உருவாக்கப்படுகிறது என்க.
1) அனைத்து வினைபடு பொருட்களும், முழுவதுமாக வினையில் ஈடுபடுவதில்லை எனில், வினைகட்டுப்பாட்டுக் காரணி யாது?
2) உருவாகும் யூரியாவின் அளவினைக் கண்டறிக. மேலும் வினைபுரியாமல் மிகுதியாக உள்ள வினைக்காரணியைக் கண்டறிக.
சமன்படுத்தப்பட்ட சமன்பாடு,
2 NH3 (g) + CO2 (g) → H2NCONH2 (aq) + H2O (l)
தீர்வு:
1) இவ்வினையில் அம்மோனியா முழுவதும் வினைபடுகிறது. எனவே அம்மோனியா வினை கட்டுபாட்டுக் காரணி ஆகும். CO2 முழுவதும் வினைபுரியாமல் எஞ்சியுள்ளது எனவே CO2 மிகுதியாக உள்ள வினைக் காரணியாகும்.
2) உருவாகும் யூரியாவின் அளவு
= உருவான யூரியாவின் மோல்களின் எண்ணிக்கை × யூரியாவின் மோலார் நிறை
= 19 மோல்கள் × 60 g mol-1
= 1140 g = 1.14 kg
வினைபுரியாமல் எஞ்சியுள்ள CO2 அளவு
= எஞ்சியுள்ள CO2 மோல்களின் எண்ணிக்கை × CO2 மோலார் நிறை
= 7 மோல்கள் × 44 g mol-1
= 308 g.