11 வது வேதியியல் : அலகு 13 : ஹைட்ரோகார்பன்கள்
ஆல்கைன்களின் இயற்பியல் மற்றும் வேதியியல் பண்புகள்:
ஆல்கைன்களின் இயற்பியல் பண்புகள்:
1. படிவரிசையின் முதன் மூன்று சேர்மங்கள் வாயுக்களாகும். அதனை தொடர்ந்து வரும் எட்டு சேர்மங்கள் நீர்மங்களாகும் மற்றும் உயர் ஆல்கைன்கள் திட நிலையில் உள்ளன. அசிட்டிலீனை தவிர பிற அனைத்தும் நிறம் மற்றும் மணமற்றவை. அசிட்டிலீன் பூண்டின் மணமுடையது.
2. இவை நீரில் சிறிதளவு கரையும். ஆனால் கரிமக் கரைப்பான்களான பென்சீன், அசிட்டோன் மற்றும் எத்தில் ஆல்கஹால் ஆகியவற்றில் எளிதில் கரையும்.
ஆல்கைன்களின் வேதியியல் பண்புகள்
முப்பிணைப்பு கார்பனில் ஹைட்ரஜன் கொண்ட ஆல்கைன்கள் அமிலத்தன்மை வாய்ந்தது. இவை பலபடியாக்கல் மற்றும் சேர்க்கை வினைகளில் ஈடுபடும்.
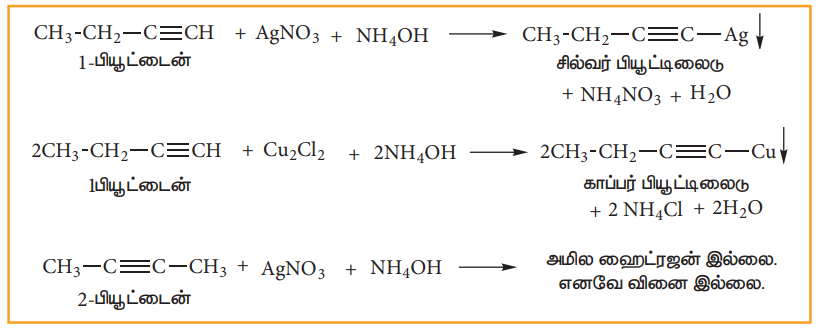
1. ஆல்கைன்களின் அமிலத் தன்மை:
ஆல்கைன்கள் முப்பிணைப்பு கார்பனில் ஹைட்ரஜன் கொண்டிருப்பின் அமிலத் தன்மை வாய்ந்தவையாக உள்ளன. இப்பண்பினை ஆல்கைன்களில் உள்ள sp இனக்கலப்பு கார்பன் அணுக்களைக் கொண்டு விளக்கலாம். sp - இனக்கலப்பு ஆர்பிட்டாலின் (50%) s-பண்பு உள்ளது. இது ஆல்கீனில் உள்ள sp2 இனக்கலப்பு ஆர்பிட்டாலின் (33%) மற்றும் ஆல்கேனில் உள்ள sp3 இனக்கலப்பு ஆர்பிட்டாலின் (25%) ஆகியவற்றை விட அதிகம். இதன் விளைவாக, கார்பன் அதிக எலக்ட்ரான் கவர் தன்மை பெறுவதால், காரங்களுக்கு H+ அயனிகளை வழங்குதல் எளிதாக நிகழ்கிறது. எனவே முப்பிணைப்பு கார்பன் அணுக்களுடன் இணைந்துள்ள ஹைட்ரஜன் அமிலத் தன்மை உடையதாகும்.
2. ஆல்கைன்களின் சேர்க்கை வினை
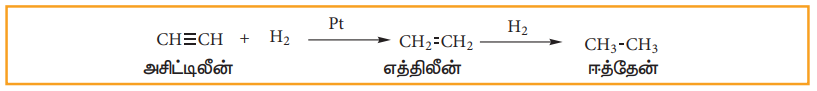
i) ஹைட்ரஜனை சேர்த்தல்
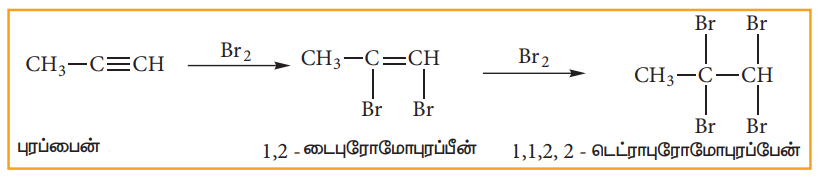
ii) ஹாலஜனை சேர்த்தல்:
CCl4 ல் உள்ள Br2 யை (செம்பழுப்பு) ஆல்கைன்களுடன் சேர்க்கும்போது, புரோமின் கரைசல் நிறமற்றதாகின்றது. இதுவே நிறைவுறா தன்மையை கண்டறிவதற்கான சோதனையாகும்.
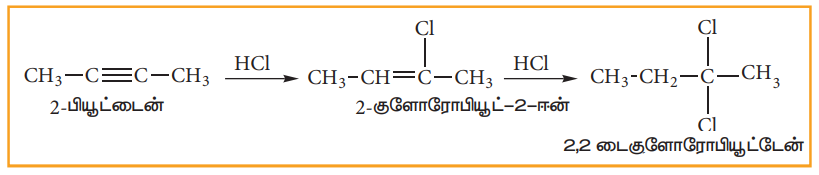
iii) ஹைட்ரஜன் ஹாலைடுகளை சேர்த்தல்:
சீர்மையான ஆல்கைன்களுடன் ஹைட்ரஜன் ஹாலைடுகள் வினைபுரிவது எலக்ட்ரான் கவர்பொருள் சேர்க்கை வினையாகும். இவ்வினை மார்கோனிகாஃப் விதியினை பின்பற்றுகின்றன.
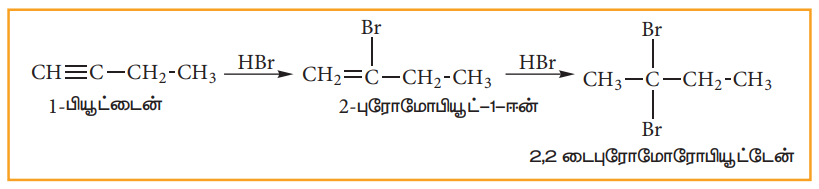
சீர்மையற்ற ஆல்கைனுடன் HBr சேர்க்கை வினையானது மார்கோனிகாஃப் விதியின் படி நடைபெறுகின்றது.
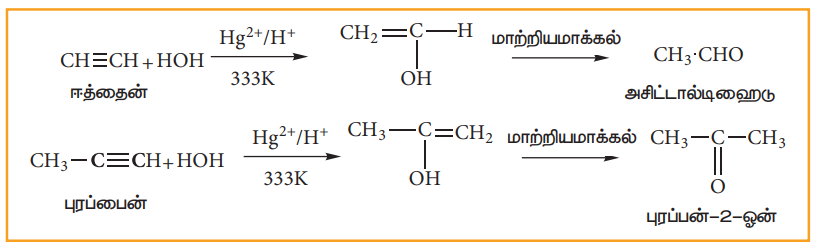
iv) நீரினை சேர்த்தல்:
ஆல்கைன்களை மெர்குரிக் சல்பேட் மற்றும் நீர்த்த கந்தக அமிலத்தின் H2SO4 முன்னிலையில் 333K வெப்பநிலையில், வெப்பப்படுத்துவதால் நீரேற்றம் அடைந்து கார்பனைல் சேர்மங்களைத் தருகின்றன.
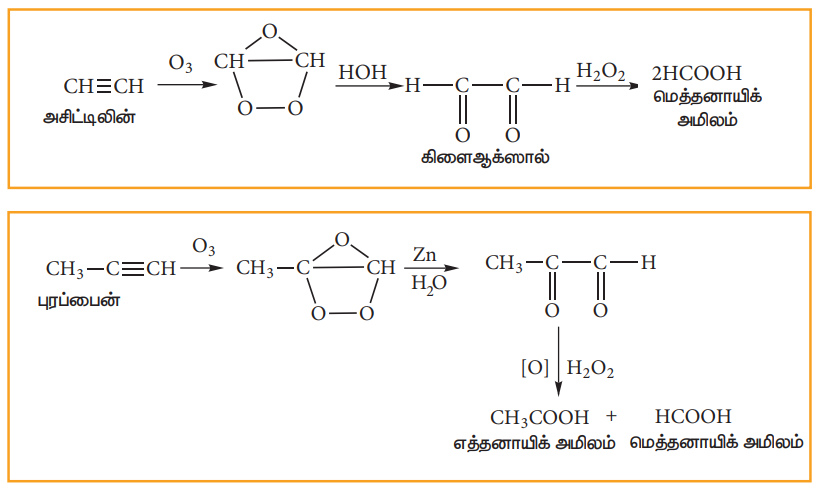
3. ஓசோனேற்றம்:
ஆல்கைன்களின் முப்பிணைப்பில், ஓசோன் இணைந்து ஓசோனைடுகளைத் தருகின்றன. இவை நீரினால் நீராற்பகுக்கப்பட்டு கார்பனைல் சேர்மங்களைத் தருகின்றன. இவ்வினையில் உருவாகும் ஹைட்ரஜன் பெராக்ஸைடு (H2O2), கார்பனைல் சேர்மங்களை கார்பாக்ஸிலிக் அமிலங்களாக ஆக்சிஜனேற்றம் செய்கின்றன.
4. பலபடியாக்கல்:
ஆல்கைன்கள் இரண்டுவகையான பலபடியாக்கல் வினைக்கு உட்படுகின்றன
(i) நேரிய பலபடியாக்கல்:
ஈத்தைனை, குப்ரஸ்குளோரைடு மற்றும் அமோனியம் குளோரைடு கரைசல்கள் வழியாக செலுத்தும் போது, நேரிய பலபடியை உருவாக்குகின்றது.
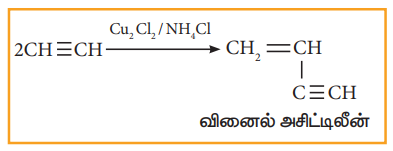
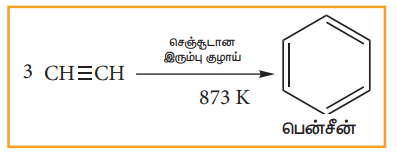
(ii) வளைய பலபடியாக்கல்
செஞ்சூடான இரும்பு குழாயின் வழியே ஈத்தைனை செலுத்தும் போது, வளைய பலபடியாக்கல் நடைபெறுகின்றது. மூன்று ஈத்தைன் மூலக்கூறுகள் பலபடியாக்கலுக்கு உட்பட்டு பென்சீனைத் தருகின்றது.