11 வது வேதியியல் : அலகு 5 : கார மற்றும் காரமண் உலோகங்கள்
பாடச்சுருக்கம்
பாடச்சுருக்கம்
நவீன தனிம வரிசை அட்டவணையில் தொகுதி-1 மற்றும் தொகுதி-2ல் அடங்கியுள்ள தனிமங்களின் இணைதிற எலக்ட்ரான்கள் s ஆர்பிட்டாலில் இடம் பெறுவதால் இவை s - தொகுதி தனிமங்கள் என்றழைக்கப்படுகின்றன. முதல் தொகுதி தனிமங்கள் ns1 என்ற பொதுவான எலக்ட்ரான் அமைப்பினைப் பெற்றிருக்கின்றன. இவை கார உலோகங்கள் எனப்படுகின்றன. தொகுதி 2 தனிமங்கள் ns2 என்ற பொதுவான எலக்ட்ரான் அமைப்பினைப் பெற்றுள்ளன. இவை காரமண் உலோகங்கள் என அழைக்கப்படுகின்றன. இவை புவிமேலோட்டில் காணப்படுகின்றன. இவற்றின் ஆக்சைடுகள் மற்றும் ஹைட்ராக்சைடுகள் காரத்தன்மை உடையவை. இவை அதிக வினைத்திறனை உடையவை மேலும் M+ மற்றும் M2+ நேர் அயனிகளை உருவாக்குகின்றன. இவ்விரு தொகுகளிலும் மேலிருந்து கீழாக வரும்போது இயற் மற்றும் வேதிப்பண்புகள் சீராக மாற்றமடைகின்றன. தொகுதியில் மேலிருந்து கீழாக வரும் போது அணு மற்றும் அயனி ஆரம் அதிகரிக்கின்றது. அனால் அயனியாக்கும் ஆற்றல் குறைகிறது.
சோடியத்தின் முக்கியச் சேர்மங்கள் சோடியம் கார்பனேட், சோடியம் குளோரைடு, சோடியம் ஹைட்ராக்சைடு மற்றும் சோடியம் ஹைட்ரஜன் கார்பனேட் ஆகியவை. காஸ்ட்னர் – கெல்னர் முறையில் சோடியம் ஹைட்ராக்சைடு பெருமளவில் தயாரிக்கப்படுகிறது. சால்வே முறையில் சோடியம் கார்பனேட் தயாரிக்கப்படுகிறது.
காரமண் உலோகங்களின் வேதியியல், கார உலோகங்களின் வேதியியலோடு ஒத்துள்ளது. எனினும், காரமண் உலோகங்களின் குறைந்த அணு மற்றும் அயனி உருவளவு, நேர் அயனிகளின் மீதான அதிக மின்சுமை ஆகியவற்றால் சில பண்புகளில் மாறுபட்டுள்ளன. கார உலோக ஆக்சைடுகள் மற்றும் ஹைட்ராக்சைடுகளைக் காட்டிலும், கார உலோக ஆக்சைடுகள் மற்றும் ஹைட்ராக்சைடுகள் குறைவான காரத்தன்மையினைப் பெற்றுள்ளன. காரமண் உலோகங்களும், ஹைட்ரஜன் மற்றும் ஹேலஜன்களுடன் இணைந்து முறையே ஹைட்ரைடுகள் மற்றும் ஹேலைடுகளைத் தருகின்றன.
கால்சியம் ஆக்சைடு (சுட்ட சுண்ணாம்பு), கால்சியம் ஹைட்ராக்சைடு (நீர்த்த சுண்ணாம்பு), கால்சியம் சல்பேட் ஹெமிஹைட்ரேட் (பாரீஸ்சாந்து) கால்சியம் கார்பனேட், சோடா சுண்ணாம்பு ஆகியவை கால்சியத்தின் முக்கியச் சேர்மங்களாகும். சுண்ணாம்புக்கல் மற்றும் களிமண்ணை பயன்படுத்தி, சுழற்றும் சூலையில் வெப்பப்படுத்தி, போரட்லேண்ட் சிமெண்ட் தயாரிக்கப்படுகிறது. கிடைக்கும் விளைபொருள் 2 - 3% அளவுள்ள நன்கு தூள் செய்யப்பட்ட ஜிப்சத்துடன் சேர்க்கப்படுகிறது. கால்சியத்தின் அனைத்து சேர்மங்களும் வெவ்வேறு பயன்களைக் கொண்டுள்ளன.
உயிர்த் திரவங்களில் (Biological Fluids) சோடியம் மற்றும் பொட்டாசியத்தின் ஒற்றை இணைதிற அயனிகள் மற்றும் கால்சியம் மற்றும் மெக்னீசியத்தின் இரு இணைதிற அயனிகள் ஆகியன காணப்படுகின்றன. இந்த அயனிகள் அயனிச் சமநிலைத் தன்மை மற்றும் நரம்பு தூண்டல்களை கடத்துதலில் முக்கியப் பங்காற்றுகின்றன.
கருத்து வரைபடம்
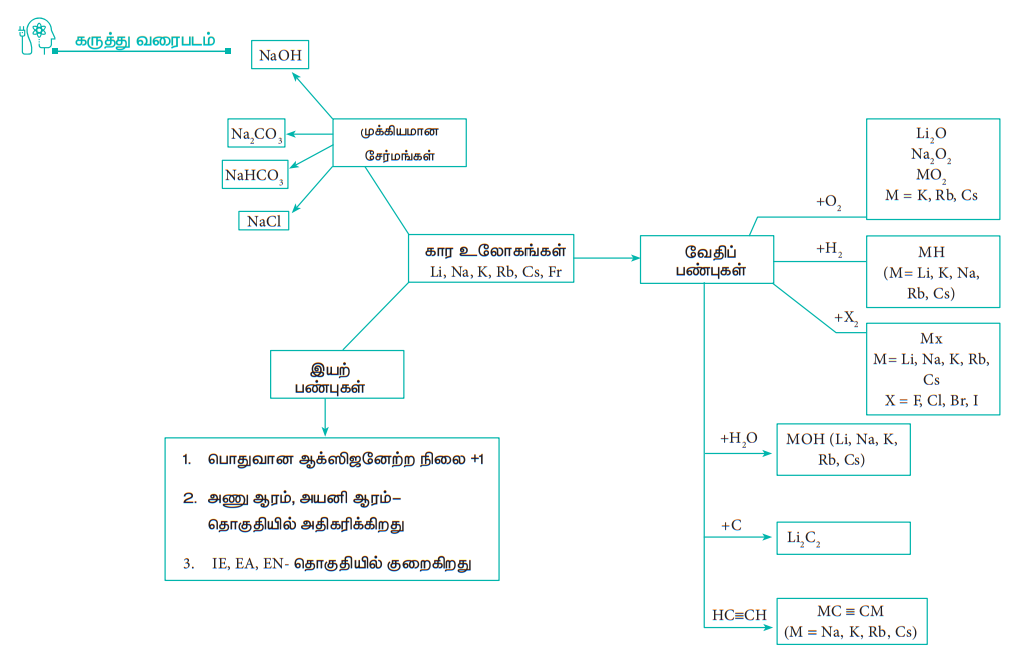
இணையச் செயல்பாடு
கார மற்றும் காரமண் தனிமங்களுக்கான சுடர் ஆய்வு (மெய்நிகர் ஆய்வகம்)
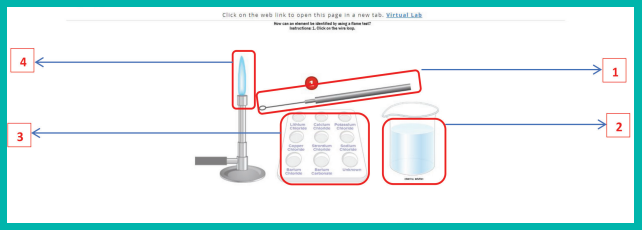
நிலை 1: இணையப்பக்கத்தினைத் திறந்து கொடுக்கப்பட்ட உரலியைத் (URL) தட்டச்சு செய்க அல்லது விரைவுத் துலக்கக் குறியீட்டினை ஸ்கேன் செய்க. சுடர் ஆய்வுக் காட்சிப் பலகையில் காட்சிப் பொத்தானைச் சொடுக்குக. படத்திலிருப்பது போன்ற கூடர் ஆய்விற்கான வலைப்பக்கத்தினை காணலாம்.
நிலை 2: மெய்நிகர் சுடர் ஆய்வினை மேற்கொள்ள கீழ்க்காணும் நெறிகளைப் பின்பற்றுக.
1. வளைவுக் கம்பியின் (1) மீது சொடுக்குக.
2. வளைவுக் கம்பியைச் சுத்தப்படுத்தும் கரைசலுக்குள் (2) நகர்த்துக. சுத்தப்படுத்தும் கரைசலின் மீது சொடுக்குக. வளைவுக் கம்பியில் வேறேதும் உப்பு இல்லை என்பதை உறுதி செய்ய ஒவ்வொரு ஆய்விற்கு முன்பும் கம்பி சுத்தம் செய்யப்படவேண்டும்.
3. ஆய்வு செய்ய விழையும் உப்புக் கரைசலில் (3) வளைவுக் கம்பியைச் செலுத்துக. உப்புக் கரைசலின் மீது சொடுக்குக.
4. வளைவுக்கம்பியை சுடரின் (4) மீது நகர்த்தி அதன்மீது சொடுக்குக.
5. குறிப்பிட்ட உலோக அயனிக்கேற்றவாறு சுடரின் நிறம் மாறுவதைக் காணலாம்.
Ppppppppp