11 வது வேதியியல் : அலகு 7 : வெப்ப இயக்கவியல்
எரிதல் வெப்பத்தின் பயன்பாடுகள்
எரிதல் வெப்பத்தின் பயன்பாடுகள்:
(1) உருவாதல் வெப்பத்தை கணக்கிடுதல்:
கரிம சேர்மங்களின் எரிதல் வெப்பத்தை எளிதில் அளவிட முடியும் என்பதால், இதைப் பயன்படுத்தி மற்ற சேர்மங்களின் உருவாதல் வெப்பத்தை கணக்கிடமுடியும்.
எடுத்துக்காட்டாக மீத்தேனின் திட்ட உருவாதல் என்தால்பி (ΔHf0) மதிப்பை கணக்கிடுவோம். H2,C (கிராஃபைட்) மற்றும் CH4 ஆகியவற்றின் எரிதல் என்தால்பி மதிப்புகள் முறையே -285.8, -393.5 மற்றும் -890.4 kJ mol-1.
பின்வருமாறு சமன்பாடுகளை எழுதுவதன் மூலம் உருவாதல் என்தால்பியை விளக்க முடியும். திட்ட வெப்ப அழுத்த நிலைகளில், தூயநிலையிலுள்ள, தனித்த வாயுக்கள் மற்றும் தனிமங்களின் திட்ட உருவாதல் என்தால்பி மதிப்புகள் பூஜ்ஜியம் என எடுத்துக் கொள்ளப்படுகின்றன. மீத்தேன் அதன் தனிமங்களிலிருந்து உருவாவதற்கான வெப்ப வேதிச் சமன்பாடுகள்
C(கிராஃபைட்) + 2H2 (g) → CH4(g)
ΔHf0 = X kJ mol-1 ---------- (i)
கொடுக்கப்பட்ட சேர்மங்களின் எரிதல் வினைக்கான வெப்ப வேதிச் சமன்பாடுகள்
H2 (g) + 1/2 O2 (g) → H2O (l)
ΔH0 = - 285.8 kJ mol-1 ---------- (ii)
C(கிராஃபைட்) (s) + O2 (g) → CO2 (g)
ΔH° = - 393.5 kJ mol-1 ---------- (iii)
CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (l)
ΔH° = - 890.4 kJ mol-1 ---------- (iv)
தேவைப்படும் சமன்பாடு (i)ல் மீத்தேன், விளைபொருள் பக்கத்தில் இருப்பதால், சமன்பாடு (iv) ன் மறுதலையை (reverse) எழுத வேண்டும்.
CO2 (g) + 2 H2O (l) → CH4 (g) + 2O2
ΔH° = + 890.4 kJ mol-1 ---------- (v)
சமன்பாடு (i) ஐ பெற
(i) = [(ii) × 2] + (iii) + (v)
X = [(- 285.8) × 2] + [- 393.5] + [+ 890.4]
= - 74.7kJ
1 மோல் மீத்தேன் உருவாதலின்போது வெளிப்படும் வெப்பம் = - 74.7 kJ
மித்தேனின் உருவாதல் வெப்பம் = - 74.7 kJmol-1
(2) உணவுப் பொருட்கள் மற்றும் எரிபொருட்களின் கலோரி மதிப்புகளை கணக்கிடுதல்:
ஒரு கிராம் பொருளை முழுமையாக எரிக்கும்போது வெளிப்படும் வெப்பத்தின் அளவு (கலோரிகளில் அல்லது ஜூல்களில்) அச்சேர்மத்தின் கலோரி மதிப்பு என வரையறுக்கப்படுகிறது. இதன் SI அலகு JKg-1. எனினும் இது வழக்கமாக cal g-1 எனும் அலகில் குறிப்பிடப்படுகிறது.
கரைசல் வெப்பம் :
ஒரு பொருள் ஒரு கரைப்பானில் கரைக்கப்படும் போது பொதுவாக வெப்பமாற்றம் உணரப்படுகிறது. குறிப்பிட்ட வெப்பநிலையில், ஒருமோல் சேர்மத்தை, குறிப்பிட்ட அளவுள்ள கரைப்பானில் கரைக்கும் போது ஏற்படும் வெப்பமாற்றம் அச்சேர்மத்தின் கரைசல் வெப்பம் என வரையறுக்கப்படுகிறது.
நடுநிலையாக்கல் வெப்பம்:
நீர்த்தகரைசலில், ஒரு கிராம் சமான நிறை கொண்ட ஒருஅமிலமானது, ஒரு கிராம் சமான நிறை கொண்ட ஒருகாரத்தால் முற்றிலும் நடுநிலையாக்கப்படும் போது, ஏற்படும் என்தால்பி மாற்றம் நடுநிலையாக்கல் வெப்பம் என வரையறுக்கப்படுகிறது.
HCl (aq) + NaOH (aq) → NaCl (aq) + H2O (l) ΔH = - 57.32 kJ
H+ (aq) + OH- (aq) → H2O (l) ΔH = - 57.32 kJ
எந்த ஒரு வலிமை மிகு அமிலம் மற்றும் வலிமை மிகு காரம் ஆகியவற்றின் நடுநிலையாக்கல் வெப்ப மதிப்பு ஏறக்குறைய - 57.32 kJ. அமிலம் அல்லது காரத்தின் தன்மையை பொறுத்து இம்மதிப்பு மாறுவதில்லை, பின்வரும் எடுத்துக்காட்டுகள் இதற்குச் சான்றாக அமைகின்றன.
HCl (aq) + KOH (aq) → KCl (aq) + H2O (l) ΔH = - 57.32 kJ
HNO3 (aq) + KOH (aq) → KNO3 (aq) + H2O (l) ΔH = - 57.32 kJ
H2SO4 (aq) + 2 KOH (aq) → K2SO4 (aq) + 2 H2O (l) ΔH = - 57.32 kJ × 2
அமில காரங்கள் பற்றிய அர்ஹீனியஸ் கொள்கை மூலம் இதற்கான காரணத்தினை விளக்கமுடியும். இக்கொள்கைப்படி "வலிமை மிகு அமிலங்கள், மற்றும் வலிமை மிகுகாரங்கள் அவற்றின் நீர்க்கரைசல்களில் முற்றிலும் அயனிகளாக பிரிகையுற்று முறையே H+ மற்றும் OH- அயனிகளைத் தருகின்றன. எனவே மேற்கூறிய அனைத்து வினைகளிலும் நிகழும் நடுநிலையாக்கல் வினையினை பின்வருமாறு குறிப்பிடலாம்
H+ (aq) + OH- (aq) → H2O (l) ΔH = - 57.32 kJ
மோலார் உருகுதல் வெப்பம்:
ஒரு மோல் திண்மப்பொருள், அதன் உருகுநிலையில் திரவநிலைக்கு மாற்றப் படும்போது, ஏற்படும் என்தால்பி மாற்றம், அதன் மோலார் உருகுதல் வெப்பம் என வரையறுக்கப்படுகிறது.
எடுத்துக்காட்டாக பனிக்கட்டியின் உருகுதல் வெப்பத்தை பின்வருமாறு குறிப்பிட முடியும்.
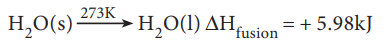
மோலார் ஆவியாதல் வெப்பம்:
ஒரு மோல் நீர்மம், அதன் கொதி நிலையில் ஆவிநிலைக்கு மாற்றப்படும்போது ஏற்படும் என்தால்பி மாற்றம், அதன் மோலார் ஆவியாதல் வெப்பம் என வரையறுக்கப்படுகிறது.
எடுத்துக்காட்டாக நீரின் ஆவியாதல் வெப்பத்தை பின்வருமாறு குறிப்பிட முடியும்
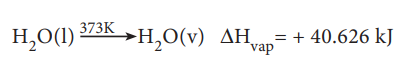
மோலார் பதங்கமாதல் வெப்பம்:
ஒரு திண்மம் அதன் திரவ நிலைக்கு மாறாமல், நேரடியாக வாயு நிலைக்கு மாறும் ஒரு செயல்முறை பதங்கமாதல் எனப்படுகிறது. ஒரு மோல் திண்மப்பொருளை, அதன் பதங்கமாதல் வெப்பநிலையில் நேரடியாக ஆவிநிலைக்கு மாற்றப்படும் போது ஏற்படும் என்தால்பி மாற்றம், அப்பொருளின் மோலார் பதங்கமாதல் வெப்பம் என வரையறுக்கப்படுகிறது. எடுத்துக்காட்டாக அயோடினின் பதங்கமாதல் வெப்பத்தை பின்வருமாறு குறிப்பிடமுடியும்.
I2 (s) → I2 (v) ΔHsub = + 62.42 kJ
மிகக் குறைந்த வெப்பநிலையில் வளிமண்டல அழுத்தத்தில் திண்ம கார்பன் – டை - ஆக்சைடானது வாயுநிலைக்கு மாறுவது, பதங்கமாதல் செயல்முறைக்கு மற்றுமொரு எடுத்துக்காட்டாகும்.
நிலைமாற்ற வெப்பம்:
ஒரு மோல் தனிமம், அதன் ஒரு புறவேற்றுமை வடிவத்திலிருந்து, மற்றொரு புறவேற்றுமை வடிவத்திற்கு மாற்றமடையும்போது ஏற்படும் என்தால்பி மாற்றம், நிலைமாற்ற வெப்பம் என வரையறுக்கப்படுகிறது.
எடுத்துக்காட்டாக வைரம் அதன் புறவேற்றுமை வடிவமான கிராஃபைட்டாக மாற்றமடையும் வினையை குறிப்பிடலாம்.

இதைப் போலவே சல்பர் மற்றும் பாஸ்பரஸின் புற வேற்றுமை வடிவங்களுக்குக்கிடையே மாற்றத்தினை பின்வருமாறு குறிப்பிடலாம்..
S(மோனோக்ளினிக்) → S(ரோம்பிக்) ΔHtrans = - 0.067 kJ
P(வெண்மை) → P(சிவப்பு) ΔHtrans = - 4.301 kJ