பல்வேறு வினாக்களுக்கான கேள்வி பதில்கள் - சரியான விடையினைத் தேர்வு செய்க | 11th Chemistry : UNIT 8 : Physical and Chemical Equilibrium
11 வது வேதியியல் : அலகு 8 : இயற் மற்றும் வேதிச்சமநிலை
சரியான விடையினைத் தேர்வு செய்க
மதிப்பீடுக
சரியான விடையினைத் தேர்வு செய்க
1. ஒரு மீள் வினையின் Kp மற்றும் Kf மதிப்புகள் முறையே 0.8 × 10-5 மற்றும் 1.6 × 10-4 எனில், சமநிலை மாறிலியின் மதிப்பு ---------
அ) 20
ஆ) 0.2 × 10-1
இ) 0.05
ஈ) இவற்றில் ஏதுமில்லை
[விடை : அ) 20]
தீர்வு:
1. Kp = 0.8 × 10-5 ; Kf = 1.6 × 10-4; KC = ?
KC = Kf / Kp = 1.6 × 10-4 / 0.8 × 10-5 = 20
2. 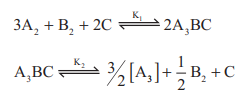
ஆகிய சமநிலைகளுக்கு ஒரு குறிப்பிட்ட வெப்பம் மற்றும் அழுத்த நிலையில் சமநிலை மாறிலிகளின் மதிப்புகள் கொடுக்கப்பட்டுள்ளன. K1 மற்றும் K2 விற்கு இடையேயான தொடர்பு யாது?
அ) K1 = 1 / √K2
ஆ) K2 = K1 -1/2
இ) K12 = 2K2
ஈ) K1 / 2 = K2
[விடை : ஆ) K2 = K1 -1/2 ]
தீர்வு:
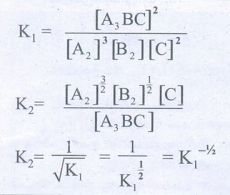
3. ஒரு வினையின் சமநிலை மாறிலி அறைவெப்பநிலையில் K1 மற்றும் 700K ல் K2 ஆகும். K1 > K2 எனில்,
அ) முன்னோக்கு வினை ஒரு வெப்பம் உமிழ்வினை.
ஆ) முன்னோக்கு வினை ஒரு வெப்பம் கொள்வினை.
இ) இவ்வினை சமநிலையை அடையாது.
ஈ) பின்னோக்கு வினை ஒரு வெப்ப உமிழ்வினை
[விடை : அ) முன்னோக்கு வினை ஒரு வெப்பம் உமிழ்வினை]
தீர்வு:
வெப்பநிலை உயரும்போது K மதிப்பு குறைகிறது. எனவே முன்னோக்கு வினை வெப்பம் உமிழ்வினை.
4. N2 (g) மற்றும் H2 (g) ஆகியவற்றிலிருந்து NH3 உருவாதல் ஒரு மீள் வினையாகும்
N2 (g) + 3H2 (g) ⇌ 2NH3 (g) + வெப்பம் இவ்வினையின் மீது வெப்பநிலை உயர்வினால் ஏற்படும் விளைவு என்ன?
அ) சமநிலையில் மாற்றமில்லை.
ஆ) அம்மோனியா உருவாதலுக்கு சாதகமாக உள்ளது.
இ) சமநிலை இடது பக்கத்திற்கு நகரும்.
ஈ) வினையின் வேகம் மாறாது.
[விடை : இ) சமநிலை இடது பக்கத்திற்கு நகரும்.]
தீர்வு:
முன்னோக்கு வினை வெப்பம் உமிழ்வினை எனவே வெப்பநிலை உயர்வு பின்னோக்கு வினையை தூண்டுகிறது.
5. குளிர்ந்த நீரில் கார்பன்டை ஆக்சைடு வாயுவின் கரைதிறனை எவ்வாறு அதிகரிக்கலாம்.
அ. அழுத்தத்தினை அதிகரித்து
ஆ. அழுத்தத்தினை குறைத்து
இ. கன அளவினை அதிகரித்து
ஈ. இவற்றில் ஏதுமில்லை
[விடை : அ. அழுத்தத்தினை அதிகரித்து]
தீர்வு:
ஒரு நீர்மத்தில் வாயுவின் கரைதிறனானது அழுத்தத்தை அதிகரிக்கும் போது அதிகரிக்கிறது.
6. கீழ் கண்டவற்றில் எது சரியான கூற்று அல்ல?
அ. சமநிலையில் உள்ள ஒரு அமைப்பிற்கு Q ன் மதிப்பு எப்போதும் சமநிலை மாறிலியை விட குறைவாக இருக்கும்.
ஆ. ஒரு பக்கத்திலிருந்தும் சமநிலையினை அடையலாம்.
இ. வினையூக்கியானது முன்னோக்கு மற்றும் பின்னோக்கு வினைகளை சம அளவில் பாதிக்கும்.
ஈ. வெப்ப நிலையினை பொருத்து சமநிலை மாறிலி மதிப்புகள் மாறுபடும்.
[விடை : அ. சமநிலையில் உள்ள ஒரு அமைப்பிற்கு Q ன் மதிப்பு எப்போதும் சமநிலை மாறிலியை விட குறைவாக இருக்கும்.]
தீர்வு:
சமநிலையில் Q = KC
7. 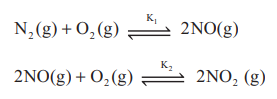
மேற்கண்டுள்ள வினைகளின் சமநிலை மாறிலிகளின் மதிப்புகள் முறையே K1 மற்றும் K2
NO2 (g) ⇌ ½ N2 (g) + O2 (g) என்ற வினையின் சமநிலை மாறிலி யாது?
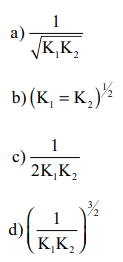
[விடை : a) 1 / √ K1 K2 ]
தீர்வு:
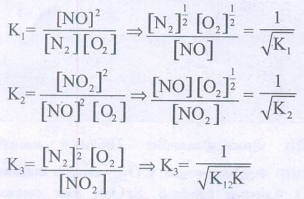
8. 2A(g) ⇌ 2B(g) + C2(g) என்ற சமநிலையில், 400K வெப்பநிலையில் A, B மற்றும் C2 வின் சமநிலைச்செறிவுகள் முறையே 1 × 10-4 M. 2.0 × 10-3 M, 1.5 × 10-4 M. 400K, வெப்பநிலையில் சமநிலையின் KC மதிப்பு யாது?
அ) 0.06
ஆ) 0.09
இ) 0.62
ஈ) 3 × 10-2
[விடை : அ) 0.06]
தீர்வு:
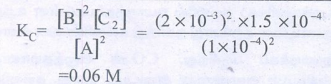
= 0.06 M
9. ஒரு வினைக்கு சமநிலை மாறிலி மதிப்பு 3.2 × 10-6 என்பதன் பொருள் சமநிலையானது
அ) பெரும்பாலும் முன்னோக்கு திசையினை நோக்கி இருக்கும்.
ஆ) பெரும்பாலும் பின்னோக்கு திசையினை நோக்கி இருக்கும்.
இ) ஒருபோதும் நிறுவ முடியாது.
ஈ) இவற்றில் ஏதுமில்லை.
[விடை : ஆ) பெரும்பாலும் பின்னோக்கு திசையினை நோக்கி இருக்கும்.]
தீர்வு:
KC = 10-3 - 10-3 ⇒ சமநிலை
KC >103 ⇒ முன்னோக்கு வினை நடைபெறும், வினை முற்றுபெறும்.
KC < 10-3 ⇒ பின்னோக்கு வினை நடைபெறும், வினை முற்றுபெறாது.
10. N2(g) + 3H2 (g) ⇌ 2NH3 (g) என்ற வினையின் Kc / Kp = ?
அ) 1/RT
ஆ) √RT
இ) RT
ஈ) ( RT)2
[விடை : ஈ) ( RT)2]
தீர்வு:
∆ng = 2 – 4 = -2
Kp = KC(RT) ∆ng
Kp = KC(RT)-2
Kp = KC (1/ (RT)2)
Kp(RT)2 = KC
KC / Kp = (RT)2
11. AB (g) ⇌ A(g) + B(g) என்ற வினையின், சமநிலையில், மொத்த அழுத்தம் P-ஆக உள்ள போது AB ஆனது 20% சிதைவடைந்தால், பின்வரும் எந்த சமன்பாட்டினால் சமநிலை மாறிலி Kp யானது மொத்த அழுத்தம் P யுடன் தொடர்படுத்தப்படும்
அ) P = 24 Kp
ஆ) P = 8 Kp
இ) 24 P = Kp
ஈ) இவற்றில் எதுவுமில்லை
[விடை : அ) P = 24 Kp]
தீர்வு:
AB (g) ⇌ A(g) + B(g)

ஃ P = 24 Kp
12. கீழ்கண்ட வினைகளில் எவ்வினைக்கு Kp மற்றும் Kc சமம் அல்ல
அ) 2 NO(g) ⇌ N2(g) + O2(g)
ஆ) SO2 (g) + NO2 ⇌ SO3(g) + NO(g)
இ) H2 (g) + I2 (g) ⇌ 2HI(g)
ஈ) PCl5 (g) ⇌ PCl3 (g) + Cl2 (g)
[விடை : ஈ) PCl5 (g) ⇌ PCl3 (g) + Cl2 (g)]
தீர்வு:
∆ng = 2 – 1 = 1
ஃ KP ≠ Kc
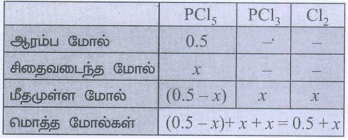
13. PCl5 ⇌ PCl3 + Cl2 என்ற வினையின், சமநிலையில், PCl5 ன் சிதைவடைதல் பின்னம் x, PCl5 ன் தொடக்கச் செறிவு 0.5 மோலாக இருந்தால், சமநிலையில் வினைபடு பொருள்கள் மற்றும் வினைவிளை பொருள்களின் மொத்த மோல்கள் எண்ணிக்கை
அ) 0.5 - x
ஆ) x + 0.5
இ) 2x + 0.5
ஈ) x + 1
[விடை : ஆ) x + 0.5 ]
தீர்வு:
PCl5 ⇌ PCl3 + Cl2;
14. X ⇌ Y + Z மற்றும் A ⇌ 2B ஆகிய வினைகளில் Kp1 மற்றும் K p2 ன் மதிப்புகள் 9:1 என்ற விகிதத்தில் உள்ளது. X மற்றும் A ன் பிரிகை வீதம் மற்றும் தொடக்கச் செறிவுகள் ஆகியன சமமாக இருந்தால், சமநிலையில் மொத்தம் அழுத்தம் P1 மற்றும் P2 வின் விகிதம் -----------
அ) 36 : 1
ஆ) 1 : 1
இ) 3 : 1
ஈ) 1 : 9
[விடை : அ) 36 : 1]
தீர்வு:

15. Fe(OH)3 (S) ⇌ Fe3+ (aq) + 3OH ̄(aq), என்ற வினையில் OH- அயனியின் செறிவு ¼ மடங்காக குறைந்தால், Fe3+ன் சமநிலைச் செறிவானது
அ) மாறாது
ஆ) ¼ மடங்காக அதுவும் குறையும்
இ) 4 மடங்காக அதிகரிக்கும்
ஈ) 64 மடங்காக அதிகரிக்கும்
[விடை : ஈ) 64 மடங்காக அதிகரிக்கும்]
தீர்வு:
[Fe3+] = a
[OH-] = b
[Fe3+] = xa
[OH-] = ¼ b
ஃ Kc = [Fe3+] [OH-]3
Kc = ab3
K1c = [Fe3+] [OH-]3
K1c = xa = (1/4 b)3 = x (ab3 / 64)
சமநிலையில் Kc = K1c
ab3 = x (ab3 /64)
1 = x/64
x = 64
16. ஒரு குறிப்பிட்ட வெப்பநிலையில், Kp = 0.5 என்ற வினையினை கருதுவோம்.
PCl5 (g) ⇌ PCl3 (g) + Cl2 (g)
ஒவ்வொரு வாயுவின் தொடக்க பகுதி அழுத்தம் 1 atm உள்ளவாறு, மூன்று வாயுக்களையும் ஒரு கலனில் எடுத்துக்கொண்டால், பின்வரும் கூற்றுகளில் எது சரியாக இருக்கும்.
அ) அதிகளவு PCl3 உருவாகும்.
ஆ) அதிகளவு Cl2 உருவாகும்
இ) அதிகளவு PCl5 உருவாகும்
ஈ) இவற்றில் ஏதுமில்லை
[விடை : இ) அதிகளவு PCl5 உருவாகும்]
தீர்வு:
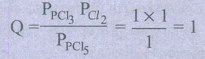
Kp = 0.5 ; ஃ Q > Kp
எனவே பின்னோக்கு வினை நடைபெறும் அதிகளவு PCl5 உருவாகும்
17. ஒரு லிட்டர் கன அளவுடைய குடுவையில், சமமோலார் செறிவுகளுடைய H2 மற்றும் I2 சமநிலை அடையுமாறு வெப்பப்படுத்தப்படுகிறது. முன்னோக்கு மற்றும் பின்னோக்கு ஆகிய இரு வினைகளின் வினைவேக மாறிலிகளின் மதிப்புகள் சமமாக இருந்தால் சமநிலையில், H2ன் தொடக்கச் செறிவில் எவ்வளவு சதவீதம் வினைக்கு உட்பட்டிருக்கும் -------------
அ) 33%
ஆ) 66%
இ) (33)2%
ஈ) 16.5 %
[விடை : அ) 33% ]
தீர்வு:
V = 1L
H2 + I2 ⇌ 2HI
[H2 ] ஆரம்பம் = [I2] ஆரம்பம் = a
[H2]eq = [I2]eq = (a-x)
மற்றும் [HI]eq = 2x
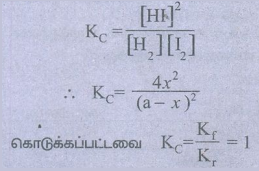
ஃ 4x2 = (a-x)2
4x2 = a2 + x2 – 2ax
3x2 + 2ax – a2 = 0
x = - a & x = a/3
பிரிகை வீதம் = a/3 × 100 = 33.33%
18. ஒரு வேதிச் சமநிலையில், முன்னோக்கு வினையின் வினைவேக மாறிலி 2.5 × 102 மற்றும் சமநிலை மாறிலி 50 எனில் பின்னோக்கு வினையின் வினைவேக மாறிலி
அ) 11.5
ஆ) 5
இ) 2 × 102
ஈ) 2 × 10−3
[விடை : ஆ) 5]
தீர்வு:
Kf = 2.5 × 102; K C = 50; K b = ?
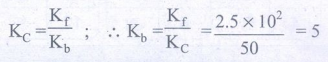
19. பின்வருவனவற்றுள் எது/எவை இயற் சமநிலை செயல்முறைகளின் பொதுவான பண்பு அல்ல?
அ) கொடுக்கப்பட்ட ஒரு வெப்பநிலையில், சமநிலையானது, ஒரு மூடிய அமைப்பில் மட்டுமே சாத்தியம்.
ஆ) எதிர் – எதிர் செய்முறைகள் ஒரே வேகத்தில் நடைபெறும் மேலும் இங்கு, நிலையான ஆனால் இயங்கு நிலை இருக்கும்.
இ) அனைத்து இயற் செயல்முறைகளும் சமநிலையில் நடைபெறாமல் நின்றுவிடும்.
ஈ) அமைப்பின் அனைத்து அளவிடப்படும் பண்புகளும் மாறாமலிருக்கும்,
[விடை : இ) அனைத்து இயற் செயல்முறைகளும் சமநிலையில் நடைபெறாமல் நின்றுவிடும்.]
தீர்வு
அனைத்து இயற்பியல் செயல்முறைகளும் சமநிலையில் சமவேகத்தில் நடைபெறும்.
20. SO2 மற்றும் O2 ஆகியவற்றிலிருந்து இரண்டு மோல்கள் SO3 உருவாகும் வினைக்கு சமநிலை மாறிலி K1 ஒரு மோல் SO3 சிதைவுற்று SO2 மற்றும் O2 ஆகியவற்றைத் தரும் வினையின் சமநிலை மாறிலி
a) 1/K1
b) K21
c) (1/K1)1/2
d) K1/2
[விடை : c) (1/K1)1/2]
தீர்வு:
2SO2(g) + O2(g) ⇌ 2SO3(g) ; K1
SO3(g) ⇌ SO2(g) + ½ O2(g) ; K2
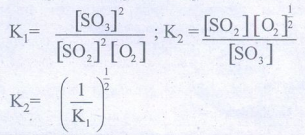
21. சமநிலைகளை அவற்றின் தொடர்புடைய நிபந்தனைகளுடன் பொருத்துக.
i. திரவம் ⇌ வாயு
ii. திண்மம் ⇌ திரவம்
iii. திண்மம் ⇌ வாயு
iv. கரைபொருள்(s) (கரைசல்) ⇌ கரைபொருள்
1. உருகுநிலை
2. செறிவூட்டப்பட்ட கரைசல்
3. கொதிநிலை
4. பதங்கமாதல்
5. செறிவூட்டப்படாத கரைசல்
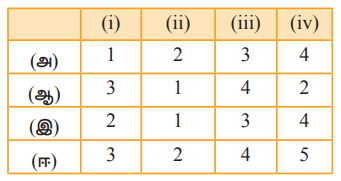
[விடை : ஆ) ]
22. A + B ⇌ C என்ற சமநிலையில் உள்ள மீள்வினையினைக் கருதுவோம், A மற்றும் B ஆகிய வினைபடுபொருட்களின் செறிவினை இருமடங்காக உயர்த்தினால், சமநிலை மாறிலியின் மதிப்பு
அ) இருமடங்காகும்
ஆ) நான்கில் ஒரு பங்காகிறது
இ) பாதியாகும்
ஈ) மாறாமலிருக்கும்
[விடை : ஈ) மாறாமலிருக்கும்]
தீர்வு:
KC மதிப்பு ஆரம்பச் செறிவைப் பொறுத்ததல்ல.
23. [Co (H2O)6] 2+(aq) (இளஞ்சிவப்பு) + 4Cl- (aq) ⇌ [CoCl4]2-(aq) (நீலம்) + 6H2O (l)
மேற்கண்ட வினையில், சமநிலையில், அறை வெப்பநிலையில், வினைக்கலவையானது நீல நிறத்திலிருக்கும். இக்கலவையை குளிர்விக்க அது இளஞ்சிவப்பு நிறமாக மாறுகிறது. கொடுக்கப்பட்டுள்ள தகவல்களின் அடிப்படையில், கீழ்கண்டவற்றில் எது சரியானது?
அ) முன்னோக்கு வினையில், ΔH > 0
ஆ) பின்னோக்கு வினையில் ΔH = 0
இ) முன்னோக்கு வினையில் ΔH < 0
ஈ) ΔH இன் குறியீட்டினை கொடுக்கப்பட்டுள்ள தகவல்களின் அடிப்படையில் கணிக்க இயலாது
[விடை : அ) முன்னோக்கு வினையில், ΔH > 0]
தீர்வு:
வெப்பநிலை குறையும்போது வினை பின்னோக்கி நடைபெறுவதால், அது வெப்ப உமிழ்வினை. எனவே முன்னோக்கு வினை வெப்பம் உமிழ் வினை (ΔH > 0)
24. கீழ்கண்ட வினைகளின் சமநிலை மாறிலிகள்:
N2 + 3H2 ⇌ 2NH3 ; K1
N2 + O2 ⇌ 2NO ; K2
H2 + ½ O2 ⇌ H2 O ; K3
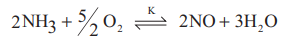
என்ற வினையின் சமநிலை மாறிலி மதிப்பு;
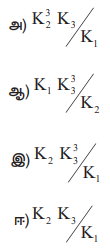
[விடை : இ) K2 K33 / K1]
தீர்வு:
2NH3 ⇌ N2 + 3H2; 1/K1
N2 + O2 ⇌ 2NO; K2
3H2 + 3/2 O2 ⇌ 3H2 O; K33
மூன்று சமநிலைகளையும் கூட்ட
2NH3 + 5/2 O2 ⇌ 2NO + 3H2 O
சமநிலைவினைகளை கூட்டும்போது அவற்றின் K மதிப்புகளை பெருக்கவேண்டும்
K = 1/K1 K2 K33
25. 400K வெப்பநிலையில் 20லிட்டர் கலனில் 0.4atm அழுத்தமுடைய CO2(g) மற்றும் அதிகளவு SrO உள்ளது (திண்ம SrO ன் கனஅளவை புறக்கணிக்க). கலனில் பொருத்தப்பட்டுள்ள உந்து தண்டினை தற்போது நகர்த்தி கலனின் கன அளவு குறைக்கப்படுகிறது. CO2 ன்அழுத்தமானது அதிகபட்ச அளவினை அடையும் போது, கலனின் அதிகபட்ச கனஅளவின் மதிப்பு யாது?
கொடுக்கப்பட்டவை:
SrCO3 (S) ⇌ SrO (S) + CO2 (g)
Kp = 1.6 atm (NEET 2017)
அ) 2 லிட்டர்
ஆ) 5 லிட்டர்
இ) 10 லிட்டர்
ஈ) 4 லிட்டர்
[விடை : ஆ) 5 லிட்டர்]
தீர்வு:
T2 = 400K V1 = 20லி
P1 = 0.4 atm
T2 = 400K V2 = ? P2 = PCO2 = Kp = 1.6 atm
P1 V1 = P2 V2
V2 = P1 V1 / P2 = 0.4 × 20 / 1.6 = 5 லிட்டர்