11 வது வேதியியல் : அலகு 8 : இயற் மற்றும் வேதிச்சமநிலை
திடப்பொருள் அல்லது வாயுக்கள் திரவத்தில் கரைவதால் ஏற்படும் சமநிலை திரவத்தில் திடப்பொருள்
திடப்பொருள் அல்லது வாயுக்கள் திரவத்தில் கரைவதால் ஏற்படும் சமநிலை திரவத்தில் திடப்பொருள்
ஒரு குறிப்பிட்ட வெப்பநிலையில் சர்க்கரையை நீரில் சேர்க்கும் போது அது கரைந்து சர்க்கரைக் கரைசலை உருவாக்குகிறது. இக்கரைசலுடன் அதிகளவு சர்க்கரையை தொடர்ந்து நீங்கள் சேர்க்கும் போது, ஒரு குறிப்பிட்ட நிலையில் சேர்க்கப்பட்ட சர்க்கரை கரையாமல் திட நிலைமையிலேயே இருக்கும் ஒரு நிலையை நீங்கள் அடைவீர்கள். மேலும் இதன் விளைவாக உருவான கரைசல் தெவிட்டிய கரைசல் (saturated solution) என்றழைக்கப்படுகிறது. இச்செயல் முறையிலும் திடமற்றும் கரைசல் நிலைமைகளில் காணப்படும் கரைப்பொருள் மூலக்கூறுகளுக்களுக்கிடையே இயங்குச்சமநிலை உருவாகிறது
சர்க்கரை (திண்மம்) ⇌ சர்க்கரை (கரைசல்)
இச் செயல்முறையில்,
{கரைபொருளின் கரைதல் வேகம்} = {கரைபொருளின் படிகமாதல் வேகம்}
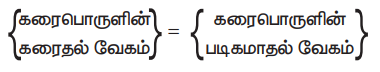
திரவத்தில் வாயு
கொடுக்கப்பட்ட அழுத்தத்தில், ஒரு வாயுவானது, ஒரு திரவத்தில் கரையும் போது, வாயு நிலைமையில் உள்ள வாயு மூலக்கூறுகளுக்கும், திரவத்தில் கரைந்துள்ள வாயு மூலக்கூறுகளுக்கும் இடையே சமநிலை காணப்படுகிறது.
எடுத்துக்காட்டு
கார்பன்-டை-ஆக்சைடு கரைந்துள்ள பானங்களில் பின்வரும் சமநிலை காணப்படுகிறது.
CO2(g) ⇌ CO2 (கரைசல்)
இத்தகைய வாயு - கரைசல் சமநிலையினை விளக்குவதற்கு ஹென்றியின் விதி பயன்படுத்தப்படுகிறது.