கணக்குகளுக்கான தீர்வுகள் - தன் மதிப்பீடு - வேதியியல்: இயற் மற்றும் வேதிச்சமநிலை | 11th Chemistry : UNIT 8 : Physical and Chemical Equilibrium
11 வது வேதியியல் : அலகு 8 : இயற் மற்றும் வேதிச்சமநிலை
தன் மதிப்பீடு - வேதியியல்: இயற் மற்றும் வேதிச்சமநிலை
தன்மதிப்பீடு
1. பின்வரும் வினையினைக் கருதுக.
Fe3+(aq) + SCN-(aq) ⇌ [Fe(SCN)]2+ (aq)
Fe3+ மற்றும் SCN- ஆகியன முறையே துவக்கத்தில் 1×10-3M மற்றும் 8×10-4M என்ற மோலார் செறிவுகளை பெற்றுள்ள ஒரு கரைசல் தயாரிக்கப்படுகிறது. சமநிலையில் [Fe(SCN)]2+ன் செறிவு 2×10-4M எனில், சமநிலை மாறிலியின் மதிப்பினைக் கண்டறிக.
தீர்வு :
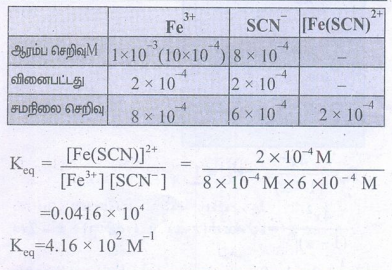
= 0.0416 × 104
K eq = 4.16 × 102 M-1
2. 1atm NO மற்றும் 1atm O2 ஐ தொடக்க செறிவுகளாகக் கொண்ட NOன் வளிமண்டல ஆக்சிஜனேற்ற வினை.
2NO(g) + O2(g) ⇌ 2NO2 (g)
ஆய்ந்தறியப்படுகிறது. சமநிலையில், ஆக்சிஜனின் பகுதி அழுத்தம் 0.52 atm எனில் இவ்வினைக்கான Kpன் மதிப்பைக் காண்க.
தீர்வு :
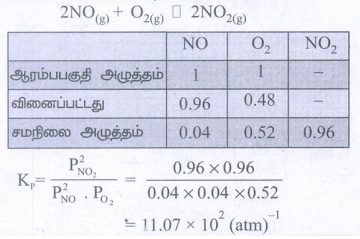
= 11.07 × 102 (atm)-1
தன் மதிப்பீடு
3. ஹைட்ரஜனை தொழில் முறையில் தயாரிக்க பின்வரும் நீர்வாயு மாற்ற வினை மிக முக்கியமானதாகும்.
CO(g) + H2O(g) ⇌ CO2(g) + H2(g)
கொடுக்கப்பட்ட வெப்பநிலையில் Kp = 2.7, 2L குடுவையில் 0.13மோல் CO, 0.56 மோல் நீர் 0.78 மோல் CO2 மற்றும் 0.28 மோல் H2 ஆகியன எடுத்துக்கொள்ளப்பட்டால், சமநிலையை அடைய வினை எந்த திசையில் நிகழும் எனக் கண்டறிக.
தீர்வு:
CO(g) + H2O(g) ⇌ CO2(g) + H2(g)
Kp = 2.7
[CO] = 0.13, [H2O] = 0.56
[CO2] = 0.78 , [H2] = 0.28
V = 2L
Kp = KC (RT)Δng Δng = 2 – 2 = 0
2. 7 = KC (RT)o
KC = 2. 7

Q = 3
Q > KC
எனவே வினை பின்னோக்கிய திசையில் நிகழும்.
தன்மதிப்பீடு
4) 423K வெப்பநிலையில், 1dm3 கலனில் 1 மோல் PCl5 எடுத்துக்கொள்ளப்பட்டு சமநிலை அடைய அனுமதிக்கப்படுகிறது. வினைக்கலவையின் சமநிலைச் செறிவுகளைக் காண்க. (PCl5 சிதைவடையும் வினைக்கு 423Kல் KC ன் மதிப்பு 2)
தீர்வு:
PCl5 ⇌ PCl3 + Cl2
கொடுக்கப்பட்டவை
[PCl5]ஆரம்பம் = 1 mol ; V = 1 dm3 ; KC = 2

2 – 2x = x2
x2 + 2x – 2 = 0
a x2 + bx + c = 0 என்ற இருபடி சமன்பாட்டின்
தீர்வுகள்
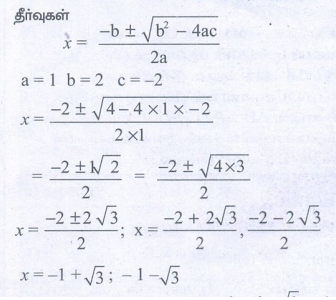
x நேர்குறி உடையது. அதனால் -1 - √3 சாத்தியமற்றது
எனவே x = -1 + 1.732 = 0.732
ஃ சமநிலை செறிவுகள்

தன் மதிப்பீடு
5. 298 K வெப்பநிலை மற்றும் 1 atm அழுத்தத்தில் பின்வரும் வினைக்கான சமநிலை மாறிலி 0.15
N2O4 (g) ⇌ 2NO2 (g)
வினை நிகழும் நிபந்தனை பின்வருமாறு மாற்றியமைக்கப்படுகிறது. வெப்பநிலை 100° C ஆக 1 atm அழுத்தத்தில் அதிகரிக்கப்படுகிறது. இந்நிலையில் சமநிலை மாறிலியின் மதிப்பு காண்.
தீர்வு:
N2O4 (g) ⇌ 2NO2 (g)
T1 = 298 K KP1 = 0.15
T2 = 100oC = 100 + 273 = 373K;
KP2 = ?

KP2 = 104.7 × 0.15
KP2 = 15.705