11 வது வேதியியல் : அலகு 7 : வெப்ப இயக்கவியல்
கலோரி மீட்டர் முறையினை பயன்படுத்தி ΔU மதிப்புகளை அளவிடல்
(அ) ΔU அளவிடுதல்
மாறாத கனஅளவில், வேதி வினைகளில், வெளிப்படும் வெப்பம் பாம் கலோரிமீட்டர் கொண்டு அளவிடப்படுகிறது.
பாம் கலோரிமீட்டரின் உள்கலன் (பாம்) மற்றும் மூடி ஆகியன வலிமையான எஃகினால் செய்யப்பட்டுள்ளது. உலோக மூடியானது, திருகாணிகள் மூலம் இறுக்கமாக பொருத்தப்பட்டுள்ளது.
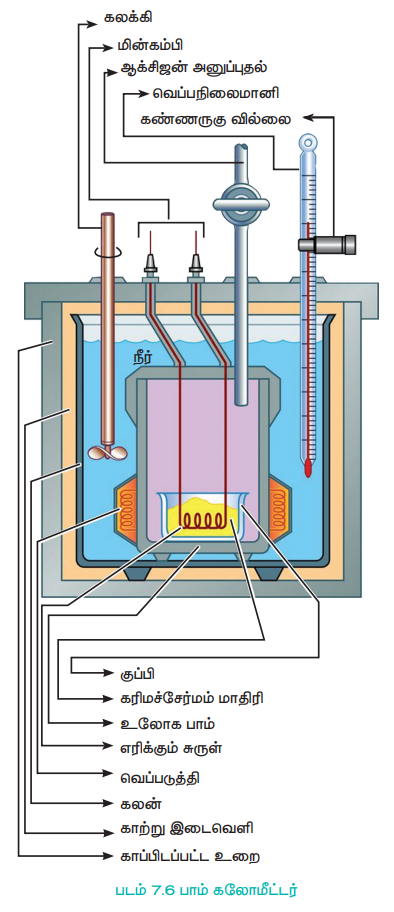
படம் 7.6 பாம் கலோமீட்டர்
எடையிடப்பட்ட (wகி) கரிம சேர்மமானது ஒரு பிளாட்டின தட்டில் எடுத்துக் கொள்ளப்படுகிறது. இத்தட்டானது மின்பாய்தல் மூலம் உடனடியாக எரிதலை தூண்டுவதற்காக மின்கம்பிகளுடன் பொருத்தப்பட்டுள்ளது உள் கலனில் அதிகளவு ஆக்ஸிஜன் செலுத்தி அழுத்தப்பட்டு இறுக்கமாக மூடப்படுகிறது. உள் கலன் (பாம்) ஆனது கலோரிமீட்டரினுள் உள்ள நீரில் அமிழ்த்தி வைக்கப்பட்டுள்ளது. வினையில் உருவாகும் வெப்பம் நீர் முழுவதும் சீராக பரவச் செய்ய கலோரிமீட்டரின் சுவர்களுக்கும், உள்கலனிற்கும் (பாம்) இடையே ஒரு கலக்கி உள்ளது. மின்வில்லை உருவாக்கி சேர்மம் எரிக்கப்படுகிறது.
கலோரி மீட்டரின் உள்கலனில் (பாம்), எடையிடப்பட்ட, எரியக்கூடிய கரிம சேர்மம், ஆக்ஸிஜன் சேர்த்து எரிக்கப்படுகிறது. சேர்மம் எரிக்கப்படும் போது உருவாகும் வெப்பம், கலோரி மீட்டர் மற்றும் அதைச் சூழ்ந்துள்ள நீரினால் உறிஞ்சப்படுகிறது. வெப்பநிலை மாற்றத்தை அளவிட பெக்மென் வெப்பநிலைமானி பொருத்தப்பட்டுள்ளது. பாம் கலோரி மீட்டர் மூடப்பட்டுள்ளதால், அதன் கனஅளவில் மாற்றம் ஏற்படுவதில்லை. எனவே வெப்ப அளவீடுகளானது மாறாத கனஅளவில் எரிதல் வெப்பத்திற்குச் (ΔUC0) சமம்.
இவ்வினையில் உருவான வெப்பத்தின் அளவானது (ΔUC0), கலோரி மீட்டர் மற்றும் நிரால் உறிஞ்சப்பட்ட வைப்ப மதிப்புகளின் கூடுதலுக்குச்சமம்.
கலோரி மீட்டரால் உறிஞ்சப்பட்ட வெப்பம்
q1 = k.ΔT
இங்கு k என்பது கலோரி மீட்டர் மாறிலி எனப்படுகிறது. மேலும் k = mC CC
mC = கலோரி மீட்டரின் நிறை
CC = கலோரி மீட்டரின் வெப்ப ஏற்புதிறன்
நீரால் உறிஞ்சப்பட்ட வெப்பம் q2 = mW CW ΔT
இங்கு mW என்பது நீரின் மோலார் நிறை,
CW நீரின் மோலார் வெப்ப ஏற்புத்திறன் (75.29 J K-1 mol-1)
எனவே ΔUc = q1 + q2
= k.ΔT + mw CW ΔT
= (k + mW CW) ΔT
ஒரு தெரிந்த அளவுடைய திட்ட பொருளை (பென்சாயிக் அமிலம்) எரிப்பதன் மூலம், கலோரி மீட்டர் மாறிலியின் (k) மதிப்பினை தீர்மானிக்க முடியும். பென்சாயிக் அமிலத்தின் எரிதல் வினை வெப்பம் - 3227 kJ mol-1 என்ற தெரிந்த ஒரு மதிப்பாகும்.
மாறா அழுத்தத்தில் என்தால்பி மாற்றத்தை சமன்பாடு (7.17)ஐ பயன்படுத்தி கணக்கிடலாம்.
ΔHC0(அழுத்தம்) = ΔUC0(கனஅளவு) + ΔngRT
பாம் கலோரி மீட்டரின் பயன்கள்:
1. எரிதல் வினைகளில் வெளிப்படும் வெப்பத்தை அளவிட பாம்கலோரி மீட்டர் பயன்படுகிறது.
2. உணவுப் பொருட்களின் கலோரி மதிப்பினை நிர்ணயித்திட இது பயன்படுகிறது.
3. வளர்சிதை மாற்ற ஆய்வுகள், உணவு பதப்படுத்துதல், வெடி பொருட்களை சோதித்தறிதல் போன்ற பல்வேறு தொழிற்துறைகளில் பாம்கலோரி மீட்டர் பயன்படுகிறது.