11 வது வேதியியல் : அலகு 7 : வெப்ப இயக்கவியல்
கணக்குகளுக்கான தீர்வுகள்: வெப்ப வேதிச்சமன்பாடுகள் (Thermochemical equations)
கணக்கு 7.2
C2H5OH (l) + 3O2 (g) → 2CO2 (g) + 3 H2O (l)
என்ற வினைக்கு திட்ட என்தால்பி மாற்ற மதிப்பை கணக்கிடுக. C2H5OH (l), CO2 (g) மற்றும் H2O (l) ஆகியவற்றின் திட்ட உருவாதல் என்தால்பி மதிப்புகள் முறையே 277, -393.5 மற்றும் -285.5 kJ mol-1 வரையறையின் படி O2(g) ன் திட்ட உருவாதல் என்தால்பி மதிப்பு பூஜ்ஜியமாகும்.
தீர்வு
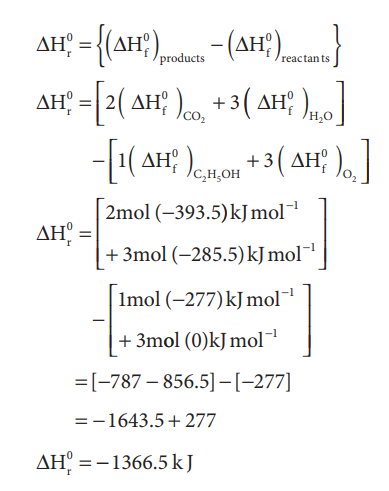
= [-787 - 856.5] - [-277]
= -1643.5 + 277
ΔHr0 = -1366.5 kJ
கணக்கு 7.3
128.0 கிராம் ஆக்ஸிஜனை 0°C லிருந்து 100°C க்கு வெப்பப்படுத்தும் போது ΔU மற்றும் ΔH மதிப்புகளை கணக்கிடுக. தோராயமாக CV மற்றும் CP மதிப்புகள் முறையே 21 J mol-1 K-1 மற்றும் 29 J mol-1 K-1 (வேறுபாடானது 8 J mo-1 K-1 இது தோராயமாக R மதிப்பிற்குச் சமம்)
தீர்வு
இங்கு
ΔU = n CV (T2 – T1)
ΔH = n CP (T2 – T1)
மேலும்
n = 128 / 32 = 4 மோல்கள்
T2 = 100°C = 373K ; T1 = 0°C = 273K
ΔU = n CV (T2 – T1)
ΔU = 4 × 21 × (373 - 273)
ΔU = 8400 J
ΔU = 8.4 kJ
ΔH = n CP (T2 – T1)
ΔH = 4 × 29 × (373 - 273)
ΔH = 11600 J
ΔH = 11.6 kJ