11 வது வேதியியல் : அலகு 7 : வெப்ப இயக்கவியல்
கணக்குகளுக்கான தீர்வுகள்: கிப்ஸ் கட்டிலா ஆற்றல் (G)
கிப்ஸ் கட்டிலா ஆற்றல் (G), திட்ட கட்டிலா ஆற்றல் மாற்றத்திற்கும் ΔG0, சமநிலை மாறிலிக்கும் K(eq) இடையே உள்ள தொடர்பு
கணக்கு 7.8
300K வெப்ப நிலையில், CO + (1/2) O2 → CO2 என்ற வினை தன்னிச்சையானது எனக்காட்டுக. CO2 மற்றும் CO ஆகியன உருவாவதற்கான திட்ட கட்டிலா ஆற்றல் மாற்றங்கள் முறையே -394.4 மற்றும் -137.2 kJ mole-1.
CO + (1/2) O2 → CO2
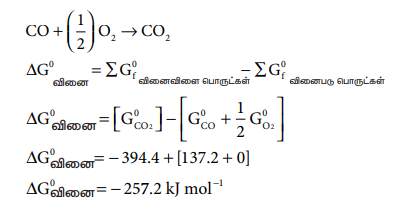
ΔG0வினை = - 394.4 + [137.2 + 0]
ΔG0வினை = - 257.2 kJ mol-1
கொடுக்கப்பட்ட வெப்பநிலையில் ΔG0வினை மதிப்பு எதிர்குறியை பெறுகிறது, எனவே வினை தன்னிச்சையாக நிகழும்.
கணக்கு 7.9
298 K வெப்பநிலையில் ஆக்ஸிஜனை ஓசோனாக மாறும் 3/2 O2 → O3 (g) வினைக்கு ΔG0 காண்க, திட்டஅழுத்த அலகுகளில் இவ்வினையின் Kp மதிப்பு 2.47 × 10-29
தீர்வு:
ΔG0 = - 2.303 RT log Kp
இங்கு
R = 8.314 JK-1 mol-1
Kp = 2.47 × 10-29
T = 298K
ΔG0 = -2.303 (8.314) (298) log (2.47 × 10-29)
ΔG0 = 163229 Jmol-1
ΔG0 = 163.229 KJ mol-1
11th Chemistry : UNIT 7 : Thermodynamics : Solved Example Problems: Gibbs free energy (G) in Tamil : 11th Standard
TN Tamil Medium School Samacheer Book Back Questions and answers, Important Question with Answer.
11 வது வேதியியல் : அலகு 7 : வெப்ப இயக்கவியல் : கணக்குகளுக்கான தீர்வுகள்: கிப்ஸ் கட்டிலா ஆற்றல் (G) - : 11 ஆம் வகுப்பு
தமிழ்நாடு பள்ளி சமசீர் புத்தகம் கேள்விகள் மற்றும் பதில்கள்.
11 வது வேதியியல் : அலகு 7 : வெப்ப இயக்கவியல்