12 ஆம் வகுப்பு விலங்கியல் : அத்தியாயம் 10 : உயிரி தொழில் நுட்பவியலின் பயன்பாடுகள்
மருத்துவத்தில் உயிரி தொழில் நுட்பவியலின் பயன்பாடுகள்
மருத்துவத்தில் உயிரி தொழில் நுட்பவியலின் பயன்பாடுகள் (Applications in medicine)
1. மறுசேர்க்கை மனித இன்சுலின் (Recombinant Human Insulin)
கணையத்திலுள்ள லாங்கர்ஹான் திட்டுகளில் காணப்படும் β செல்களிலிருந்து மனித இன்சுலின் உற்பத்தியாகிறது. இது 51 அமினோ அமிலங்களால் ஆனது. இவை 'A' மற்றும் 'B' என்னும் இரண்டு பாலிபெப்டைடு சங்கிலிகளாக அமைக்கப்பட்டுள்ளன. 'A' சங்கிலி 21 அமினோ அமிலங்களையும் 'B' சங்கிலி 30 அமினோ அமிலங்களையும் கொண்டுள்ளன. A மற்றும் B ஆகிய இரண்டு சங்கிலிகளும் டைசல்ஃபைடு பிணைப்புகள் மூலம் இணைக்கப்பட்டுள்ளன. இரத்தத்தில் சர்க்கரையின் அளவை இன்சுலின் கட்டுப்படுத்துகிறது. செல்கள் குளுகோஸை எடுத்துக் கொண்டு அதை ஆற்றலாக மாற்றி வெளியிடுவதற்கு இன்சுலின் உதவுகிறது. இன்சுலின் பற்றாக்குறையினால் 'டயாபடிஸ் மெலிடஸ்' எனும் சர்க்கரை நோய் உண்டாகிறது. சிகிச்சை அளிக்காவிடில் மரணத்தை ஏற்படுத்தக்கூடிய நோயான இது இரத்தத்தில் குளுக்கோஸின் அளவு அதிகரித்தல் மற்றும் சிக்கலான அறிகுறிகளையும் கொண்டு காணப்படுகிறது. தொடர்ச்சியான இன்சுலின் சார்பு சிகிச்சை மூலம் இப்பற்றாக்குறை நோயைச் சரி செய்யலாம்.
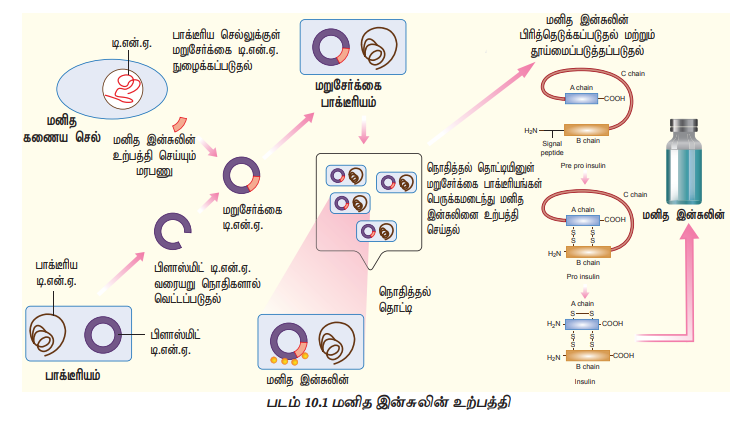
முற்காலத்தில், பன்றிகள் மற்றும் பசுக்களின் கணையங்களிலிருந்து பிரித்தெடுக்கப்பட்டு தூய்மைப்படுத்தப்பட்ட இன்சுலினை சர்க்கரை நோயாளிக்குச் செலுத்தி சிகிச்சையளிக்கப்பட்டது. விலங்கு இன்சுலினுக்கும் மனித இன்சுலினுக்கும் அமைப்பில் சிறிய அளவில் வேறுபாடுகள் உள்ளதால், சில நோயாளிகளில் இது ஒவ்வாமையை ஏற்படுத்தியது. 1970களின் பிற்பகுதியில் டி.என்.ஏ மறுசேர்க்கைத் தொழில் நுட்பத்தைப் பயன்படுத்தி இன்சுலின் உற்பத்தி செய்யப்பட்டது. இத்தொழில் நுட்பத்தில், மனித இன்சுலினுக்கான மரபணு, எ.கோலையின் பிளாஸ்மிட்டில் நுழைக்கப்படுகிறது. ஒருதலைமை வரிசையை (leader sequence) முன்புறம் கொண்டு அதைத் தொடர்ந்த 'A' மற்றும் ' துண்டங்கள் (சங்கிலிகள்) மற்றும் அவற்றை இணைக்கும் 'C' என்னும் மூன்றாவது சங்கிலி ஆகியவற்றால் ஆன முன்னோடி பாலிபெப்டைடு சங்கிலியாக முதன்மை - முன்னோடி இன்சுலின் (Pre-Pro Insulin) உருவாகிறது. மொழி பெயர்ப்புக்குப்பின் தலைமை வரிசையும் 'C' சங்கிலியும் வெட்டப்பட்டு நீக்கப்படுவதால், 'A' மற்றும் 'B' சங்கிலிகள் மட்டும் எஞ்சுகின்றன (படம் 10.1).
1921ல் பெஸ்ட் மற்றும் பேன்டிங் என்பவர்கள், நாயின் கணையத்திட்டுகளிலிருந்து பிரித்து எடுக்கப்பட்ட இன்சுலின் ஹார்மோனின், சர்க்கரை நோய் குணப்படுத்தும் திறனை விளக்கிக் காட்டினார்கள்.
டி.என்.ஏ மறுசேர்க்கைத் தொழில் நுட்பத்தால் உருவாக்கப்பட்டு மனிதனுள் செலுத்தப்பட்ட முதல் மருந்துப்பொருள் இன்சுலின் ஆகும். 1982ல் சர்க்கரை நோயைக் குணப்படுத்துவதற்காக இந்த இன்சுலினைப் பயன்படுத்த அனுமதியளிக்கப்பட்டது. 1986ல் 'ஹியுமுலின்' (Humulin) என்னும் வணிகப் பெயரோடு, சந்தையில் மனித இன்சுலின் விற்பனை செய்யப்பட்டது.
2. மனித ஆல்ஃபா லேக்டால்புமின் (Human or lactalbumin)
ஆல்ஃபா லேக்டால்புமின் என்பது 123 அமினோ அமிலங்களையும் 4 டைசல்ஃபைடு இணைப்புகளையும் 14178 டால்டன் மூலக்கூறு எடையையும் கொண்ட ஒரு புரதம் ஆகும். மனித தாய்ப்பாலிலுள்ள புரதங்களுள் 25% புரதம் ஆல்ஃபா லேக்டால்புமின் ஆகும். இது பால் சுரப்பிகளால் உற்பத்தி செய்யப்படுகிறது. லேக்டால்புமின் கால்சியம் மற்றும் துத்தநாக அயனிகளுடன் இணைந்து பாக்டீரியங்களைக் கொல்லும் பண்பையும் கட்டி எதிர்ப்புச் செயல்பாடுகளையும் கொண்டுள்ளது.
மறுசேர்க்கை செய்யப்பட்ட மனித ஆல்ஃபா லேக்டால்புமின் மரபணுவைக் கொண்டு பசுவின் மரபியல்பை மாற்றி அதன் விளைவாக பசும்பாலின் உணவு மதிப்பை அதிகரிக்கச் செய்ய முயற்சிக்கப்பட்டது. உடற்செல் உட்கரு மாற்றிப் பொருத்துதல் மூலம் நலமான, மரபியல்பு மாற்றப்பட்ட பசுக்கள் உருவாக்கப்பட்டன. அப்பசுவின் பாலில், ஒரு லிட்டருக்கு 1.55 கிராம் மறுசேர்க்கை ஆல்ஃபா லேக்டால்புமின் உற்பத்தி சாத்தியமானது. இதே போன்று மரபியல்பு மாற்றப்பட்ட வெள்ளாடுகள் உருவாக்கப்பட்டு, அவற்றின் பாலைப் பரிசோதித்ததில், அதில் ஒரு மில்லி லிட்டருக்கு 0.1 முதல் 0.9 மில்லி கிராம் மனித ஆல்ஃபா லேக்டால்புமின் இருப்பது கண்டறியப்பட்டது.
உடற்செல் உட்கரு மாற்றிப் பொருத்துதல் எனும் தொழில் நுட்பத்தில், ஒரு உடற்செல்லையும் ஒரு அண்ட செல்லையும் கொண்டு ஒரு உயிருள்ள கரு உருவாக்கப்படுகிறது. விலங்கு நகலாக்கம் எனும் பாடப்பகுதியில் இத்தொழில்நுட்பம் குறித்து விரிவாக விவரிக்கப்பட்டுள்ளது
உங்களுக்குத் தெரியுமா?
1997ல் முதன் முதலில் ரோஸி எனும் மரபியல்பு மாற்றப்பட்ட பசு உருவாக்கப்பட்டது. இப்பசுவின் பால், மனித லேக்டால்புமின் கொண்ட புரதச் செறிவு மிக்க பாலாகக் காணப்பட்டது. சாதாரண பசுவின் பாலை விட, புரதம் செறிந்த (2.4கிராம்/லிட்டர்) இப்பசும்பாலானது பச்சிளம் குழந்தைகளுக்கு ஏற்ற உணவூட்டம் மிக்க ஒரு சரிவிகித உணவாகும்.
3. இன்டர்ஃபெரான்கள்
பாலூட்டிகளின் செல்கள் வைரஸ்களால் பாதிக்கப்படும் போது, அச்செல்களால் உற்பத்தி செய்யப்படும் சிற்றினக்குறிப்பிடு தன்மையுடைய, புரதத்தாலான, வைரஸ் எதிர்ப்புப் பொருட்களே 'இன்டர்ஃபெரான்கள்' ஆகும். 1957ல் அலிக்ஐசக்ஸ் (AlickIsaacs) மற்றும் ஜீன்லின்ட்மேன் (Jean Lindemann) என்பவர்களால் இண்டர்ஃபெரான்கள் முதன் முதலில் கண்டுபிடிக்கப்பட்டன. அவற்றின் அமைப்பின் அடிப்படையில் இன்டர்ஃபெரான்கள் α, β மற்றும் Ƴ என வகைப்படுத்தப்பட்டுள்ளன. இவை, செல்லில் உள்ள டி.என்.ஏ வைத் தூண்டி, வைரஸ் எதிர்ப்பு நொதிகளைச் சுரக்கச் செய்து அதன்மூலம் வைரஸ்களின் பெருக்கத்தைத் தடுத்து செல்களைப் பாதுகாக்கின்றன. காரணி VIIIஐப் போன்றே இன்டர்ஃபெரான்களை இரத்தத்திலிருந்து பிரித்தெடுக்கலாம். ஆனால், இதற்கு மிக அதிக அளவில் இரத்தம் தேவைப்படுவதால் இது நடைமுறைச் சாத்தியம் இல்லை. இச்சிக்கலைக் கடப்பதற்கு, இன்டர்ஃபெரான்களை rDNA தொழில் நுட்பம் மூலம் உருவாக்குவது உகந்ததாகும். மறுசேர்க்கை இண்டர்ஃபெரான்கள் (recombinant interferons) உற்பத்திக்கு ‘எ.கோலை' யை விட 'சாக்கரோமைசெஸ் செரிவிசியே' என்னும் ஈஸ்ட் பொருத்தமானதாகும். ஏனெனில், புரதங்களைச் சர்க்கரையேற்றம் (Glycosylation) அடைய வைக்கத் தேவையான இயங்குதளம் 'எ.கோலை'யில் இல்லை. புற்றுநோய், எய்ட்ஸ், தண்டுவட மரப்பு நோய் (multiple sclerosis). கல்லீரல் அழற்சி (hepatitis-c), அக்கிப்புடை (herpes zoster) போன்ற பல்வேறு நோய்களுக்கான சிகிச்சையில் இன்டர்ஃபெரான்கள் பெரிதும் பயன்படுகின்றன. இவ்விதம், பல சிகிச்சைப் பயன்பாடுகளை இவை கொண்டிருந்தாலும் அவற்றின் அதீதமான உற்பத்திச் செலவு காரணமாக, சாதாரண மனிதனுக்கு இன்னும் எட்டாக்கனியாகவே இன்டர்ஃபெரான்கள் விளங்குகின்றன.
4. மறுசேர்க்கைத் தடுப்பூசிகள்/ தடுப்பு மருந்துகள் (Recombinant vaccines)
புதிய தலைமுறைத் தடுப்பூசிகளை உருவாக்க டி.என்.ஏ மறுசேர்க்கைத் தொழில் நுட்பம் பயன்படுகிறது. இம்முறையின் மூலம், பாரம்பரியத் தடுப்பூசி உற்பத்தி முறைகளிலிருந்த வரம்புகளைக் கடக்க இயலும்.
வழக்கமான நடைமுறைகளில் உற்பத்தி செய்யப்படும் தடுப்பூசிகளுடன் ஒப்பிடும்போது, மறுசேர்க்கைத் தடுப்பூசிகள் சீரான தரத்துடன் குறைவான பக்கவிளைவுகளைக் கொண்டுள்ளன. மறுசேர்க்கைத் தடுப்பூசிகளின் பல்வேறு வகைகளாவன:
i) துணை அலகு தடுப்பூசிகள்
ii) வலு குறைக்கப்பட்ட மறுசேர்க்கைத் தடுப்பூசிகள்
iii) டி.என்.ஏ தடுப்பூசிகள்
துணை அலகு தடுப்பூசிகள் (Subunit vaccines)
நோயுண்டாக்கும் உயிரியை, முழு உயிரியாகப் பயன்படுத்தாமல், அவ்வுயிரியின் பகுதிகளை மட்டும் பயன்படுத்தித் தயாரிக்கப்படும் தடுப்பூசிகளுக்கு 'துணை அலகு தடுப்பூசிகள்' என்று பெயர். புதிய வகை துணை அலகு தடுப்பூசிகள் தயாரிக்க டி.என்.ஏ மறுசேர்க்கைத் தொழில் நுட்பம் ஏற்றதாகும். இம்முறையில், நோயுண்டாக்கும் உயிரியிலுள்ள புரதங்கள், பெப்டைடுகள் மற்றும் அவற்றின் டி.என்.ஏக்கள் ஆகிய கூறுகள் பயன்படுத்தப்படுகின்றன. தயாரிப்பில் தூய்மை, நிலைப்புத்தன்மை மற்றும் பாதுகாப்பான பயன்பாடு ஆகியவை இவ்வகைத் தடுப்பூசிகளின் நன்மைகளாகும்.
மரபுப்பொறியியல் என்னும் அறிவியற்புலத்தைப் பயன்படுத்தி 'மூலக்கூறு மருந்தாக்கம்' என்னும் முறை மூலம் வாய்வழி தடுப்பு மருந்துகள் தயாரிக்கப்படுகின்றன. தேர்ந்தெடுக்கப்பட்ட மரபணுக்கள் தாவரங்களுக்குள் புகுத்தப்பட்டு மரபியல்பு மாற்றப்படுவதால், அம்மரபணுக்களுக்குரிய புரதம் உற்பத்தியாகிறது. உண்ணத்தகுந்த தடுப்பு மருந்துகள் கோழைப்படலத்தை இலக்காகக் கொண்டவை. இவை, உடல் பகுதி மற்றும் கோழைப்படலம் சார்ந்த தடைகாப்பு வினைகளைத் தூண்டுகின்றன. தற்பொழுது, மனித மற்றும் விலங்கு நோய்களான, மணல்வாரி, காலரா, கால் மற்றும் வாய் நோய் மற்றும் கல்லீரல் அழற்சி போன்றவற்றிற்கான உண்ணத்தகுந்த தடுப்பு மருந்துகள் உற்பத்தி செய்யப்பட்டுள்ளன.
வலு குறைக்கப்பட்ட மறுசேர்க்கைத் தடுப்பூசிகள் (Attenuated recombinant vaccines)
மரபியல்பு மாற்றப்பட்ட நோயுண்டாக்கி உயிரிகளில் (பாக்டீரியா அல்லது வைரஸ்) அவற்றின் நோயுண்டாக்கும் தன்மை நீக்கப்பட்டு தடுப்பூசிகளாகப் பயன்படுத்தப்படுகின்றன. பாக்டீரியா அல்லது வைரஸ்களை மரபுப் பொறியியல் மாற்றம் மூலம் உயிருள்ள தடுப்பூசிகளாகப் (live vaccines) பயன்படுத்தலாம். இத்தகைய தடுப்பூசிகள் 'வலு குறைக்கப்பட்ட மறுசேர்க்கைத் தடுப்பூசிகள்' எனப்படும்.
டி.என்.ஏ தடுப்பூசிகள் (DNA vaccines)
டி.என்.ஏ தடுப்பூசிகளை மரபியல் நோய்த்தடுப்பு முறையாகப் பயன்படுத்தும் ஒரு புதிய அணுகுமுறை 1990ல் நடைமுறைக்கு வந்தது. டி.என்.ஏ மூலக்கூறுகள் மூலம் உடலில் தடைகாப்பு வினைகள் தூண்டப்படுகின்றன. ‘எதிர்ப்பொருள் தூண்டி புரதத்திற்கு’ (antigenic protein) குறியீடு செய்யும் ஒரு மரபணுவை டி.என்.ஏ தடுப்பூசி கொண்டுள்ளது. இந்த மரபணுவை பிளாஸ்மிட்டுக்குள் செலுத்தி, பின்னர் ஒரு இலக்கு விலங்கின் உடல் செல்களுக்குள் ஒன்றிணையச் செய்யப்படுகிறது. உள்ளே சென்ற அந்த டி.என்.ஏ, எதிர்ப்பொருள் தூண்டி மூலக்கூறுகளை உருவாக்க செல்களுக்கு உத்தரவிடுகிறது. அவ்விதம் உருவாக்கப்பட்ட மூலக்கூறுகள் செல்களுக்கு வெளியே காணப்படுகின்றன. செல்களால் உருவாக்கப்பட்டு, சுதந்திரமான மிதந்து கொண்டிருக்கும் இம்மூலக்கூறைக் காணும் நமது தடைகாப்பு, தனது வலுவான எதிர்ப்பை, எதிர்ப்பொருள் உருவாக்கத்தின் மூலம் தெரிவிக்கிறது. டி.என்.ஏ தடுப்பூசியால் நோயை உருவாக்க இயலாது. ஏனெனில், இது நோயுண்டாக்கும் மரபணுவின் ஒரு பகுதி நகல்களையே கொண்டுள்ளது. வடிவமைக்கவும் மலிவாக உற்பத்தி செய்வதற்கும் டி.என்.ஏ தடுப்பூசிகள் எளிதானவை.
1997ல் முதன் முதலில் உருவாக்கப்பட்ட செயற்கைத் தடுப்பூசி, ஹெப்படைடிஸ் B (HbsAg) நோய்க்கு எதிரான மறுசேர்க்கைத் தடுப்பூசி ஆகும். இது, ரிகாம்பிவேக்ஸ் (Recombivax) மற்றும் என்ஜெரிக்ஸ் B (Engerix B) என்னும் வணிகப் பெயர்களில் விற்பனையாகிறது. அமெரிக்கா, ஃப்ரான்ஸ் மற்றும் பெல்ஜியம் நாடுகளுக்கு அடுத்தபடியாக, ஹெப்படைடிஸ் B தடுப்பூசியைச் சொந்தமாகத் தயாரித்த நான்காவது நாடு இந்தியா ஆகும்.
இவ்வாறு புதிய தொழில் நுட்ப முறைகளின் மூலம் உருவாக்கப்படும் தடுப்பூசிகள் உறுதியான பல நன்மைகளைக் கொண்டுள்ளன. அவையாவன: இலக்கு புரத உற்பத்தி, நீண்டு நிலைக்கும் நோய்த்தடைகாப்பு மற்றும் குறிப்பிட்ட நோயுண்டாக்கிகளுக்கு எதிரான தடைகாப்பு வினைகளை குறைந்த நச்சு விளைவுகளுடன் விரைவாகத் தூண்டுதல் ஆகியன.
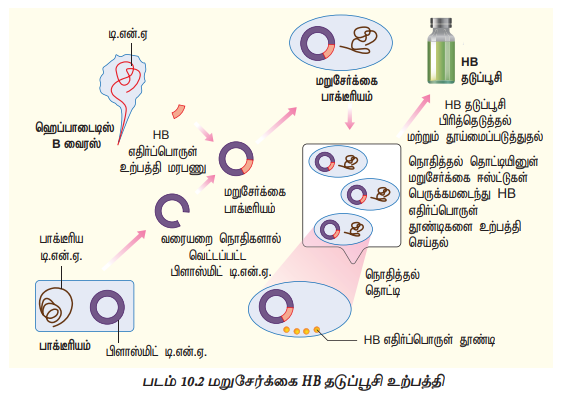
சாக்கரோமைசெஸ் செரிவிசியே எனும் ஈஸ்ட்டில், ஹெப்படைடிஸ் B புறபரப்பு எதிர்பொருள் தூண்டிக்கான (HbsAg) மரபணுவை நகலாக்கம் செய்து, துணை அலகு தடுப்பூசியாக மறுசேர்க்கை ஹெபாடைடிஸ் B தடுப்பூசி உற்பத்தி செய்யப்படுகிறது (படம் 10.2).