அணு அமைப்பு | முதல் பருவம் அலகு 4 | 7 ஆம் வகுப்பு அறிவியல் - அணு எண் மற்றும் நிறை எண் | 7th Science : Term 1 Unit 4 : Atomic Structure
7 ஆம் வகுப்பு அறிவியல் : முதல் பருவம் அலகு 4 : அணு அமைப்பு
அணு எண் மற்றும் நிறை எண்
அணு எண் மற்றும் நிறை எண்
அனைத்துத் தனிமங்களும் ஒரே மாதிரியான எலக்ட்ரான்கள், புரோட்டான்கள் மற்றும் நியூட்ரான்களால் ஆனவை எனில், எவ்வாறு ஓரு கார்பன் கார்பன் அணு, ஓர் இரும்பு அணுவிலிருந்து மாறுபடுகிறது? தொடர்ந்து நிகழ்ந்த ஆய்வுகளின் மூலம் ஓர் அணுவின் உட்கருவினுள் உள்ள புரோட்டான்களே அந்தத் தனிமம் எத்தகையது என்பதை நிர்ணயம் செய்கிறது என்று அறிந்தனர். எடுத்துக்காட்டாக, ஒரு அணுவின் உட்கருவினுள் ஒரே ஒரு புரோட்டான் இருந்தால் அத்தகைய அணு ஹைட்ரஜன் அணுவாகும். ஒரு அணுவின் உட்கருவினுள் எட்டு புரோட்டான்கள் இருந்தால் அது ஆக்சிஜன் அணுவாகும்.
அணு எண் (z)
ஒரு அணுவில் காணப்படும் எலக்ட்ரான்கள் அல்லது புரோட்டான்களின் மொத்த எண்ணிக்கையே அந்த அணுவின் அணு எண் ஆகும். இது Z என்ற எழுத்தால் குறிக்கப்படுகிறது. ஓர் அணுவின் அணு எண் தெரியுமானால் அவ்வணுவில் காணப்படும் எலக்ட்ரான்கள் அல்லது புரோட்டான்களின் எண்ணிக்கையை நம்மால் கண்டறிய இயலும்.
கீழே கொடுக்கப்பட்டிருக்கும் படங்களை உற்றுநோக்கவும். ஹைட்ரஜன் அணுக்கருவானது ஒரே ஒரு புரோட்டானைக் கொண்டுள்ளது. அணுக்கருவிற்கு வெளியே ஒரு எலக்ட்ரான் மட்டுமே சுற்றி வருகிறது. எனவே ஹைட்ரஜனின் அணு எண் (Z) 1 ஆகும்.
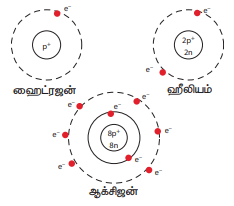
ஹீலியம் அணுவானது அதன் அணுக்கருவினுள் இரண்டு புரோட்டான்களையும் அணுக்கருவிற்கு வெளியே இரண்டு எலக்ட்ரான்களையும் கொண்டுள்ளது. எனவே, அதன் அணு எண் (Z) 2 ஆகும்.
படத்தில் கொடுக்கப்பட்ட ஆக்சிஜனின் அணு அமைப்பினைக் காணவும். அதன் அணு எண் யாது?
முயற்சி செய்க
கார்பனின் அணு எண் (Z) 6 எனில் அந்த அணுவானது அதன் சுற்றுப் பாதையில் எத்தனை எலக்ட்ரான்களைக் கொண்டுள்ளது?
நிறை எண் (A) அல்லது அணுநிறை
ஒரு அணுவின் மொத்த நிறையும் அதன் அணுக்கருவினுள் காணப்படுகிறது என்று நாம் படித்தோம். இதிலிருந்து, நாம் நிறை எண்ணைப் பெற முடியும். நிறை எண் என்பது அணுக்கருவினுள் உள்ள மொத்த புரோட்டான்கள் மற்றும் நியூட்ரான்களின் எண்ணிக்கையின் கூடுதலுக்குச் சமமாகும்.
நிறை எண் அல்லது அணுநிறை = புரோட்டான்களின் எண்ணிக்கை + நியூட்ரான்களின் எண்ணிக்கை
A = p + n
ஒரு லித்தியம் அணுவானது 3 புரோட்டான்களையும், 4 நியூட்ரான்களையும் கொண்டுள்ளது. எனவே, அதன் நிறை எண் (A) = 3 + 4 = 7. ஒரு சோடியம் அணுவானது 11 புரோட்டான்களையும் 12 நியூட்ரான்களையும் கொண்டுள்ளது. எனவே அதன் நிறை எண் (A) = 11 + 12 = 23.
ஒரு தனிமத்தின் குறியீட்டை எழுதும்போது, அவற்றின் அணு எண் மற்றும் நிறை எண்ணும் எழுதப்படுகின்றன. உதாரணமாக, ஹைட்ரஜன், கார்பன் மற்றும் ஆக்சிஜனின் குறியீடுகள் 1H1, 6C12, 8O16 என்று எழுதப்படுகின்றன. தனிம ஆவர்த்தன அட்டவணையில் உள்ள தனிமங்கள் அனைத்துமே கீழ்க்காணும் எலக்ட்ரான்கள், புரோட்டான்கள் மற்றும் நியூட்ரான்களின் சேர்க்கையைக் கொண்டுள்ளன.
ஐசோடோப்புகள்
ஒரே தனிமத்தின் அணுக்கள் வெவ்வேறு எண்ணிக்கையுள்ள நியூட்ரான்களைப் பெற்றிருக்கலாம். அத்தகைய அணுக்கள் ஒரே அணு எண்ணையும் வெவ்வேறு நிறை எண்களையும் பெற்றுள்ளன. அவை ஐசோடோப்புகள் என அழைக்கப்படுகின்றன. உதாரணமாக ஹைட்ரஜன் அணுவானது மூன்று ஐசோடோப்புகளைப் பெற்றுள்ளது. அவை: புரோட்டியம் (1H1), டியூட்ரியம் (1H2), டிரிட்டியம் ( 1H3).
ஐசோபார்கள்
ஒரே நிறை எண்ணையும் வெவ்வேறு அணு எண்களையும் கொண்ட அணுக்கள் ஐசோபார்கள் எனப்படுகின்றன. எ.கா. கால்சியம்(20Ca40) மற்றும் ஆர்கான் - (18Ar40).
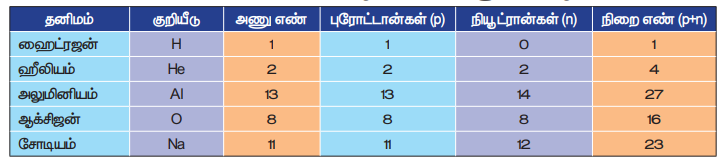
அட்டவனை 4.2 தனிமங்களின் குறியீடுகள் மற்றும் அவற்றின் அணு எண் மற்றும் நிறை எண்.
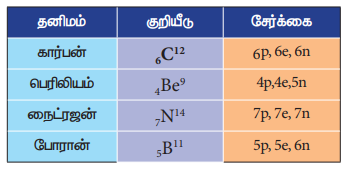
அட்டவணை 4.3 தனிமங்களின் குறியீடுகள்
முயற்சி செய்க
1. அனைத்து அணுக்களின் அணு எண் மற்றும் நிறை எண் ஆகியவை எப்போதும் முழு எண்ணாகவே இருப்பது ஏன்?
2. ஒரு சல்பர் அணுவானது 16 புரோட்டான்களையும், 16 நியூட்ரான்களையும் கொண்டுள்ளது. அதன் அணு எண் மற்றும் நிறை எண்ணின் மதிப்பினைக் காண்க.
செயல்பாடு 3

மேலே கொடுக்கப்பட்டுள்ள அட்டவணையினை உற்றுநோக்கி பின்வரும் வினாக்களுக்கு விடையளிக்கவும்.
1. நான் சுவாசித்தலுக்குப் பயன்படுகிறேன். நான் இல்லாமல் உங்களால் உயிர் வாழ முடியாது. எனது பெயரையும், குறியீட்டையும் எழுதுக. ஆக்சிஜன், O.
2. இது பலூன்களை நிரப்பப் பயன்படுகிறது. இது ஒரு வாயுவாகும். இதனை அடையாளம் காண்க. இதன் நிறை எண் என்ன?ஹட்ரஜன். (A=l).
3. வாழைப்பழத்தில் உள்ள தனிமத்தின் பெயரைக் குறிப்பிடுக. அதன் அணு எண் யாது? பொட்டாசியம் (Z = 19)
4. நான் பட்டாசுகளில் காணப்படுகிறேன். நான் எத்தனை புரோட்டான்களைக் கொண்டுள்ளேன்? சல்பர் (p = 16)
5. நான் உயர்ந்த மதிப்புமிக்க தனிமம். நான் யாரென்று கண்டுபிடி. என்னுடைய நிறை எண்ணைக் கூற முடியுமா?