வகைப்பாடு, - புரதங்கள் - உயிரி மூலக்கூறுகள் | 11th Botany : Chapter 8 : Biomolecules
11 வது தாவரவியல் : அலகு 8 : உயிரி மூலக்கூறுகள்
புரதங்கள் - உயிரி மூலக்கூறுகள்
புரதங்கள்
அனைத்துப் பெருமூலக் கூறுகளிலும் அதிகப் பல்வகைமை பெற்ற மூலக்கூறுகள் புரதங்களாகும். ஒரு செல்லின் உலர் எடையில், 2/3 பங்கு புரதங்களாக உள்ளன. ‘புரோட்டீன்' என்ற சொல்லை முன்வைத்தவர் ஜெரார்டஸ், ஜோஹானஸ் முல்டர் ஆவார். முதல் இடம் எனப் பொருள் பெற்ற 'புரோட்டியோஸ்' என்ற கிரேக்கச் சொல்லில் இருந்து புரதம் என்ற சொல் உருவாகியது.
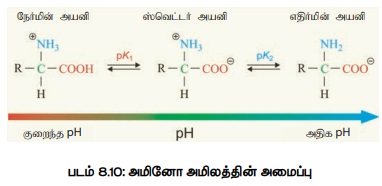
ஒவ்வொரு அமினோ அமிலமும், கார அல்லது அமிலத் தன்மை அல்லது இரண்டையும் பெற்ற அமிலமாக உள்ளது. ஊடகத்தின் pH (ஹைட்ரஜன் அயனிச்செறிவிற்கேற்ப)-ற்கு ஏற்ப அமினோ அமிலம் ஒன்று கார நிலையிலோ, அல்லது அமில நிலையிலோ காணப்படும். ஆகையால் இவை ஆம்போடெரிக் என்று அழைக்கப்படுகிறது. ஒரு குறிப்பிட்ட pH அளவில் கார மற்றும் அமிலத் தன்மை இரண்டையும் வெளிப்படுத்துகிறது. இந்த நிலையில் அது இரு துருவ நிலைபெற்ற ஸ்விட்டர் அயனி என அழைக்கப்படுகிறது. ஸ்விட்டர் அயனி இரண்டு அல்லது மேற்பட்ட செயலாக்கத் தொகுதிகள் கொண்டிருக்கும். இவற்றில் ஒன்று நேர்மின் அயனி, மற்றொன்று எதிர்மின் அயனியாக இருக்கும். இதன் நிகர மின்னூட்டம் பூஜ்யமாகும். இந்த நிலையை அமினோ அமிலத்திற்கு உண்டாக்க உதவும் குறிப்பிட்ட pH நிலைக்கு ஒத்த மின்னிய புள்ளி என்று பெயர் (படம் 8.10).
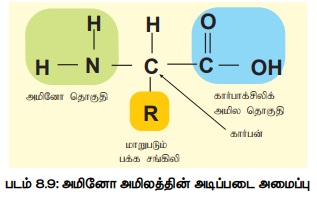
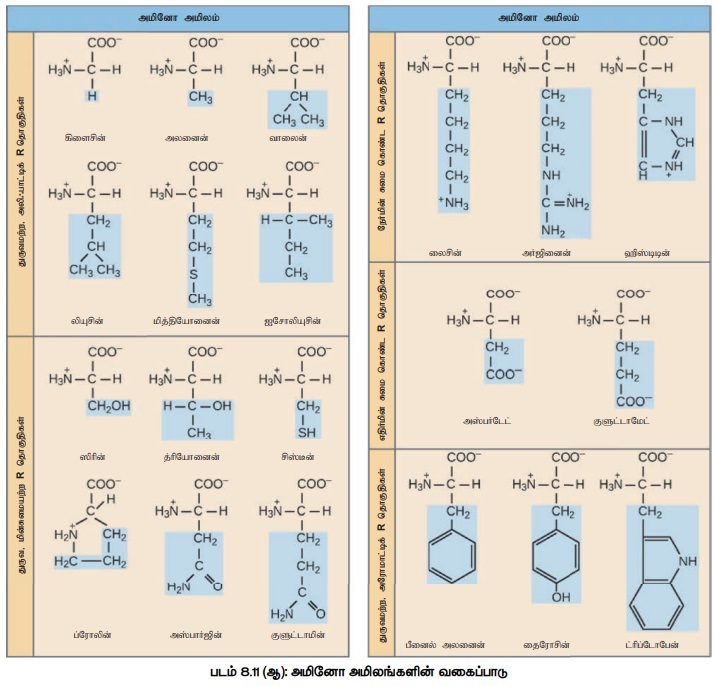
1. அமினோ அமிலங்களின் வகைப்பாடு
காணப்படும் R தொகுப்பின் தன்மைக்கு ஏற்ப இவை அமில,
கார, துருவ, துருவமற்ற வகைகள் என வகைப்படுத்தப்பட்டுள்ளன.
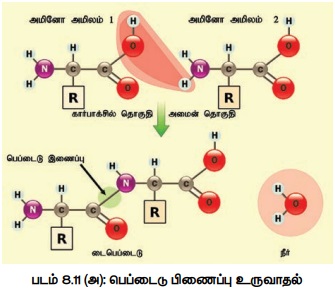
இரு அமினோ அமிலங்கள் வினைபுரிந்து ஒரு மூலக்கூறு நீரை
வெளியேற்றிப் பிணையுறும் செயலுக்குப் பெப்டைடு பிணைப்பு என்று பெயர். இப்பிணைப்பின்
போது ஒரு அமினோ அமிலத்தின் அமினோ தொகுப்பு மற்றொன்றின் கார்பாக்ஸில் தொகுப்புடன் வினைபுரிந்து
நீர் வெளியேற்றப்பட்டு டைபெப்டைடு உருவாகிறது. பல அமினோ அமிலங்கள்
இந்தப் பெப்டைடு பிணைப்பை ஏற்படுத்தும்போது, மணிகோர்த்தது போல் அமைந்த நீள் திரள் உருவாகிறது.
இந்த இழைக்குப் பாலிபெப்டைடு என்று பெயர். 1953-ஆம் ஆண்டு ஃப்ரெட் சாங்கர் என்பவர் இன்சுலின்
என்ற புரதத்தை முதன் முதலில் வரிசைப்படுத்தினார். (8.11 அ,ஆ).
உங்களுக்குத் தெரியுமா?
ஃப்ரெட்
சாங்கர் என்பவர் இன்சுலின்
என்ற புரதத்தை முதன் முதலில் வரிசைப்படுத்தினார்.

லைனஸ் ஃபாலிங் மற்றும் ராபர்ட் கோரி 1951-ம் ஆண்டு புரதத்தின் இரண்டாம் நிலை அமைப்பான
திருகுச்சுழல் (α -helix) மற்றும் தகடு (β-sheet) அமைப்பை முன்மொழிந்தனர். அதற்காக அவர்களுக்கு
நோபல் பரிசு 1954-ம் ஆண்டு வழங்கப்பட்டது.

2. புரதத்தின் அமைப்பு
புரதச் சேர்க்கையின் போது ரைபோசோம்களில் பல அமினோ அமிலங்கள்
அவற்றிற்குரிய வரிசையில் அமைக்கப்பட்டுப் பெப்டைடு இணைப்புகள் மூலம் நிலை நிறுத்தப்படுகின்றன.
இவ்வாறு பாலிபெப்டைடு சங்கிலி ஒன்று உருவான பின்னர், சிறப்பாகச் செயல்படுவதற்கு ஏற்ப
முப்பரிமாண அமைப்பை அடைவதற்காக உருமாற்றம் அடைந்து குறிப்பிட்ட புரதம் உருவாகிறது.
மடிப்புறும் தன்மைக்கு ஏற்பத் தோன்றும் புரதங்கள் முதல் நிலை, இரண்டாம் நிலை, மூன்றாம்
நிலை மற்றும் நான்காம் நிலை அமைப்பு என நான்கு வகைகளாக அறியப்படுகிறது (படம்
8.12).
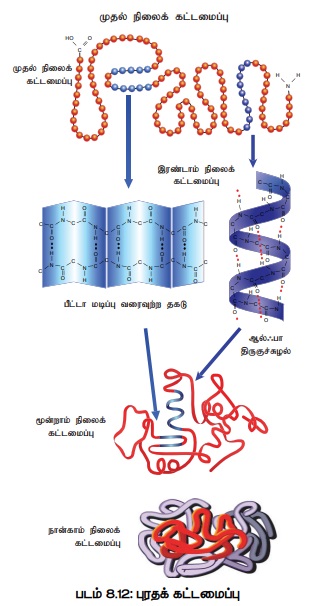
• பல அமினோ அமிலங்கள் பாலிபெப்டைடு சங்கிலியில் அடுத்தடுத்து நீள் வரிசையில் சேர்க்கப்பட்டுள்ள நிலை, முதல் நிலை (Primary structure) அமைப்பாகும்.
• இரண்டாம் நிலை (Secondary structure) அமைப்பு, வினைத் தொகுதிகள் வெளிப்பரப்பில் வெளியாகி ஹைட்ரஜன் பிணைப்புகள் மூலம் மூலக்கூறு இடைச்செயல் புரிவதால் தோன்றுகிறது. இதனால் பாலிபெப்டைடு சங்கிலி மடிப்புறுகிறது. இதனால் திருகுச் சுருள் கொண்டα சுருள் அமைப்பு அல்லது β மடிப்பு வரைவுற்ற தகடு என்ற இரண்டாம் நிலை அமைப்புகள் உருவாகின்றன.
• மூன்றாம் புரத நிலை (Tertiary protein structure) என்பது இரண்டாம் நிலையிலுள்ள புரதம் மேலும் சுருண்டு மேலாண்மையான கோள உருவம் அடைந்து உருவாகும் அமைப்பு ஆகும். இதனைக் களம் என்று அழைப்பர்.
• நான்காம்
புரத நிலை (Quaternary protein
structure) அமைப்பு , ஒன்றிற்கு மேற்பட்ட பாலிபெப்டைடு சங்கிலிகள் கொண்ட சிக்கலான
புரதங்களில் காணப்படுகிறது. இதனால் ஒரு பெரிய பல அடுக்கு புரதம் உருவாகிறது. இதில்
உள்ள பாலிபெப்டைடு சங்கிலிகள் தனியே துணை அலகுகள்
(sub units) எனப்படுகின்றன. இத்தகைய செயல்படும்
புரதம் பல அடுக்கு எனப்படும்.
எடுத்துக்காட்டு: நொதிகள் வினையூக்கிகளாகச் செயல்படுவதால்
இவை குறிப்புச் சார்பு அற்ற செயல் புரதங்களாகும் - உயிர் எதிர் பொருட்கள் பல்வேறு உயிரினங்களுக்குக்குறிப்பு
சார்பு பெற்றுச் சிக்கலான கிளைக்கோபுரதங்களாக உள்ளன.
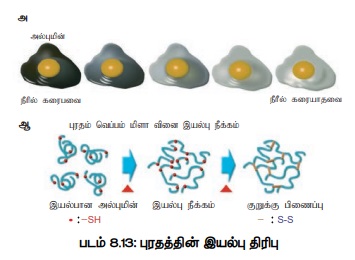
3. புரதத்தின் இயல் திரிபு
புரதத்தின் இயல் திரிபு என்பது அதன் முப்பரிமாண வடிவத்தை
இழப்பதாகும். புரதத்தை வெப்பத்துக்குள்ளாகும் போது அதன் அணுக்கள் வேகமாக அதிர்வுக்குள்ளாகி
ஹைட்ரஜன் பிணைப்புகள் மற்றும் அயனிப்பிணைப்புகள் துண்டிக்கப்படுவதால் இது நேரிடுகிறது.
இந்தச் சூழ்நிலையில் புரத மூலக்கூறுகள் நீட்சி அடைந்து அமைப்பு உருக்குலைந்த இழைகளாகின்றன.
சோப்பு, சலவைப்பொருட்கள், அமிலம், ஆல்கஹால், சில நுண்ணுணியிர் நீக்கிகள் ஆகியவை இழைக்களுக்கிடையேயான
பிணைப்புகளைக் குலைத்து மூலக்கூறைச் செயலிழக்கச் செய்கின்றன (படம் 8.13).

வெப்பப்படுத்தும் போது புரதங்கள் சகபிணைப்பற்ற
பிணைப்புகளாகத் திரிதலடைகின்றன. இச்செயல்பாடு புரதத்தின் இயல் திரிபு என்பதைக் கிரிஸ்டியன்
ஆன்பின்சன் என்பவர் விளக்கினார்.
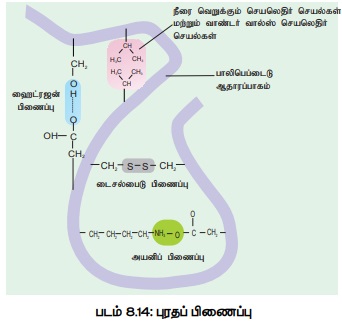
4. புரதத்தில் காணப்படும் பிணைப்புகள்
நான்கு விதமான வேதிப்பிணைப்புகள் புரதங்களில் உள்ளன (படம்: 8.14).
ஹைட்ரஜன் பிணைப்பு :
பாலிபெப்டைடு சங்கிலியில் உள்ள சில ஹைட்ரஜன் அணுக்களுக்கும், ஆக்ஸிஜன் அல்லது நைட்ரஜன் அணுக்களுக்குகிடையே தோன்றுகிறது. ஹைட்ரஜன் அணுக்கள் குறைந்த நேர்மின் தன்மையும், ஆக்ஸிஜன் மற்றும் நைட்ரஜன் அணுக்கள் குறைந்த எதிர்மின் தன்மையும் உடையவை. எதிரெதிர் மின் தன்மையால் ஈர்ப்பு உண்டாகி ஹைட்ரஜன் பிணைப்பு ஏற்படுகிறது.
இப்பிணைப்புகள் வலுவற்றவையாக இருந்தாலும் பெரும் எண்ணிக்கையில்
மூலக்கூறின் முப்பரிமாண வடிவத்தை நிலைப்படுத்துகின்றன (படம் 8.14).
அயனிப்பிணைப்பு:
பெப்டைடு பிணைப்பால் இணையாத மின் தன்மை கொண்ட தொகுப்புகளுக்கிடையே இது உருவாகிறது. ஹைட்ரஜன் பிணைப்பை விட இது வலுவானது . pH மாற்றங்கள் மற்றும் வெப்பநிலை மாற்றங்களால் துண்டிக்கப்படும் பிணைப்பு இதுவாகும்.
டைசல்ஃபைடு பிணைப்பு :
சிஸ்டீன், மீத்தியோனைன் போன்ற அமினோ அமிலங்கள் சல்ஃபர் கொண்டவை. இவை சல்ஃபர் அணுக்களுக்கும் அமினோ அமிலங்களுக்கும் இடையே இரட்டைச் சல்ஃபர் இணைப்பு பாலத்தினை அமைக்கின்றன.
நீர் வெறுக்கும் பிணைப்பு:
இந்தப் பிணைப்பு புரதத்தின் அமைப்பைத் தக்கவைக்க உதவுகிறது. கோளப் புரதங்கள் கரைசல் ஒன்றில் வைக்கப்படும் போது அவற்றின் நீர்வெறுக்கும் தொகுப்புகள் நீர் மூலக்கூறுகளை வெறுத்துக் கோளத்தின் உள் நோக்கி அமைந்து ஈர்க்கப்படுகின்றன. இதற்கு நீர் வெறுக்கும் பிணைப்பு என்று பெயர்.
உங்களுக்குத் தெரியுமா?
சல்ஃபர் அணுக்களுக்கிடையேயுள்ள இடைவெளி
அதிகமாகும்போது புரதங்கள் வளைகிறது. அதனால் அதிகச் சுருள்களைக் கொண்டு முடி காணப்படுகிறது.

5. புரதத்தை அறிவதற்கான சோதனை
புரதங்களில் பெப்டைடு பிணைப்புகள் (-C-N-) இருப்பதால்,
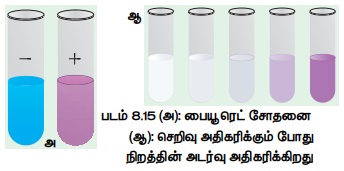
பையூரெட் சோதனையின் போது ஊதா நிறம் தோன்றுகிறது. புரதக்கரைசலுடன் சோடியம் ஹைட்ராக்ஸைடு
கரைசலைச் சமஅளவும் அத்துடன் சில துளிகள் 0.5% தாமிர (II) சல்ஃபேட்டையும் சேர்த்து மெதுவாகக்
கலக்கும் போது, வெப்பமேற்றாமலேயே ஊதா நிறம் தோன்றுகிறது. இந்த நிறமே புரதத்தை அறிய
உதவும் குறியீடாகக் கருதப்படுகிறது (படம் 8.15 அ மற்றும் ஆ).