அணு அமைப்பு | அலகு 12 | 8 ஆம் வகுப்பு அறிவியல் - வேதியியல் வாய்பாடு அல்லது மூலக்கூறு வாய்பாடு | 8th Science : Chapter 12 : Atomic Structure
8 ஆம் வகுப்பு அறிவியல் : அலகு 12 : அணு அமைப்பு
வேதியியல் வாய்பாடு அல்லது மூலக்கூறு வாய்பாடு
வேதியியல் வாய்பாடு அல்லது மூலக்கூறு வாய்பாடு
வேதியியல் வாய்பாடு என்பது ஒரு குறிப்பிட்ட வேதிச்சேர்மம் அல்லது
மூலக்கூறைக் குறிக்கும் எளிய வழிமுறையாகும். இது, ஒரு சேர்மத்தில் இடம்பெற்றுள்ள ஒவ்வொரு
மூலக்கூறிலும் உள்ள அணுக்களின் எண்ணிக்கையைக் குறிக்கிறது. ஒரு வேதிச் சேர்மத்தின்
வேதியியல் வாய்பாட்டை எழுதும் வழி முறைகள் கீழே விளக்கப்பட்டுள்ளன.
படி 1: நேர் அயனியின் குறியீடு இடது புறத்திலும், எதிர் அயனியின்
குறியீடு வலது புறத்திலும் இருக்குமாறு, ஒரு தனிமம் அல்லது அயனியின் குறியீட்டை அருகருகே
எழுத வேண்டும்.
படி 2: அயனிகளின் இணைதிறன்களை தனிமங்களின் குறியீட்டிற்கு மேற்புறத்தில்
எழுதவும் (மின்சுமை குறியீடான '+' (அ) '-' என்பவற்றை எழுதக்கூடாது).
படி 3: தேவையெனில் இணைதிறன் விகிதங்களைச் சுருக்கி அவற்றின்
மிகக் குறைந்த விகிதங்களை எழுதுக. இல்லையெனில், தனிமம் அல்லது அயனியின் இணைதிறனை இடமாற்றம்
செய்க. அந்த விகித எண்களை அடுத்த தனிமத்தின் குறியீட்டிற்கு கீழ்புறத்தில் எழுதவும்
(1 என்ற எண்ணை எழுத வேண்டிய அவசியமில்லை).
இவ்வாறு ஒரு வேதிச்சேர்மத்தின் வேதி வாய்பாட்டை எழுதலாம்.
கால்சியம் குளோரைடின் மூலக்கூறு வாய்ப்பாடினை எழுதும் முறையினை
இப்பொழுது நாம் பார்ப்போம்.
படி
1:
கால்சியம் மற்றும் குளோரின் ஆகியவற்றின் குறியீடுகளை எழுதவும். Ca Cl
படி
2: அத்தனிமத்தின் குறியீட்டின் மேல் அயனிகளின் இணைதிறனை எழுதவும்
Ca2 Cli
படி 3: தனிமங்களின் இணைதிறன்களை மாற்றி எழுதுக. Ca Cl2
எனவே, கால்சியம் குளோரைடின் மூலக்கூறு வாய்பாடு CaCl2,
ஆகும்.
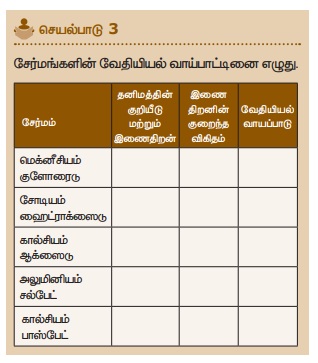
செயல்பாடு 3
சேர்மங்களின்
வேதியியல் வாய்பாட்டினை எழுது.