அணு அமைப்பு | அலகு 12 | 8 ஆம் வகுப்பு அறிவியல் - அடிப்படைத் துகள்கள் | 8th Science : Chapter 12 : Atomic Structure
8 ஆம் வகுப்பு அறிவியல் : அலகு 12 : அணு அமைப்பு
அடிப்படைத் துகள்கள்
அடிப்படைத் துகள்கள்
1878ஆம் ஆண்டில் சர் வில்லியம் குரூக் என்பவர் மின்னிறக்கக்
குழாயைக் கொண்டு சோதனை மேற்கொள்ளும்போது இரு உலோக மின்வாய்களுக்கு இடைப்பட்ட பகுதியில்
கண்ணிற்குப் புலப்படும் வகையில் ஒளிக்கற்றை பாய்வதைக் கண்டார். இக்கதிர்கள் குரூக்
கதிர்கள் கேதோடு கதிர்கள் எனப்பட்டன. இச்சோதனையில் பயன்படுத்தப்படும் மின்னிறக்கக்
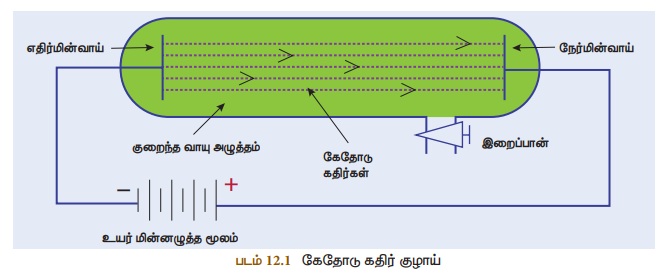
குழாய் 'குரூக்குழாய்' அல்லது 'கேதோடு கதிர் குழாய்' எனப்படுகிறது. கேதோடு கதிர் குழாய்
என்பது வாயு நிரப்பப்பட்ட, இருபுறமும் மூடப்பட்ட ஒரு நீண்ட கண்ணாடிக்குழாயாகும். இதன்
இருமுனைகளிலும் இரு உலோகத் தகடுகள் (மின்வாய்கள்) அதிக மின்னழுத்த வேறுபாடு தரும் மின்கலனுடன்
இணைக்கப்பட்டுள்ளன. மின்கலனின் எதிர்மின் முனையுடன் இணைக்கப்படும் மின்வாய் கேதோடு
(எதிர்மின்வாய்) எனவும், நேர்மின் முனையுடன் இணைக்கப்படும் ஆனோடு (நேர்மின்வாய்) எனவும்
அழைக்கப்படுகிறது. மேலும், அதன் பக்கக்குழாயானது இறைப்பானுடன் (Pump) இணைக்கப்பட்டுள்ளது.
மின்னிறக்கக் குழாயினுள் உள்ள அழுத்தத்தைக் குறைக்க இறைப்பான் பயன்படுகிறது.
மின்சாரம்
காற்றின் வழியே பாயும் போது வாயு மூலக்கூறுகளிலிருந்து எலக்ட்ரான்கள் வெளியேறுவதால்
அயனிகள் உருவாகின்றன. மின்னிறக்கம் எனப்படும்.
1. எலக்ட்ரான்
கண்டுபிடிப்பு
10,000 வோல்ட் அல்லது அதற்கு மேற்பட்ட உயர் அழுத்த இதுவே மின்சாரத்தை
வளி மண்டல அழுத்தத்தில் வாயு அல்லது காற்றினால் நிரப்பப்பட்ட மின்னிறக்கக் குழாயினுள்
செலுத்தும் போது காற்றின் வழியே எந்தவித மின்சாரமும் பாய்வதில்லை. ஆனால் மின்னிறக்கக்குழாயில்
0.001 மிமீ அளவிலான மிகக் குறைந்த வளிமண்டல அழுத்தத்தில் நிரப்பப்பட்டிருக்கும் வாயுவின்
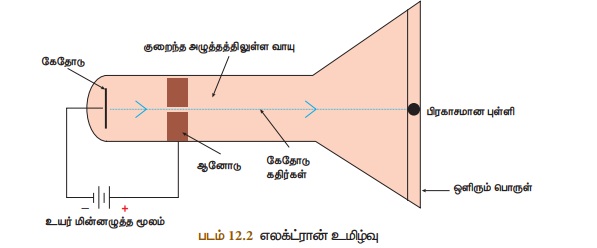
வழியே 10,000 வோல்ட் அளவிலான உயர் அழுத்த மின்சாரத்தைச் செலுத்தும் போது குழாயின் மறுமுனையில்
ஒளிர்தல் ஏற்படுவதைக் காணலாம். இக்கதிர்கள் எதிர்மின்வாயிலிருந்து வெளிவருவதால் கேதோடு
கதிர்கள் (எதிர்மின்வாய்க் கதிர்கள்) எனப்பட்டன. பின்னர் இவை எலக்ட்ரான்கள் எனப் பெயரிடப்பட்டன.
காற்று
மின்கடத்தாப் பொருளாக இருப்பது இயற்கையின் வரமாகும். ஒருவேளை காற்று ஒரு சிறந்த மின்
கடத்தியாக இருக்குமானால், எதிர்பாராத விபத்தினால் உருவாகும் சிறு மின்பொறிகூட மிகப்பெரிய
ஆபத்தினை விளைவிக்கக்கூடும்.
கேதோடு
கதிர்களின் பண்புகள்
• கேதோடு கதிர்கள் எதிர்மின் முனையிலிருந்து நேர்மின் முனையை
நோக்கி நேர்கோட்டில் பயணிக்கின்றன.
• கேதோடு கதிர்கள் துகள்களால் உருவாக்கப் பட்டவை. எனவே, இவை
நிறை மற்றும் இயக்க ஆற்றலைப் பெற்றிருக்கின்றன.
.• கேதோடு கதிர்கள் எதிர்மின்சுமையைப் பெற்றுள்ளதால், அவை மின்புலம்
மற்றும் காந்தப்புலத்தால் விலக்கமடைகின்றன.
• கேதோடு கதிர்களின் பண்புகள் மின்னிறக்கக் குழாயில் நிரப்பப்படும்
வாயுக்களைப் பொருத்து மாறுபடுவதில்லை.
தொலைக்காட்சிப்
பெட்டியில் கேதோடு கதிர்கள் மின்காந்த சுருள்களால் உருவாக்கப்படும் காந்தப்புலத்தால்
விலகலடைந்து அதன் முகப்புத் திரையில் வீழ்த்தப்படுகின்றன. ஒளிப்படத்தை உருவாக்குகின்றன.
2. புரோட்டான்
கண்டுபிடிப்பு
அணுவானது நடுநிலைத் தன்மை உடையது. அணுவில் எதிர் மின்னூட்டம்
கொண்ட துகள்கள் இருப்பதால் அவற்றைச் சமன் செய்ய அதே அளவிலான நேர்மின்னூட்டம் கொண்ட
துகள்கள் இருக்க வேண்டும் என் கோல்ட்ஸ்டீன் கருதினார்.
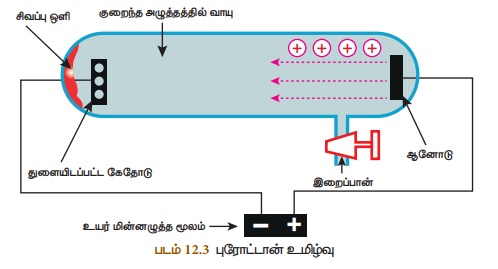
கோல்ட்ஸ்டீன், துளையிடப்பட்ட எதிர்மின் வாயைப் பயன்படுத்தி எதிர்மின்வாய்க்
கதிர் சோதனையை மீண்டும் நடத்தினார். குறைந்த அழுத்தத்தில் உள்ள வாயுவினுள் உயர் மின்
அழுத்தத்தைச் செலுத்தும்போது எதிர் மின்வாயின் பின்புறம் மங்கிய சிவப்பு நிற ஒளியானது
தோன்றுவதைக் கண்டார். இக்கதிர்கள் நேர்மின்வாயிலிருந்து உருவாவதால் அவை நேர்மின்வாய்க்
கதிர்கள் அல்லது ஆனோடு கதிர்கள் அல்லது கால்வாய் கதிர்கள் என அழைக்கப்பட்டன. நேர்மின்வாய்க்
கதிர்கள் நேர்மின்னூட்டம் கொண்ட துகள்களால் ஆனவை.
கண்ணிற்குப்
புலப்படாத கதிர்கள் துத்தநாக சல்பைடு பூசப்பட்ட திரையில் விழும் போது கண்ணிற்குப்புலப்படும்
ஒளியை உமிழ்கின்றன. இப்பொருள்கள் ஒளிரும் பொருள்கள் எனப்படுகின்றன.
ஆனோடு
கதிர்களின் பண்புகள்
• ஆனோடு கதிர்கள் நேர் கோட்டில் செல்கின்றன.
• ஆனோடு கதிர்கள் துகள்களால் ஆனவை.
• ஆனோடு கதிர்கள் மின்புலம் மற்றும் காந்தப் புலத்தால் விலக்கமடைகின்றன.
அவை நேர் மின்னூட்டம் கொண்டுள்ளதால் எதிர் மின்வாயை நோக்கி விலக்கமடைகின்றன.
• நேர் மின்வாய்க் கதிர்களின் பண்புகள் மின்னிறக்கக் குழாயினுள்
இருக்கும் வாயுவின் தன்மையைச் சார்ந்து அமையும்.
• துகளின் நிறை மின்னிறக்கக் குழாயிலுள்ள வயுவின் அணு நிறைக்குச்
சமமாக இருக்கும்.
ஹைட்ரஜன்
வாயுவை மின்னிறக்கக் குழாயினுள் எடுத்துக்கொள்ளும் போது பெறப்படும் நேர்மின்துகள்கள்
புரோட்டான்கள் எனப்படுகின்றன. ஒரு ஹைட்ரஜன் அணுவிலிருந்து ஒரு எலக்ட்ரானை நீக்கும்போது
ஒரு புரோட்டான் கிடைக்கிறது. எனவே புரோட்டான் என்பதை ஹைட்ரஜன் அயனி (H+) எனவும் அழைக்கலாம்..
H → H+ + e-
3. நியூட்ரான்
கண்டுபிடிப்பு
ஜே.ஜே.தாம்சனின் காலத்தில் இரண்டு அடிப்படைத்துகள்கள் மட்டுமே
கண்டுபிடிக்கப் பட்டிருந்தன (புரோட்டான் மற்றும் எலக்ட்ரான்). 1932ஆம் ஆண்டு ஜேம்ஸ்
சாட்விக் மற்றொரு அடிப்படைத்துகளான நியூட்ரானைக் கண்டு பிடித்தார். அணுவில் நியூட்ரான்களின்
அமைவிடத்தைப் பற்றிய தெளிவான விளக்கத்தை ரூதர்போர்டு தனது அணுக்கொள்கையில் குறிப்பிட்டுள்ளார்.
ரூதர்போர்டு அணுமாதிரியைப் பற்றி விரிவாக உங்களது மேல்வகுப்புகளில் அறிந்து கொள்ளலாம்.
நியூட்ரானின்
பண்புகள்
. • நியூட்ரான் மின்சுமையற்ற துகள். எனவே, இது மின்
நடுநிலைத்தன்மை வாய்ந்தது.
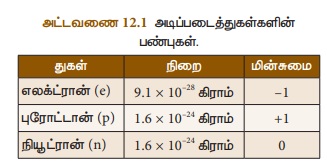
• இதன் நிறை புரோட்டானின் நிறைக்குச் சமமானது நியூட்ரானின் நிறை
1.6 × 10-24 கி.
செயல்பாடு 1