அணு அமைப்பு | அலகு 12 | 8 ஆம் வகுப்பு அறிவியல் - வேதிச் சேர்க்கை விதிகள் | 8th Science : Chapter 12 : Atomic Structure
8 ஆம் வகுப்பு அறிவியல் : அலகு 12 : அணு அமைப்பு
வேதிச் சேர்க்கை விதிகள்
வேதிச் சேர்க்கை விதிகள்
வேதிவினைகளின் பருமனறி அளவீடுகளை உற்றுநோக்கும்போது இவ்வினைகள்
அனைத்தும் குறிப்பிட்ட விதிகளுக்கு உட்பட்டு நடக்கின்றன என்பதை அறியலாம். இவ்விதிகளே
'வேதிச் சேர்க்கை விதிகள் ஆகும். அவையாவன:
1. பொருண்மை அழியா விதி.
2. மாறாவிகித விதி.
3. பெருக்கல் விகித விதி.
4. கே- லூசாக்கின் பருமன் இணைப்பு விதி.
இப்பாடத்தில் முதல் இரண்டு விதிகளைப் பற்றிப் பார்ப்போம். அடுத்த
இரண்டு விதிகளைப் பற்றி ஒன்பதாம் வகுப்பில் விரிவாகக் காணலாம்.
1. பொருண்மை
அழியா விதி (நிறை அழிவின்மை விநி)
1774ஆம் ஆண்டு லவாய்சியர் என்ற பிரஞ்ச் வேதியியலாளர் ஒரு வேதிவினை
நிகழும்போது வினைபடு பொருள் மற்றும் வினைவிளை பொருள் ஆகியவற்றின் நிறைகளுக்கு இடையேயான
தொடர்பினைப் பற்றிக் கூறினார். இவ்விதிப்படி ஒரு வேதிவினை நிகழும்போது உருவாகும் வினைவிளைபொருள்களின்
மொத்த நிறையானது வினைபடுபொருள்களின் மொத்த நிறைக்குச் சமம்". மேலும் "ஒரு
வேதிவினையின் மூலம் நிறையை ஆக்கவோ, அழிக்கவோ முடியாது" எனவும் பொருண்மை அழியா
விதி கூறுகிறது. ஆதலால், இவ்விதியை நிறை அழிவின்மை விதி எனவும் கூறலாம்.
செயல்பாடு 5
மூடியுடன்
கூடிய ஒரு குடுவையில் ஒருசில பனிக்கட்டித் துண்டுகளை எடுத்துக்கொண்டு அதன் நிறையைக்
கணக்கிடுக. சிறிது நேரத்தில் பனிக்கட்டித் துண்டுகள் உருகி நீராக மாறக்கூடிய மாற்றத்தினைக்
காணலாம். தற்போது மீண்டும் குடுவையின் நிறையைக் காண்க. பனிக்கட்டி உருகுவதற்கு முன்பும்,
உருகிய பின்பும் கணக்கிடப்பட்ட நிறையை ஒப்பிட்டுப் பார்த்தால் இரண்டும் ஒரே அளவில்
இருக்கும். இதன் மூலம் இயற்பியல் மாற்றத்தின்போது அல்லது நிலைமாற்றத்தின்போது பொருள்களின்
நிறையானது மாறாமல் இருக்கும் என்பதை அறியலாம்.
நைட்ரஜன் மற்றும் ஹைட்ரஜனிலிருந்து அம்மோனியா உருவாதல் வினையை
நாம் (ஹேபர் முறை) கருதுவோம்.
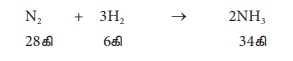
ஹேபர் முறையில் அம்மோனியா உருவாதல் வினை நடைபெறும்போது வினைபடுபொருள்கள்
மற்றும் வினைவிளைபொருள்களின் மொத்த நிறையானது தொடர்ந்து சமமாகவே இருக்கும்.
இவற்றிலிருந்து, இயற்பியல் அல்லது வேதியியல் மாற்றத்தின் மூலம்
நிறையை ஆக்கவோ அல்லது அழிக்கவோ முடியாது என்பது தெளிவாகிறது. எனவே, ஆற்றல் அழிவின்மை
விதி நிரூபிக்கப்படுகிறது.
செயல்பாடு 6
5%
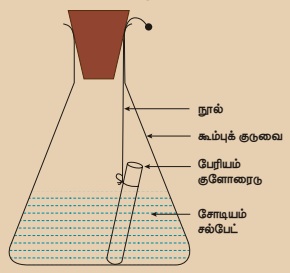
பேரியம் குளோரைடு கரைசல் (5 கி பேரியம் குளோரைடு 100 மி.லி நீரில் கரைக்கப்பட்ட கரைசல்)
மற்றும் சோடியம் சல்பேட் கரைசல்களைத் தனித்தனியாகத் தயாரிக்கவும். சிறிதளவு சோடியம்
சல்பேட் கரைசலை கூம்புக் குடுவையிலும், சிறிதளவு பேரியம் குளோரைடு கரைசலை சோதனைக் குழாயிலும்
எடுத்துக் கொள்க. சோதனைக் குழாயை கூம்புக் குடுவையினுள் தொங்கவிடுக. கூம்புக் குடுவையின்
நிறையைக் காண்க. அதன்பின் இரண்டு கரைசல்களும் ஒன்றாகச் சேரும் வண்ணம் கூம்புக்குடுவையை
நன்றாகக் கலக்கவும். வேதிவினை முடிந்தபின் குடுவையின் நிறையைக் காண்க. இரண்டு கரைசல்களுக்கிடையே
நிகழும் வினையைக் கவனித்துப் பதிவு செய்தால் குடுவையின் நிறையானது வேதிவினைக்கு முன்னும்
வேதிவினைக்குப் பின்னும் சமமாக இருக்கும்.
2. மாறா
விகித விதி
ஜோசப் ப்ரௌஸ்ட் என்ற அறிவியல் அறிஞர் 1779ம் ஆண்டு மாறா விகித விதியைக் கூறினார். அவரின் கூற்றுப்படி ஒன்றுக்கு மேற்பட்ட தனிமங்கள் குறிப்பிட்ட நிறை விகிதத்தில் ஒன்றிணைந்து சேர்மத்தை உருவாக்குகின்றன." இரண்டு அல்லது அதற்கு மேற்பட்ட தனிமங்களைக் கொண்ட சேர்மங்களை அவர் உற்றுநோக்கி, அவை எங்கிருந்து பெறப்பட்டாலும், யார் அதைத் தயார் செய்தாலும், அவை ஒரே விகிதத்தில் தனிமங்களைப் பெற்றுள்ளன எனக் கண்டறிந்தார். உதாரணமாக, பல்வேறு மூலங்களான மழை, கிணறு, கடல், ஆறு ஆகியவற்றிலிருந்து நாம் நீரைப் பெற்றாலும் அதிலுள்ள ஹைட்ரஜன் மற்றும் ஆக்சிஜனின் நிறை எப்பொழுதும் 1:8 என்ற விகிதத்தில் இருக்கும். இதேபோல் பல்வேறு சேர்மங்களின் தயாரிப்பு முறைமாறுபட்டாலும், அவற்றிலுள்ள தனிமங்களின் இயைபு மாறாது. அவை குறிப்பிட்ட விகிதத்தில்தான் இருக்கும். எனவே, இந்த விதி மாறாவிகித விதி எனப்படுகிறது.