அணு இயற்பியல் - அணுக்கருவின் அளவும் அதன் அடர்த்தியும் | 12th Physics : UNIT 9 : Atomic and Nuclear Physics
12 வது இயற்பியல் :அலகு 9 : அணு மற்றும் அணுக்கரு இயற்பியல்
அணுக்கருவின் அளவும் அதன் அடர்த்தியும்
அணுக்கருவின் அளவும் அதன் அடர்த்தியும்
ஆல்பா துகள் சிதறல் ஆய்வு உள்ளிட்ட பலவிதமான
செய்முறைகளைப் பயன்படுத்தி பல அணுக்கருக்களின் மீது வெவ்வேறு ஆய்வுகள் நடத்தப்பட்டுள்ளன.
அவற்றில் இருந்து, அணுக்கருவானது கிட்டத்தட்ட கோள வடிவிலானது என்று தெரிகிறது. மேலும்
செய்முறை ஆய்வுகளின் அடிப்படையில் Z> 10 கொண்ட அணுக்கருக்களுக்கு அவற்றின் ஆரம்
R ஆனது

என்ற வாய்ப்பாடு சோதனை (empirically) மூலம்
பெறப்பட்டுள்ளது. இங்கு A என்பது அணுக்கருவின் நிறை எண் மற்றும் R0 =
1.2 F (1 F = 1 X 10-15m). இங்கு F என்ற அலகு என்ரிகோ பெர்மி என்பாரின்
நினைவாக இடப்பட்டது ஆகும்.
எடுத்துக்காட்டு
8.7
19779Au அணுக்கருவின்
ஆரத்தைக் கணக்கிடுக.
தீர்வு
சமன்பாடு (8.19)-ன் படி,
R = 1.2X10-15 X (197)1/3
= 6.97 X 10-15 M-
அல்லது R = 6.97 F
எடுத்துக்காட்டு
8.8
நிறை எண் A கொண்ட அணுக்கருவின் அடர்த்தியைக்
கணக்கிடுக.
தீர்வு
சமன்பாடு (8.19)ன்படி, அணுக்கருவின் ஆரத்திற்கான

புரோட்டானுக்கும் நியூட்ரானுக்கும் இடையேயுள்ள
நிறை வேறுபாட்டைப் புறக்கணித்தால், நிறை எண் A கொண்ட அணுக்கருவின் நிறை A.m, இங்கு
m என்பது புரோட்டானின் நிறை = 1.6726 x 10-27 kg.
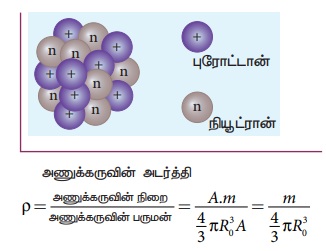
இந்த கோவையைக் கவனிக்கவும்: அணுக்கரு அடர்த்தி
நிறை எண்ணைச் சார்ந்ததல்ல. அதாவது அனைத்து அணுக்கருக்களும் (Z > 10) ஒரே அடர்த்தியை
உடையன. இது அணுக்கருவின் முக்கியமான பண்புகளில் இதுவும் ஒன்று.
கோவையில் உள்ள குறியீடுகளுக்கு மதிப்புகளைப்
பிரதியிட, அணுக்கரு அடர்த்தியின் மதிப்பு
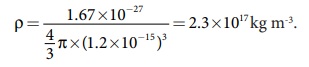
அணுக்கருவிலுள்ள நியூக்ளியான்கள் மிகவும் இறுகத் திணிக்கப்பட்ட நிலையில் இருக்கின்றன என்பதை இந்த மதிப்பு காட்டுகிறது. மேலும் இந்த அடர்த்தியின் மதிப்பை தண்ணீரின் அடர்த்தியுடன் (103kgm-3) ஒப்பிட்டுப் பார்க்கவும்.
ஒரேயொரு தேக்கரண்டி அளவு அணுக்கருவின் பருப்பொருளின் நிறையானது
கிட்டத்தட்ட டிரில்லியன் டன்களுக்குச் சமமாகும்.