Я«ЁЯ«БЯ»Ђ Я«ЄЯ«»Я«▒Я»ЇЯ«фЯ«┐Я«»Я«▓Я»Ї - Я«еЯ«┐Я«▒Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«фЯ«ЙЯ«ЪЯ»ЂЯ««Я»Ї Я«фЯ«┐Я«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ЂЯ««Я»Ї | 12th Physics : UNIT 9 : Atomic and Nuclear Physics
12 Я«хЯ«цЯ»Ђ Я«ЄЯ«»Я«▒Я»ЇЯ«фЯ«┐Я«»Я«▓Я»Ї :Я«ЁЯ«▓Я«ЋЯ»Ђ 9 : Я«ЁЯ«БЯ»Ђ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»Ђ Я«ЄЯ«»Я«▒Я»ЇЯ«фЯ«┐Я«»Я«▓Я»Ї
Я«еЯ«┐Я«▒Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«фЯ«ЙЯ«ЪЯ»ЂЯ««Я»Ї Я«фЯ«┐Я«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ЂЯ««Я»Ї
Я«еЯ«┐Я«▒Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«фЯ«ЙЯ«ЪЯ»ЂЯ««Я»Ї Я«фЯ«┐Я«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ЂЯ««Я»Ї
Я«јЯ«еЯ»ЇЯ«цЯ«хЯ»іЯ«░Я»Ђ Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕЯ«»Я»ЂЯ««Я»Ї Я«ЁЯ«цЯ«┐Я«▓Я»ЂЯ«│Я»ЇЯ«│ Я«еЯ«┐Я«»Я»ѓЯ«ЋЯ»ЇЯ«│Я«┐Я«»Я«ЙЯ«ЕЯ»ЇЯ«еЯ«┐Я«▒Я»ѕЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї
Я«ЋЯ»ѓЯ«ЪЯ»ЇЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ»іЯ«ЋЯ»ѕЯ«»Я»ѕ Я«хЯ«┐Я«Ъ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«хЯ«ЙЯ«Ћ Я«ЅЯ«│Я»ЇЯ«│Я«цЯ»Ђ Я«јЯ«ЕЯ»ЇЯ«▒Я»Ђ Я«єЯ«»Я»ЇЯ«хЯ»ЂЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я««Я»ѓЯ«▓Я««Я»Ї Я«ЋЯ«БЯ»ЇЯ«ЪЯ«▒Я«┐Я«»Я«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«ЪЯ»ЂЯ«│Я»ЇЯ«│Я«цЯ»Ђ. Я«јЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ«ЙЯ«Ћ,
Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»Ї-12 Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ«ЙЯ«ЕЯ«цЯ»Ђ 6 Я«фЯ»ЂЯ«░Я»ІЯ«ЪЯ»ЇЯ«ЪЯ«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я»ѕЯ«»Я»ЂЯ««Я»Ї 6 Я«еЯ«┐Я«»Я»ѓЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я»ѕЯ«»Я»ЂЯ««Я»Ї Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ«цЯ»Ђ.
6
Я«еЯ«┐Я«»Я»ѓЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ =
6x1.00866u = 6.05196u
6 Я«фЯ»ЂЯ«░Я»ІЯ«ЪЯ»ЇЯ«ЪЯ«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ =
6x1.00727u = 6.04362u
Я«јЯ«▓Я«ЋЯ»ЇЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ =
6x0.00055u = 0.0033u
Я«јЯ«ЕЯ«хЯ»Є, Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»Ї-12 Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«јЯ«цЯ«┐Я«░Я»ЇЯ«фЯ»ЇЯ«фЯ«ЙЯ«░Я»ЇЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї
Я«еЯ«┐Я«▒Я»ѕ =
6.05196u +6.04362u = 12.09558u
Я«єЯ«ЕЯ«ЙЯ«▓Я»Ї, Я«еЯ«┐Я«▒Я»ѕЯ««Я«ЙЯ«▓Я»ѕЯ««Я«ЙЯ«ЕЯ«┐Я«»Я»ѕЯ«ЋЯ»Ї Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ»Ђ Я«ЋЯ«БЯ»ЇЯ«ЪЯ«▒Я«┐Я«»Я«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ
Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»Ї-12 Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ = 12 u Я«ЄЯ«цЯ«┐Я«▓Я«┐Я«░Я»ЂЯ«еЯ»ЇЯ«цЯ»Ђ 6 Я«јЯ«▓Я«ЋЯ»ЇЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї
Я«еЯ«┐Я«▒Я»ѕЯ«»Я»ѕ (0.0033 u) Я«ЋЯ«┤Я«┐Я«цЯ»ЇЯ«цЯ«ЙЯ«▓Я»Ї, Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»Ї-12-Я«ЕЯ»Ї Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»Ђ
Я«еЯ«┐Я«▒Я»ѕ =11.9967 u Я«ЄЯ«ЎЯ»ЇЯ«ЋЯ»Ђ Я«єЯ«»Я»ЇЯ«хЯ»ЂЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«ЁЯ«ЪЯ«┐Я«фЯ»ЇЯ«фЯ«ЪЯ»ѕЯ«»Я«┐Я«▓Я»Ї Я«ЋЯ«БЯ»ЇЯ«ЪЯ«▒Я«┐Я«»Я«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ
Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»Ї-12 Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»Ђ Я«еЯ«┐Я«▒Я»ѕЯ«»Я«ЙЯ«ЕЯ«цЯ»Ђ, Я«ЁЯ«цЯ«┐Я«▓Я»ЂЯ«│Я»ЇЯ«│ Я«еЯ«┐Я«»Я»ѓЯ«ЋЯ»ЇЯ«│Я«┐Я«»Я«ЙЯ«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«ЋЯ»ѓЯ«ЪЯ»ЇЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ»іЯ«ЋЯ»ѕЯ«»Я»ѕ Я«хЯ«┐Я«Ъ
Am = 0.09888 ╬╝ Я«ЁЯ«│Я«хЯ»Ђ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«хЯ«ЙЯ«Ћ Я«ЅЯ«│Я»ЇЯ«│Я«цЯ»ѕЯ«ЋЯ»Ї Я«ЋЯ«хЯ«ЕЯ«┐Я«ЋЯ»ЇЯ«ЋЯ«хЯ»ЂЯ««Я»Ї. Я«ЄЯ«еЯ»ЇЯ«ц
Я«еЯ«┐Я«▒Я»ѕ Я«хЯ»ЄЯ«▒Я»ЂЯ«фЯ«ЙЯ«ЪЯ»Ђ ╬ћm Я«єЯ«ЕЯ«цЯ»Ђ Я«еЯ«┐Я«▒Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«фЯ«ЙЯ«ЪЯ»Ђ Я«ЁЯ«▓Я»ЇЯ«▓Я«цЯ»Ђ Я«еЯ«┐Я«▒Я»ѕ Я«ЄЯ«┤Я«фЯ»ЇЯ«фЯ»Ђ Я«јЯ«ЕЯ»ЇЯ«▒Я«┤Я»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї.
Я«фЯ»іЯ«цЯ»ЂЯ«хЯ«ЙЯ«Ћ, M, mP , Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї mn Я«єЯ«ЋЯ«┐Я«» Я«ЋЯ»ЂЯ«▒Я«┐Я«»Я»ђЯ«ЪЯ»ЂЯ«ЋЯ«│Я»Ї Я««Я»ЂЯ«▒Я»ѕЯ«»Я»Є AzX
- Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ, Я«фЯ»ЂЯ«░Я»ІЯ«ЪЯ»ЇЯ«ЪЯ«ЙЯ«ЕЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«еЯ«┐Я«»Я»ѓЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ Я«єЯ«ЋЯ«┐Я«»Я«хЯ«▒Я»ЇЯ«▒Я»ѕЯ«ЋЯ»Ї Я«ЋЯ»ЂЯ«▒Я«┐Я«ЋЯ»ЇЯ«ЋЯ«┐Я«ЕЯ»ЇЯ«▒Я«Е
Я«јЯ«ЕЯ«┐Я«▓Я»Ї, Я«еЯ«┐Я«▒Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«фЯ«ЙЯ«ЪЯ»Ђ
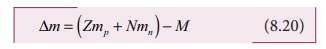
Я«ЄЯ«еЯ»ЇЯ«ц Я«еЯ«┐Я«▒Я»ѕ Я«јЯ«ЎЯ»ЇЯ«ЋЯ»Є Я««Я«▒Я»ѕЯ«еЯ»ЇЯ«цЯ«цЯ»Ђ? Я«ЄЯ«еЯ»ЇЯ«цЯ«ЋЯ»Ї Я«ЋЯ»ЄЯ«│Я»ЇЯ«хЯ«┐Я«ЋЯ»ЇЯ«ЋЯ«ЙЯ«Е
Я«хЯ«┐Я«│Я«ЋЯ»ЇЯ«ЋЯ««Я»Ї Я«љЯ«ЕЯ»ЇЯ«ИЯ»ЇЯ«ЪЯ»ђЯ«ЕЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ - Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»Ї Я«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«ЕЯ»Ї (E = mc2) Я««Я»ѓЯ«▓Я««Я»Ї Я«цЯ«░Я«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
Я«ЄЯ«еЯ»ЇЯ«ц Я«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«ЕЯ»ЇЯ«фЯ«ЪЯ«┐, Я«еЯ«┐Я«▒Я»ѕЯ«»Я»ѕ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я«ЙЯ«ЋЯ«хЯ»ЂЯ««Я»Ї, Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ѕ Я«еЯ«┐Я«▒Я»ѕЯ«»Я«ЙЯ«ЋЯ«хЯ»ЂЯ««Я»Ї Я««Я«ЙЯ«▒Я»ЇЯ«▒ Я««Я»ЂЯ«ЪЯ«┐Я«»Я»ЂЯ««Я»Ї. Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»Ї-12
Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ»ѕЯ«фЯ»ЇЯ«фЯ»іЯ«▒Я»ЂЯ«цЯ»ЇЯ«цЯ«хЯ«░Я»ѕ 6 Я«фЯ»ЂЯ«░Я»ІЯ«ЪЯ»ЇЯ«ЪЯ«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я»ЂЯ««Я»Ї 6 Я«еЯ«┐Я«»Я»ѓЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я»ЂЯ««Я»Ї Я«ЄЯ«БЯ»ѕЯ«еЯ»ЇЯ«цЯ»Ђ Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»Ї-12 Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЂЯ««Я»ЇЯ«фЯ»ІЯ«цЯ»Ђ,
Я«ЄЯ«еЯ»ЇЯ«ц Я«еЯ«┐Я«▒Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«фЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«▒Я»ЇЯ«ЋЯ»ЂЯ«џЯ»Ї Я«џЯ««Я««Я«ЙЯ«Е Я«еЯ«┐Я«▒Я»ѕ ╬ћm Я««Я«▒Я»ѕЯ«еЯ»ЇЯ«цЯ»Ђ, Я«ЁЯ«цЯ»ЂЯ«хЯ»Є Я«єЯ«▒Я»ЇЯ«▒Я«▓Я«ЙЯ«Ћ
Я«хЯ»єЯ«│Я«┐Я«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«ЪЯ»ЂЯ«│Я»ЇЯ«│Я«цЯ»Ђ. Я«ЄЯ«еЯ»ЇЯ«ц Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»Ї Я«фЯ«┐Я«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»Ї (B.E) Я«јЯ«ЕЯ»ЇЯ«▒Я»Ђ Я«ЁЯ«┤Я»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї
Я«ЁЯ«цЯ»Ђ (╬ћm)c2
Я«ЋЯ»ЇЯ«ЋЯ»Ђ Я«џЯ««Я««Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї. Я«ЅЯ«БЯ»ЇЯ««Я»ѕЯ«»Я«┐Я«▓Я»Ї, Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»Ї-12 Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ»ѕ Я«цЯ«ЕЯ«┐Я«цЯ»ЇЯ«цЯ«ЕЯ«┐ Я«еЯ«┐Я«»Я»ѓЯ«ЋЯ»ЇЯ«│Я«┐Я«»Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я«ЙЯ«ЋЯ«фЯ»Ї Я«фЯ«┐Я«░Я«┐Я«фЯ»ЇЯ«фЯ«цЯ«▒Я»ЇЯ«ЋЯ»Ђ
Я«ЄЯ«фЯ»ЇЯ«фЯ«┐Я«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ«џЯ»Ї Я«џЯ««Я««Я«ЙЯ«Е Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ѕ Я«еЯ«ЙЯ««Я»Ї Я«ЁЯ«│Я«┐Я«ЋЯ»ЇЯ«Ћ Я«хЯ»ЄЯ«БЯ»ЇЯ«ЪЯ»ЂЯ««Я»Ї.
Я«фЯ«┐Я«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я«┐Я«ЕЯ»Ї Я«ЁЯ«ЪЯ«┐Я«фЯ»ЇЯ«фЯ«ЪЯ»ѕЯ«»Я«┐Я«▓Я»Ї Я«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»Ђ
(8.20) Я«єЯ«ЕЯ«цЯ»Ђ Я«фЯ«┐Я«ЕЯ»ЇЯ«х Я«░Я»ЂЯ««Я«ЙЯ«▒Я»Ђ Я«јЯ«┤Я»ЂЯ«цЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
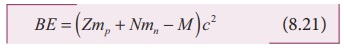
Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»Ђ Я«еЯ«┐Я«▒Я»ѕЯ«»Я»ѕ Я«хЯ«┐Я«Ъ Я«ЁЯ«БЯ»Ђ Я«еЯ«┐Я«▒Я»ѕЯ«»Я»ѕЯ«фЯ»Ї Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ»ЂЯ«хЯ«цЯ»Ђ
Я«хЯ«џЯ«цЯ«┐Я«»Я«ЙЯ«ЋЯ«ЋЯ»Ї Я«ЋЯ«░Я»ЂЯ«цЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«јЯ«ЕЯ«хЯ»Є Я«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»Ђ (8.21) Я«▓Я»Ї Z Я«јЯ«БЯ»ЇЯ«БЯ«┐Я«ЋЯ»ЇЯ«ЋЯ»ѕЯ«»Я»ЂЯ«│Я»ЇЯ«│ Я«јЯ«▓Я«ЋЯ»ЇЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї
Я«еЯ«┐Я«▒Я»ѕЯ«»Я»ѕЯ«ЋЯ»Ї Я«ЋЯ»ѓЯ«ЪЯ»ЇЯ«ЪЯ«┐ Я«фЯ«┐Я«▒Я«ЋЯ»Ђ Я«ЋЯ«┤Я«┐Я«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«фЯ»ІЯ«цЯ»Ђ,
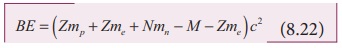
BE = [Z (mp + me ) + Nmn - M - Zme ] c2
Я«ЄЯ«ЎЯ»ЇЯ«ЋЯ»Ђ mp + me = mH
(Я«╣Я»ѕЯ«ЪЯ»ЇЯ«░Я«юЯ«ЕЯ»Ї Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ)
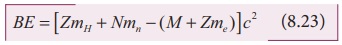
Я«ЄЯ«ЎЯ»ЇЯ«ЋЯ»Ђ M +ZmE = MA Я«ЁЯ«цЯ«ЙЯ«хЯ«цЯ»Ђ,
MA Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ»Ђ AZX Я«цЯ«ЕЯ«┐Я««Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕЯ«»Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї.
Я«ЄЯ«▒Я»ЂЯ«цЯ«┐Я«»Я«ЙЯ«Ћ, Я«ЁЯ«БЯ»Ђ Я«еЯ«┐Я«▒Я»ѕЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«ЁЯ«ЪЯ«┐Я«фЯ»ЇЯ«фЯ«ЪЯ»ѕЯ«»Я«┐Я«▓Я»Ї, Я«фЯ«┐Я«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ
Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»Ї
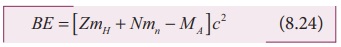
Я«ЋЯ»ЂЯ«▒Я«┐Я«фЯ»ЇЯ«фЯ»Ђ
Я«љЯ«ЕЯ»ЇЯ«ИЯ»ЇЯ«ЪЯ»ђ Я«ЕЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ-Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»Ї Я«џЯ««Я«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ««Я»ѕЯ«»Я»ѕЯ«фЯ»Ї Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐ Я«њЯ«░Я»Ђ Я«ЁЯ«БЯ»Ђ Я«еЯ«┐Я«▒Я»ѕ
Я«ЁЯ«▓Я«ЋЯ«┐Я«▒Я»ЇЯ«ЋЯ»ЂЯ«џЯ»Ї Я«џЯ««Я««Я«ЙЯ«Е Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»Ї Я«хЯ«░Я»ЂЯ««Я«ЙЯ«▒Я»Ђ lu =1.66x10-27 x (3x108)2
=14.94x10-11J = 931MeV Я«єЯ«ЋЯ»ЂЯ««Я»Ї.
Я«јЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ»Ђ
8.9
Я«фЯ«┐Я«ЕЯ»ЇЯ«хЯ«░Я»ЂЯ««Я»Ї Я«цЯ«ЋЯ«хЯ«▓Я»ЇЯ«ЋЯ«│Я»ѕЯ«фЯ»Ї Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐ 42He
Я«ЁЯ«БЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«фЯ«┐Я«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ѕЯ«ЋЯ»Ї Я«ЋЯ«БЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«ЪЯ»ЂЯ«Ћ: Я«╣Я»ђЯ«▓Я«┐Я«»Я««Я»Ї Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«ЁЯ«БЯ»Ђ Я«еЯ«┐Я«▒Я»ѕ MA
(He) = 4.00260u Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«╣Я»ѕЯ«ЪЯ»ЇЯ«░Я«юЯ«ЕЯ»Ї Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«еЯ«┐Я«▒Я»ѕ mH = 1.00785u.
Я«цЯ»ђЯ«░Я»ЇЯ«хЯ»Ђ
:
Я«фЯ«┐Я«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»Ї BE =[zmH + Nmn
- MA ]c2
Я«╣Я»ђЯ«▓Я«┐Я«»Я««Я»Ї Я«ЁЯ«БЯ»ЂЯ«хЯ«┐Я«▒Я»ЇЯ«ЋЯ»Ђ Z=2, N=A-Z=4-2=2
Я«еЯ«┐Я«▒Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«фЯ«ЙЯ«ЪЯ»Ђ
