அணு மாதிரிகள் | இயற்பியல் - அணு நிறமாலை | 12th Physics : UNIT 9 : Atomic and Nuclear Physics
12 வது இயற்பியல் :அலகு 9 : அணு மற்றும் அணுக்கரு இயற்பியல்
அணு நிறமாலை
அணு நிறமாலை
பல்வேறு திட, திரவ மற்றும் அடர்த்தியான வாயுப்
பொருள்களை வெப்பப்படுத்தினால், அவை வெளிவிடும் மின்காந்தக் கதிர்கள் தொடர் நிறமாலையாகக்
காணப்படுகின்றன. எடுத்துக்காட்டாக, ஒரு வெள்ளை நிற ஒளியை நிறமாலைமானியின் உதவியுடன்
ஆராய்ந்தால், அதில் மின்காந்தக் கதிர்களின் அனைத்து அலைநீளங்களும் தொடர் நிறமாலையாகக்
காணப்படுகின்றன.
இருபதாம் நூற்றாண்டின் முற்பகுதியில், தீச்சுடர்
மற்றும் மின்னிறக்கக் குழாய் ஆகியவற்றில் வைக்கப்பட்ட பல்வேறு தனிம அணுக்களினால் வெளிவிடப்படும்,
தனித்தன்மை கொண்ட கதிர்வீச்சுகளை ஆராய்வதில் பல அறிவியல் அறிஞர்கள் ஈடுபட்டனர். அவற்றை
நிறமாலைமானியின் உதவியால் பார்க்கும் போது அல்லது புகைப்படம் எடுத்துப் பார்க்கும்
போது, தொடர் நிறமாலைக்குப் பதிலாக ஒவ்வொன்றிற்கும் தனித்துவமாக உள்ள தனித்தனியான வரிகளின்
தொகுப்பு காணப்பட்டது. அதாவது, வெளிவிடப்படும் (நிறமாலை) ஒளியின் அலை நீளங்கள் நன்கு
வரையறுக்கப்பட்டதாகவும் அவற்றின் இருப்பு நிலை மற்றும் பொலிவு ஆகியவை அந்தந்த தனிமத்துக்கே
உரித்தனவாகவும் இருந்தன (படம் 8.21)
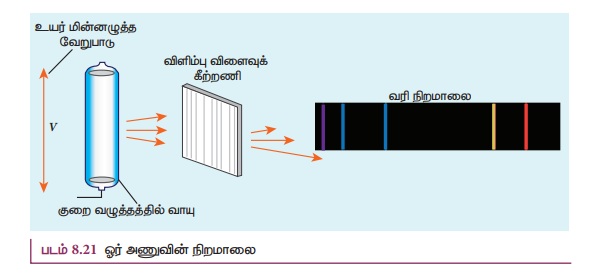
படம் 8.21 ஓர் அணுவின் நிறமாலை
ஒவ்வொரு தனிமத்திற்கும் அதற்கே உரித்தான, தனித்தன்மை
கொண்ட நிறமாலை உள்ளதையும் அதைப் பயன்படுத்தி தனிமத்தைக் கண்டறியலாம் என்பதையும் (ஒவ்வொரு
மனிதரையும் கண்டறிய அவரது விரல் ரேகைகள் பயன்படுவது போல) இதன் மூலம் புரிந்து கொள்ள
முடியும் - அதாவது, வெவ்வேறு வாயுக்களின் நிறமாலையும் வெவ்வேறாக இருக்கும். தனிமங்களின்
வரி நிறமாலைகளின் தனித்துவத்தின் அடிப்படையில், விண்மீன்கள், சூரியன் மற்றும் இனம்
கண்டறியாத சேர்மங்கள் ஆகியவற்றின் உள்ளடக்கங்களை அறிவியல் அறிஞர்கள் கண்டுபிடித்தனர்.
ஹைட்ரஜன்
நிறமாலை
குழாயில் அடைக்கப்பட்ட ஹைட்ரஜன் வாயுவை வெப்பப்படுத்தும்
போது, அதிலிருந்து நன்கு வரையறுக்கப்பட்ட, குறிப்பிட்ட அலைநீளங்களைக் கொண்ட சில மின்காந்த
கதிர்வீச்சுகள் வெளியாகின்றன. இதுவே ஹைட்ரஜன் நிறமாலை எனப்படுகிறது. (XII- வகுப்பு
தொகுதி I, அலகு - 5) ஹைட்ரஜனின் வெளிவிடு மற்றும் உட்கவர் நிறமாலைகள் படம் 8.22 (அ)
மற்றும் (ஆ) வில் கொடுக்கப்பட்டுள்ளன.
எந்தவொரு வாயுவை வெப்பப்படுத்தினாலும், வெப்ப
ஆற்றல் எலக்ட்ரான்களைக் கிளர்வுறச் செய்கிறது. அதேபோல், அணுக்களின் வழியே ஒளியை செலுத்தும்
போது, போட்டான்களை உட்கவர்வதன் மூலமாக எலக்ட்ரான்கள் கிளர்வுறுகின்றன.
போர் எடுகோள்களில் கூறப்பட்டுள்ளதைப் போல
(எடுகோள் -இ), போதுமான அளவு ஆற்றல் அளிக்கப்படும் போது, குறிப்பிட்ட அலைநீளம் (அல்லது அதிர்வெண்) கொண்ட ஆற்றலை உட்கவர்வதன் மூலம்
எலக்ட்ரான்கள் அதன் நிலையில் இருந்து அதிக ஆற்றல் நிலைக்குத் தாவுகின்றன. குறிப்பிட்ட
அலைநீளங்கள் (அல்லது அதிர்வெண்கள்) ஒளியில் இல்லாதபோது, அதன் உட்கவர் நிறமாலையில் இருள்
வரிகளாகக் காணப்படுகின்றன (படம் 8.22 (அ).
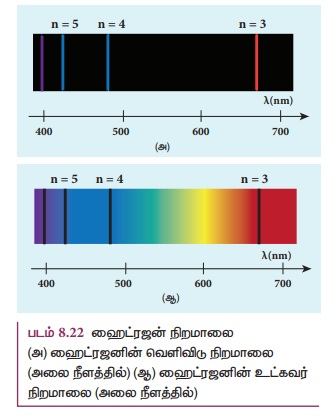
படம் 8.22 ஹைட்ரஜன் நிறமாலை (அ) ஹைட்ரஜனின்
வெளிவிடு நிறமாலை (அலை நீளத்தில்) (ஆ) ஹைட்ரஜனின் உட்கவர் நிறமாலை (அலை நீளத்தில்)
கிளர்வு நிலைகளில் எலக்ட்ரான்களின் ஆயுட்காலம்
மிகக் குறைவாக உள்ளதால் (கிட்டத்தட்ட 10-3S), தன்னியல்பு உமிழ்வின் காரணமாக
அவை மீண்டும் அடி நிலைக்குத் தாவுகின்றன. எனவே எந்த நிறங்களை, அதாவது அலைநீளங்களை
(அல்லது அதிர்வெண்கள்) அவை உட்கவர்வு செய்தனவோ அதே நிறங்களை வெளிவிடுகின்றன (படம்
8.22 (அ) இதையே வெளிவிடு நிறமாலை என்பர். இந்த வரிகளின் அலைநீளங்களை மிகவும் துல்லியமாகக்
கண்டறிய முடியும். மேலும் இந்த வெளிவிடு கதிர்வீச்சுகளில் கண்ணுறு நிறமாலையின் அலைநீளங்களை
விடக் குறைவாகவோ அதிகமாகவோ உள்ள அலைநீளங்களும் காணப்படுகின்றன.
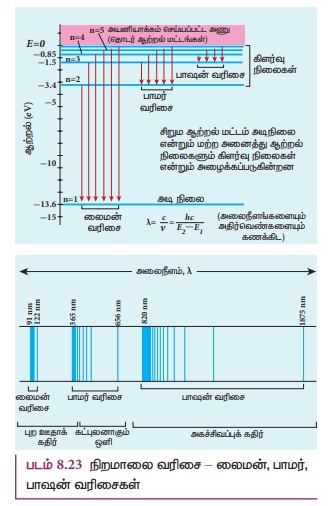
படம் 8.23 நிறமாலை வரிசை - லைமன், பாமர், பாஷன்
வரிசைகள்
ஹைட்ரஜனின் நிறமாலை வரிகள் வெவ்வேறு வரிசைத்
தொகுதிகளாக உள்ளதைக் கவனிக்கவும். (படம் 8.23). ஒவ்வொரு வரிசைத் தொகுதியிலும் அலைநீளம்
குறையக் குறைய, வரிசையிலுள்ள அடுத்தடுத்த அலைநீளங்களுக்கு இடையேயுள்ள தொலைவும் குறைகின்றது.
மேலும், ஒவ்வொரு வரிசையிலும் அலைநீளங்கள் எல்லை மதிப்பை எட்டுவதைக் காணலாம். இது வரிசை
எல்லை என்றழைக்கப்படும். இந்த வரிசைகளுக்கு லைமன் வரிசை, பாமர் வரிசை, பாஷன் வரிசை,
பிராக்கெட் வரிசை மற்றும் ஃபண்ட் வரிசை என்று பெயரிடப்பட்டுள்ளன. இந்த வரிசைகளிலுள்ள
நிறமாலை வரிகளின் அலைநீளங்கள் போர் அணு மாதிரியின் படி தருவிக்கப்பட்ட சமன்பாடுகளுடன்
சரியாக இணங்கி வருகின்றன.
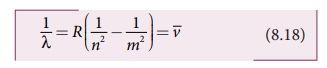
இங்கு ![]() என்பது அலை எண், அலைநீளத்தின்
தலைகீழி , R என்பது ரிட்பர்க் மாறிலி 1.09737 X 107 m-1 மற்றும்
min ஆகியவை நேர்க்குறி முழுவெண்கள்; மேலும் m > n என்ற நிபந்தனையில் பல்வேறு நிறமாலை
தொடர்கள் இங்கே விளக்கப்படுகின்றன:
என்பது அலை எண், அலைநீளத்தின்
தலைகீழி , R என்பது ரிட்பர்க் மாறிலி 1.09737 X 107 m-1 மற்றும்
min ஆகியவை நேர்க்குறி முழுவெண்கள்; மேலும் m > n என்ற நிபந்தனையில் பல்வேறு நிறமாலை
தொடர்கள் இங்கே விளக்கப்படுகின்றன:
(அ) லைமன்
வரிசை
n = 1 மற்றும் m = 2,3,4....... என சமன்பாடு
(8.18)ல் பிரதியிட, லைமன் வரிசையிலுள்ள நிறமாலை வரிகளின் அலை எண் அல்லது அலைநீளங்களைக்
கணக்கிடலாம். இவ்வரிகள் புற ஊதாப் பகுதியில் காணப்படுகின்றன.
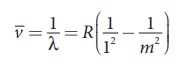
(ஆ) பாமர்
வரிசை
n= 2 மற்றும் m = 3,4,5....... என சமன்பாடு
(8.18)ல் பிரதியிட, பாமர் வரிசையிலுள்ள நிறமாலை வரிகளின் அலை எண் அல்லது அலைநீளங்களைக்
கணக்கிடலாம். இவை கண்ணுறு ஒளிப் பகுதியில் காணப்படுகின்றன.
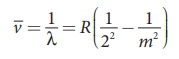
(இ) பாஷன்
வரிசை
n = 3 மற்றும் m = 4,5,6..... என சமன்பாடு
(8,18)ல் பிரதியிட பாஷன் வரிசையிலுள்ள நிறமாலை வரிகளின் அலை எண் அல்லது அலைநீளங்களைக்
கணக்கிடலாம். இவை அருகமை அகச்சிவப்புப் மின்காந்த அலைநீளப்பகுதியில் (near infra-
red) அமைந்துள்ளன.
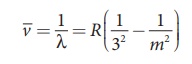
(ஈ) பிராக்கெட்
வரிசை
n = 4 மற்றும் m=5,6,7........ என சமன்பாடு
(8.18) பாஷன் பிரதியிட, பிராக்கெட் வரிசையிலுள்ள நிறமாலை வரிகளின் அலை எண் அல்லது அலைநீளங்களைக்
கணக்கிடலாம். இவ்வரிகள் அகக்சிவப்பு மின்காந்த அலைநீளப் பகுதியில் (அகச்சிவப்பு பகுதியின் மையத்தில் middle
infrared) அமைந்துள்ளன.
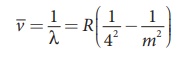
(உ) ஃபண்ட்
வரிசை
n = 5 மற்றும் m=6,7,8 என சமன்பாட (8.18)ல்
பிரதியிட, ஃபண்ட் வரிசையிலுள்ள நிறமாலை வரிகளின் அலை எண் அல்லது அலைநீளங்களைக் கணக்கிடலாம்.
இவ்வரிகளும் அகச்சிவப்புப்மின்காந்த அலைநீளப் பகுதியில் (அதிக அலைநீளம் கொண்ட அகச்சிவப்பு
பகுதியில் far infra-red)அமைந்துள்ளன.
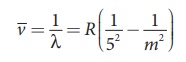
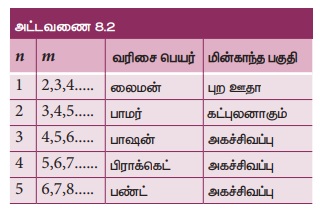
மேற்கூறிய நிறமாலை வரிசைகள் அட்டவணை 8.2-ல்
பட்டியல் இடப்பட்டுள்ளன.
போர்
அணு மாதிரியின் குறைபாடுகள்:
போர் அணு மாதிரியின் குறைபாடுகள் பின்வருமாறு:
(அ) ஹைட்ரஜன் அல்லது ஹைட்ரஜனைப் போன்ற அணுக்களுக்கு
மட்டுமே போர் அணு மாதிரி பொருத்தமானது. பிற சிக்கலான அணுக்களுக்கு இது பொருந்துவதில்லை.
(ஆ) ஹைட்ரஜன் நிறமாலையின் வரிகளை உற்றுநோக்கும்
போது, ஒவ்வொரு வரியும் பல மங்கலான வரிகளால் ஆனது எனத் தெரிகிறது. இதை நுண்வரியமைப்பு
(fine structure) என்பர். போர் கொள்கை இதற்கு
விளக்கம் தரவில்லை .
(இ) நிறமாலை வரிகளின் செறிவில் காணப்படும்
மாற்றங்களுக்கான விளக்கம் போர் அணு மாதிரியால் தரப்படவில்லை .