அணு இயற்பியல் - ஐசோடோப்புகள், ஐசோபார்கள், ஐசோடோன்கள் | 12th Physics : UNIT 9 : Atomic and Nuclear Physics
12 வது இயற்பியல் :அலகு 9 : அணு மற்றும் அணுக்கரு இயற்பியல்
ஐசோடோப்புகள், ஐசோபார்கள், ஐசோடோன்கள்
ஐசோடோப்புகள், ஐசோபார்கள் மற்றும் ஐசோடோன்கள்
ஐசோடோப்புகள்
இயற்கையில், குறிப்பிட்ட ஒரு தனிமத்தின் அணுக்கள்
சம எண்ணிக்கையுள்ள புரோட்டான்களையும், வேறுபட்ட எண்ணிக்கையுள்ள நியூட்ரான்களையும் பெற்றுள்ளதை
நாம் அறிவோம். இத்தகைய அணுக்கள் ஐசோடோப்புகள் எனப்படுகின்றன. அதாவது, சமமான அணு எண்
(Z) மற்றும் வேறுபட்ட நிறை எண் (A) கொண்ட ஒரே தனிமத்தின் அணுக்கள் ஐசோடோப்புகள் எனப்படும்.
எடுத்துக்காட்டாக, ஹைட்ரஜன் அணு மூன்று ஐசோடோப்புகளைக் கொண்டது, அவை ![]() (ஹைட்ரஜன்),
(ஹைட்ரஜன்),
![]() (டியூட்டிரியம்) மற்றும்
(டியூட்டிரியம்) மற்றும் ![]() (டிரிட்டியம்) எனக் குறிப்பிடப்படுகின்றன. இவை
அனைத்திலும் ஒரேயொரு புரோட்டான் மட்டுமே உள்ளதைக் கவனிக்கவும். ஹைட்ரஜனில் நியூட்ரான்கள்
இல்லை, டியூட்டிரியத்தில் ஒரு நியூட்ரானும் , டிரிட்டியத்தில் இரண்டு நியூட்ரான்களும்
உள்ளன.
(டிரிட்டியம்) எனக் குறிப்பிடப்படுகின்றன. இவை
அனைத்திலும் ஒரேயொரு புரோட்டான் மட்டுமே உள்ளதைக் கவனிக்கவும். ஹைட்ரஜனில் நியூட்ரான்கள்
இல்லை, டியூட்டிரியத்தில் ஒரு நியூட்ரானும் , டிரிட்டியத்தில் இரண்டு நியூட்ரான்களும்
உள்ளன.
குறிப்பிட்ட ஒரு தனிமத்தில் காணப்படும் ஐசோடோப்புகளின்
எண்ணிக்கையும் அவற்றின் அளவுகளும் தனிமத்திற்குத் தனிமம் வேறுபடும். எடுத்துக்காட்டாக
கார்பன் அணு நான்கு முக்கிய ஐசோடோப்புகள் கொண்டது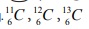 மற்றும்
மற்றும் ![]() ஆனாலும்
இயற்கையில்
ஆனாலும்
இயற்கையில் ![]() -ன் அளவு 98.9% ஆகவும்
-ன் அளவு 98.9% ஆகவும் ![]() -ன் அளவு 1.1% ஆகவும்
-ன் அளவு 1.1% ஆகவும் ![]() -ன்
அளவு 0.0001% ஆகவும் உள்ளது. மற்ற ஐசோடோப்பான
-ன்
அளவு 0.0001% ஆகவும் உள்ளது. மற்ற ஐசோடோப்பான ![]() இயற்கையாகத் தோன்றியது அல்ல, ஆய்வுக்கூடங்களில்
அணுக்கரு வினைகள் மூலம் அல்லது பிரபஞ்சக்கதிர்கள் (Cosmic rays) மூலம் மட்டுமே அதை
உருவாக்க இயலும்.
இயற்கையாகத் தோன்றியது அல்ல, ஆய்வுக்கூடங்களில்
அணுக்கரு வினைகள் மூலம் அல்லது பிரபஞ்சக்கதிர்கள் (Cosmic rays) மூலம் மட்டுமே அதை
உருவாக்க இயலும்.
அணு ஒன்றின் வேதிப்பண்புகள் அதிலுள்ள எலக்ட்ரான்களின்
எண்ணிக்கையை மட்டுமே சார்ந்திருக்கின்றன. தனிமம் ஒன்றின் ஐசோடோப்புகள் ஒரே எலக்ட்ரானிய
அமைப்பை கொண்டுள்ளதால், அவை ஒரே மாதிரியான வேதிப்பண்புகளையும் பெற்று விளங்குகின்றன.
எனவே, தனிம வரிசை அட்டவணையில் ஐசோடோப்புகள் ஒரே இடத்தில் வைக்கப்படுகின்றன.
ஐசோபார்கள்
ஐசோபார்கள் என்பவை சமமான நிறை எண் (A) மற்றும்
வேறுபட்ட அணு எண் (Z) கொண்ட வெவ்வேறு தனிமங்களின் அணுக்கள் ஆகும். அதாவது அவை சம நியூக்ளியான்
எண்ணிக்கை கொண்ட வெவ்வேறு வேதியத் தனிமங்களின் அணுக்களாகும். எடுத்துக்காட்டாக, 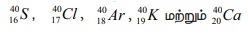 ஆகியவைசமமான நிறை எண் 40 மற்றும் வெவ்வேறு அணு எண்களையும் கொண்ட ஐசோபார்கள்.
ஐசோடோப்புக்களைப் போலல்லாமல் ஐசோபார்கள் வெவ்வேறு தனிமங்களின் அணுக்கள் ஆகும். ஆகவே
அவை மாறுபட்ட இயற்பியல் மற்றும் வேதிப் பண்புகளைப் பெற்றிருக்கும்.
ஆகியவைசமமான நிறை எண் 40 மற்றும் வெவ்வேறு அணு எண்களையும் கொண்ட ஐசோபார்கள்.
ஐசோடோப்புக்களைப் போலல்லாமல் ஐசோபார்கள் வெவ்வேறு தனிமங்களின் அணுக்கள் ஆகும். ஆகவே
அவை மாறுபட்ட இயற்பியல் மற்றும் வேதிப் பண்புகளைப் பெற்றிருக்கும்.
ஐசோடோன்கள்
சம எண்ணிக்கையில் நியூட்ரான்களைக் கொண்டுள்ள
வெவ்வேறு தனிமங்களின் அணுக்கள் ஐசோடோன்கள் எனப்படும். (எ.கா) 125B
மற்றும்136C இவற்றில் 7 நியூட்ரான்கள் உள்ளன.