நம்மைச் சுற்றியுள்ள பருப்பொருள்கள் | முதல் பருவம் அலகு 3 | 7 ஆம் வகுப்பு அறிவியல் - சேர்மங்கள் | 7th Science : Term 1 Unit 3 : Matter Around Us
7 ஆம் வகுப்பு அறிவியல் : முதல் பருவம் அலகு 3 : நம்மைச் சுற்றியுள்ள பருப்பொருள்கள்
சேர்மங்கள்
சேர்மங்கள்
இரண்டு அல்லது அதற்கு மேற்பட்ட தனிமங்களின் அணுக்கள் ஒரு குறிப்பிட்ட விகிதத்தில் வேதிப் பிணைப்பின் மூலம் இணைந்து கிடைக்கும் தூயபொருள் சேர்மம் ஆகும்.

சேர்மங்கள் அவற்றிலுள்ள தனிமங்களின் பண்புகளிலிருந்து முற்றிலும் மாறுபட்ட பண்புகளை வெளிப்படுத்துகின்றன. உதாரணமாக, ஹைட்ரஜன் மற்றும் ஆக்சிஜன் ஆகிய தனிமங்களின் அணுக்கள் ஒரு குறிப்பிட்ட விகிதத்தில் இணைந்து நீர் என்ற சேர்மத்தினை உருவாக்குகின்றன. எனினும், நீரானது ஹைட்ரஜன் மற்றும் ஆக்சிஜனின் பண்புகளைக் கொண்டிருப்பதில்லை. உதாரணமாக, அறை வெப்பநிலையில் நீரானது திரவ நிலையிலும், ஹைட்ரஜன் மற்றும் ஆக்சிஜன் ஆகியவை வாயு நிலையிலும் காணப்படுகின்றன. மேலும், ஆக்சிஜன் எரிதலுக்குத் துணை புரிகிறது. ஆனால், நீர் தீ அணைப்பானாகப் பயன்படுத்தப்படுகிறது.
அதேபோல், சோடியம் மற்றும் குளோரின் ஆகிய இரு தனிமங்களைக் கொண்ட சேர்மம் சாதாரண உப்பு (சோடியம் குளோரைடு) ஆகும். உப்பு நமது உணவில் பயன்படுத்தப்படுகிறது. ஆனால் சோடியம் மற்றும் குளோரின் ஆகியவை நச்சுத்தன்மை கொண்டவை. மேலும், அவை உண்பதற்கு ஏற்றவை அல்ல.

சேர்மங்களின் பண்புகள்
• தனிமங்கள் ஒரு குறிப்பிட்ட விகிதத்தில் இணைவதாலேயே சேர்மங்கள் உருவாகின்றன.
• ஒரு சேர்மத்தின் பண்புகள் அதனை உருவாக்கிய தனிமங்களின் பண்புகளிலிருந்து முற்றிலும் மாறுபடுகின்றன.
• சேர்மங்களை இயற்பியல் முறையில் பிரிக்க இயலாது. ஏனெனில், இவை வேதிப் பிணைப்பினால் இணைக்கப்பட்டுள்ள வெவ்வேறு தனிமங்களைக் கொண்டுள்ளன. சோடியம் குளோரைடை வடிகட்டுதல் போன்ற இயற்பியல் முறையால் பிரிக்க இயலாது.
• சேர்மங்களை வேதியியல் முறையில் மட்டுமே அவற்றின் கூறுகளாகப் பிரிக்க இயலும்.
செயல்பாடு 2
கீழ்க்காணும் அட்டவணையை நிரப்புக.
சேர்மங்கள் தனிமங்களின்உறுப்புகள்
நீர் ஹைட்ரஜன் மற்றும் ஆக்சிஜன்
உப்பு (சோடியம் குளோரைடு) சோடியம் மற்றும் குளோரின்
சோடியம் கார்பனேட் சோடியம், கார்பன் மற்றும் ஆக்சிஜன்
சமையல் சோடா (சோடியம் பைகார்பனேட்) கார்பன் ஹைட்ரஜன் மற்றும் ஆக்சிஜன்
வெள்ளைச் சர்க்கரை (சுக்ரோஸ்) கார்பன் ஹைட்ரஜன் மற்றும் ஆக்சிஜன்
கால்சியம் ஆக்சைடு கால்சியம் மற்றும் ஆக்சிஜன்
கால்சியம் ஹைட்ராக்சைடு கால்சியம் ஹைட்ரஜன் மற்றும் ஆக்சிஜன்
சோடியம் ஹைட்ராக்சைடு சோடியம் ஹைட்ரஜன் மற்றும் ஆக்சிஜன்
பொட்டாசியம் ஹைட்ராக்சைடு பொட்டாசியம் ஹைட்ரஜன் மற்றும் ஆக்சிஜன்
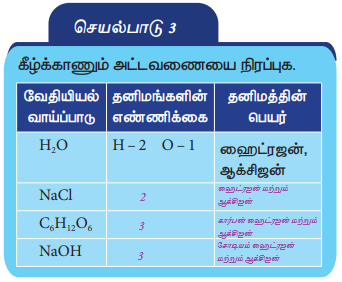
செயல்பாடு 3
கீழ்க்காணும் அட்டவணையை நிரப்புக.
அட்டவனை 3.4 தனிமங்கள் மற்றும் சேர்மங்களுக்கிடையேயான வேறுபாடுகள்
தனிமங்கள்
1. தனிமங்களே ஒரு பருப்பொருளின் எளிமையான பொருளாகும்.
2. தனிமங்கள் இணைந்து சேர்மங்களை உருவாக்குகின்றன.
3. தனிமங்களின் அடிப்படைத் துகள்கள் அணுக்கள் ஆகும்.
சேர்மங்கள்
1. இரண்டு அல்லது அதற்கு மேற்பட்ட தனிமங்கள் இணைவதின் மூலம் உருவாகும் ஒரு வேதியியல் பொருள் சேர்மம் ஆகும்.
2. சேர்மங்களை தனிமங்களாகப் பிரிக்க இயலும்.
3. சேர்மங்களின் அடிப்படைத் துகள்கள் மூலக்கூறுகள் ஆகும்.