கரிம நைட்ரஜன் சேர்மங்கள் | வேதியியல் - சுருக்கமான விடையளி | 12th Chemistry : UNIT 13 : Organic Nitrogen Compounds
12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 13 : கரிம நைட்ரஜன் சேர்மங்கள்
சுருக்கமான விடையளி
வேதியியல் : கரிம நைட்ரஜன் சேர்மங்கள்
II. சுருக்கமான விடையளி
1. C4H9NO2 என மூலக்கூறு வாய்பாட்டில் அமையும் அனைத்து மாற்றியங்களையும் எழுது, IUPAC பெயரிடுக

2. CH3 NO2 வாய்பாட்டிற்கு இரண்டு மாற்றியங்கள் உள்ளன. இவ்விரண்டையும் எவ்வாறு வேறுபடுத்துவாய்?
α - H ஐக் கொண்டுள்ள 1° மற்றும் 2° நைட்ரோ ஆல்கேன்கள் நைட்ரோ மற்றும் அசி வடிவங்களின் இயங்கு சமநிலைக் கலவையாக காணப்படுகின்றது.

நைட்ரோ வடிவம்
1. குறைவான அமிலத்தன்மை
2. NaOH ல் மெதுவாக கரைகின்றது.
3. FeCl3 கரைசலை நிறமிழக்கச் செய்கிறது.
4. மின்கடத்துத்திறன் குறைவு.
அசி வடிவம்
1. அதிக அமிலத்தன்மை போலி (அ) நைட்ரோனிக் அமிலங்கள் எனப்படும்.
2. NaOH உடன் உடனடியாக கரைகிறது.
3. FeCl3 உடன் செம்பழுப்பு நிறத்தைத் தருகிறது.
4. மின்கடத்துத்திறன் அதிகம்.
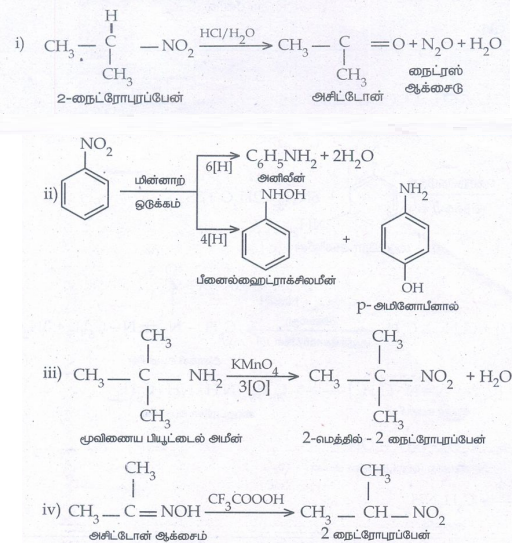
3. பின்வருவனவற்றுள் என்ன நிகழும்.
i.2 - நைட்ரோ புரப்பேனை HCl உடன் கொதிக்க வைக்கும் போது
ii. நைட்ரோ பென்சீன் வலிமையான அமில ஊடகத்தில் மின்னாற் ஒடுக்குதல்
iii. மூவிணைய பியூட்டைலமீனை KMnO4 உடன் ஆக்சிஜனேற்றம் செய்தல் iv. அசிட்டோன் ஆக்சைமை ட்ரைபுளூரோ பெராக்சி அசிட்டிக் அமிலம் கொண்டு ஆக்சிஜனேற்றம் செய்தல்
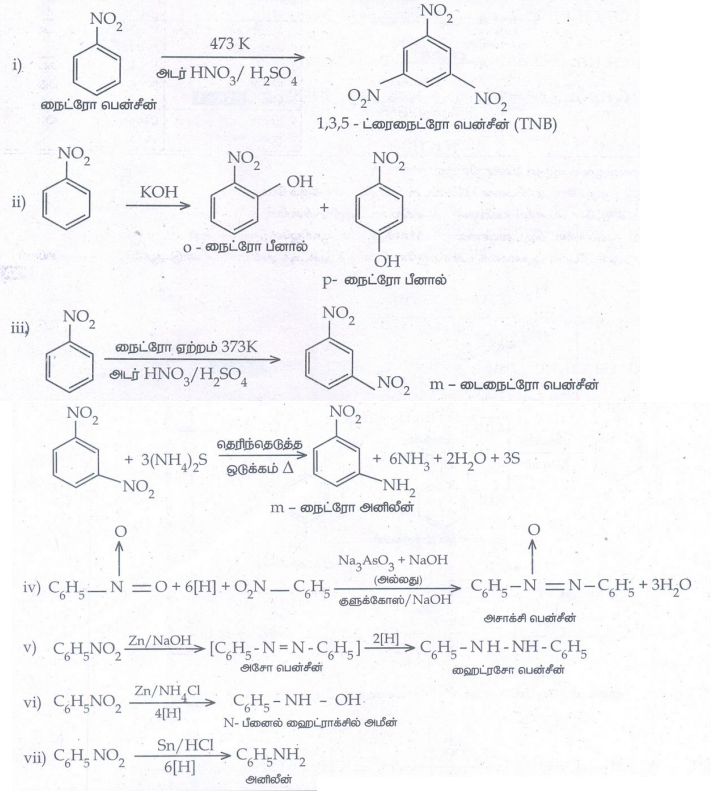
4. நைட்ரோ பென்சீனை பின்வரும் சேர்மங்களாக எவ்வாறு மாற்றுவாய்?
i. 1, 3, 5- ட்ரைநைட்ரோபென்சீன்
ii. ஆர்த்தோ மற்றும் பாரா நைட்ரோ பீனால்
iii. m - நைட்ரோ அனிலீன்
iv. அசாக்சி பென்சீன்
v. ஹைட்ரசோ பென்சீன்
vi. N - பினைல்ஹைட்ராக்சிலமீன்
vii. அனிலீன்
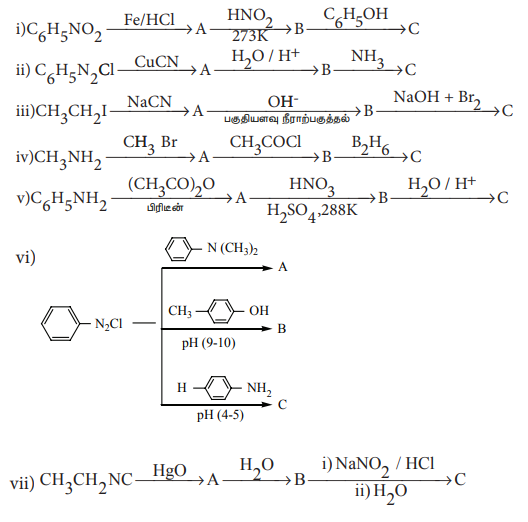
5. பின்வரும் வினைவரிசையில் உள்ள A,B மற்றும் C ஆகிய சேர்மங்களை கண்டறிக.
விடை :
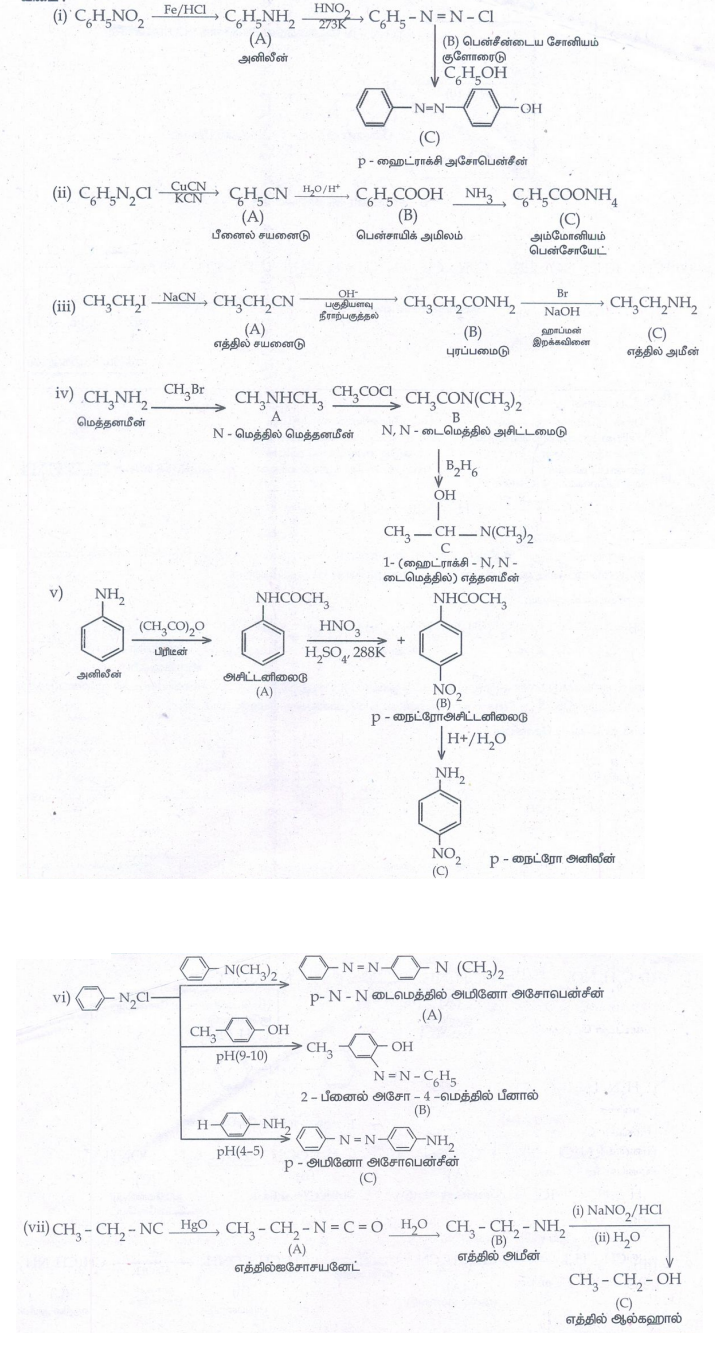
6. சிறுகுறிப்பு வரைக
i. ஹாப்மன் புரோமமைடு வினை
ii. அமோனியாவால் பகுப்பு
iii. காப்ரியல் தாலிமைடு தொகுப்பு
iv. ஸ்காட்டன் - பௌமான் வினை
v. கார்பைலமீன் வினை
vi. கடுகு எண்ணெய் வினை
vii. இணைப்பு வினை
viii. டையசோஆக்கல் வினை
ix. காம்பெர்க் வினை மார்ச் - 2020
i. ஹாப்மன் புரோமமைடு வினை:
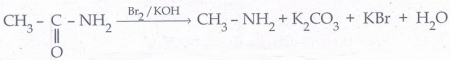
அமைடுகளை புரோமினுடன் நீர்த்த அல்லது ஆல்கஹாலில் கரைக்கப்பட்ட KOH முன்னிலையில் வினைப் படுத்த, அமைடை விட ஒரு கார்பன் குறைவான அமீன்கள் உருவாகின்றன.
ii. அம்மோனியாவால் பகுப்பு:
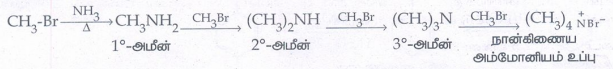
ஆல்கைல் ஹாலைடுகளை ஒரு மூடப்பட்ட குழாயில் ஆல்கஹால் கலந்த அம்மோனியாவுடன் வினைபடுத்தும் போது, 1°,2° மற்றும் 3° அமீன்கள் நான்கிணைய அம்மோனியம் உப்பு உருவாகின்றன.
iii. காப்ரியல் தாலிமைடு தொகுப்பு:
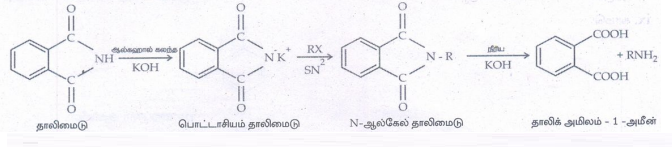
தாலிமைடை ஆல்கஹால் கலந்த KOH உடன் வினைபடுத்தும்போது பொட்டாசியம் தாலிமைடு உருவாகிறது. இதனை ஆல்கைல் ஹாலைடுடன் வினைபடுத்தும் போது N-ஆல்கைல் தாலிமைடு உருவாகிறது. இது நீராற் பகுப்படைந்து ஓரிணைய அமீனைத் தருகிறது.
iv. ஸ்காட்டன் பௌமான் வினை:
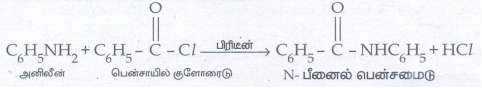
அமீன்கள் பென்சாயிலேற்றம் அடைந்து N-ஆல்கைல் பென்சமைடைத் தரும் வினை ஸ்காட்டன் பௌமன் வினையாகும்.
v. கார்பைலமீன் வினை:
C2H5NH2 + CHCL3 + 3KOH → C2H5NC + 3KCI+3H2O
ஓரிணைய அமீன்கள் குளோரோஃபார்ம் மற்றும் ஆல்கஹால் கலந்த KOH உடன் வினைபுரிந்து அருவருக்கத் தக்க மணமுடைய ஐசோசயனைடுகளைத் தருகின்றன. இது ஓரிணைய அமீன்களை கண்டறியும் சோதனை ஆகும்.
vi. கடுகு எண்ணெய் வினை:
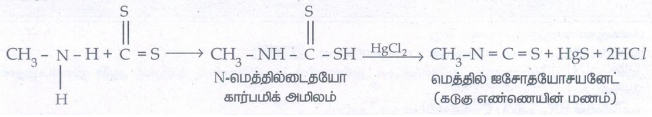
ஓரிணைய அமீன்கள், கார்பன் டைசல்பைடுடன் வினைபுரிந்து N-ஆல்கைல் டைதயோகார்பமிக் அமிலத்தைத் தருகின்றன. இவை HgCl2 உடன் வினைபுரிந்து ஆல்கைல் ஐசோ தயோசயனேட்டை உருவாக்குகின்றன.
vii. இணைப்பு வினை:
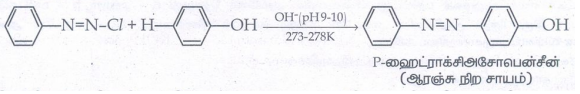
பென்சீன் டையசோனியம் குளோரைடு எலக்ட்ரான் அடர்வினை அதிகம் கொண்ட பீனாலுடன் பாரா நிலையில் எலக்ட்ரான் கவர் பதிலீட்டு வினையில் ஈடுபடுகிறது.
viii. டையசோ ஆக்கல் வினை:

அனிலீன் 273-278K ல் நைட்ரஸ் அமிலத்துடன் வினைபுரிந்து பென்சீன்டையசோனியம் குளோரைடைத் தரும் வினை டையசோ ஆக்கல் வினை:
ix. காம்பெர்க் வினை:
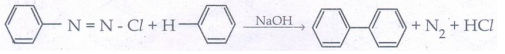
பென்சீன்டைய சோனியம் குளோரைடு NaOH முன்னிலையில் பென்சீனுடன் வினைபுரிந்து பைபீனைலைத் தரும் வினை காம்பெர்க் வினை எனப்படும்.
7. ஓரிணைய, ஈரிணைய, மூவிணைய அமீன்களை எவ்வாறு வேறுபடுத்தி அறிவாய்?
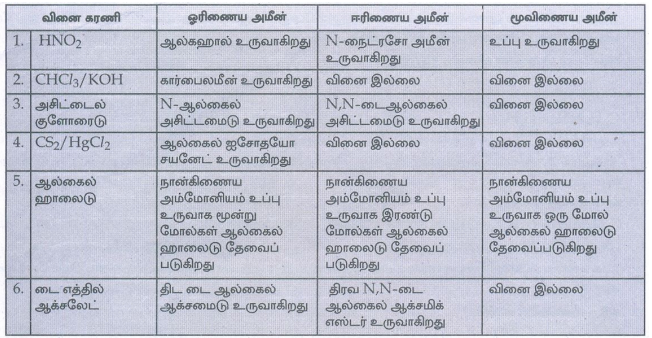
வினை கரணி
1. HNO2
2. CHCl3/KOH
3. அசிட்டைல் குளோரைடு
4. CS2/HgCl2
5. ஆல்கைல் ஹாலைடு
6.டை எத்தில் ஆக்சலேட்
ஓரிணைய அமீன்
1. ஆல்கஹால் உருவாகிறது
2. கார்பைலமீன் உருவாகிறது
3. N-ஆல்கைல் அசிட்டமைடு உருவாகிறது
4. ஆல்கைல் ஐசோதயோ சயனேட் உருவாகிறது
5. நான்கிணைய அம்மோனியம் உப்பு உருவாக மூன்று மோல்கள் ஆல்கைல் ஹாலைடு தேவைப்படுகிறது
6. திட டை ஆல்கைல் ஆக்சமைடு உருவாகிறது
ஈரிணைய அமீன்
1. N-நைட்ரசோ அமீன் உருவாகிறது
2. வினை இல்லை
3. N,N-டைஆல்கைல் அசிட்டமைடு உருவாகிறது
4. வினை இல்லை
5. நான்கிணைய அம்மோனியம் உப்பு உருவாக இரண்டு மோல்கள் ஆல்கைல் ஹாலைடு தேவைப் படுகிறது
6. திரவ N,N-டை ஆல்கைல் ஆக்சமிக் எஸ்டர் உருவாகிறது
மூவிணைய அமீன்
1. உப்பு உருவாகிறது
2. வினை இல்லை
3. வினை இல்லை
4. வினை இல்லை
5. நான்கிணைய அம்மோனியம் உப்பு உருவாக ஒரு மோல் ஆல்கைல் ஹாலைடு தேவைப் படுகிறது
6. வினை இல்லை
8. பின்வருவனவற்றிற்கு காரணம் கூறு
i. அனிலீன் பிரீடல் கிராப்ட் வினைக்கு உட்படுவதில்லை .
ii. அலிபாட்டிக் அமீன்களைவிட அரோமேட்டிக் அமீன்களின் டையசோனியம் உப்புகள் அதிக நிலைப்புத்தன்மை கொண்டது.
iii. அனிலீனின் pKb மதிப்பு மெத்திலமீனை விட அதிகம்
iv. காப்ரியல் தாலிமைடு தொகுப்பு வினை ஓரிணைய அமீன்களை தொகுப்பதற்கானது.
v. எத்திலமீன் நீரில் கரையும் ஆனால் அனிலீன் கரையாது. PTA-3
vi. அமைடுகளைவிட அமீன்கள் அதிக காரத்தன்மை உடையது. PTA - 3
vii. அரோமேட்டிக் எலக்ட்ரான்கவர் பதிலீட்டு வினைகளில் அமினோ தொகுதி o - மற்றும் p - வழி நடத்தும்தொகுதியாக இருப்பினும் அனிலீனின் நைட்ரோ ஏற்றம் செய்யும் வினைகளில் m - நைட்ரோ அனிலீன் கணிசமான விளைபொருளாக கிடைக்கிறது.
i) • அனிலீன் பிரீடல் கிராப்ட் வினைக்கு உட்படுவதில்லை.
• அனிலீன் காரத்தன்மையுடையது.
• இது தனது தனித்த இரட்டை எலக்ட்ரானை AlCl, போன்ற லூயி அமிலத்திற்கு வழங்கி சேர்க்கை விளைபொருளை உருவாக்குவதன் காரணமாக எலக்ட்ரான் கவர்பொருள் பதிலீட்டு வினை நிகழ்வது தடுக்கப்படுகிறது.
ii) • அரோமேட்டிக் அமீன்களின் டையசோனியம் அயனியின் மீதான நேர்மின்சுமை பென்சீன் வளையம் முழுமைக்கும் விரவும் தன்மையை பெற்றிருப்பதால் அரீன்டைய சோனியம் உப்புகள் நிலைப்புத் தன்மையைப் பெறுகின்றன.
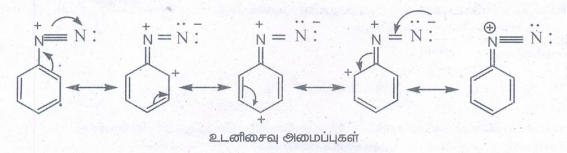
iii) • அனிலீனில் NH2 தொகுதியானது பென்சீன் வளையத்துடன் நேரடியாக இணைக்கப்பட்டுள்ளது.
• அனிலீனின் நைட்ரஜன் அணு மீதான தனித்த இரட்டை எலக்ட்ரான் பென்சீன் வளையத்தினுள் உள்ளடங்காத் தன்மையினைப் பெற்றுள்ளது.
• எனவே புரோட்டானேற்றத்திற்கு தனித்த எலக்ட்ரான் கிடைக்கக்கூடிய வாய்ப்பு குறைகிறது.
• எனவே அனிலீன் மெத்திலமீனை விட குறைந்த காரத்தன்மை உடையது. ஆதலால் அனிலீனின் pKb
• மதிப்பு மெத்திலமீனை விட அதிகம்.
iv) • காப்ரியல் தாலிமைடு தொகுப்பு முறை அலிபாட்டிக் ஓரிணைய அமீன்களை தயாரிக்க பயன்படுகிறது. ஈரிணைய மற்றும் மூவிணைய அமீன்களை இம்முறையில் தயாரிக்க முடியாது. எனவே தூய ஓரிணைய அமீன்களை இம்முறை மூலம் தயாரிக்கலாம்.
v) • எத்தில் அமீன் நீருடன் மூலக்கூறுகளுக்கு இடைப்பட்ட ஹைட்ரஜன் பிணைப்பினை ஏற்படுத்துவதால் நீரில் கரைகிறது.
• அனிலீனில் நீர் வெறுக்கும் அரைல் தொகுதி இருப்பதால், அது அதிகமாக நீருடன் ஹைட்ரஜன் பிணைப்பினை ஏற்படுத்துவதில்லை. எனவே அனிலீன் நீரில் கரைவதில்லை.
vi) • அமைடுகளில் எலக்ட்ரான் கவர் தன்மையுடைய கார்பனைல் தொகுதி எலக்ட்ரான்களை தன் பக்கமாக ஈர்க்கிறது.
• எனவே அமைடின் நைட்ரஜனில் உள்ள எலக்ட்ரான் இரட்டை புரோட்டானேற்றத்திற்கு எளிதில் கிடைப்பதில்லை.
• ஆதலால் அமைடுகள் அமீன்களை விட குறைவான காரத்தன்மை உடையவை.
• அமீன்களின் ஆல்கைல் தொகுதிகள் எலக்ட்ரான் விடுவிக்கும் தொகுதிகள், எனவே நைட்ரஜனின் எலக்ட்ரான் இரட்டை புரோட்டானேற்றத்திற்கு எளிதில் கிடைக்கின்றன.
• எனவே அமீன்கள் அமைடுகளை விட அதிக காரத்தன்மை உடையவை.
vii) • வலிமைமிக்க அமில ஊடகத்தில் அனிலீன் புரோட்டானேற்றம் அடைந்து மெட்டா ஆற்றுப்படுத்தும் அனிலீனியம் அயனியைத் தருகிறது.
• எனவே m-நைட்ரோ அனிலீன் கணிசமான விளைபொருளாகக் கிடைக்கிறது.
9. பின்வருவனவற்றை வரிசைப்படுத்துக.
i) நீரில் கரைதிறனின் ஏறுவரிசை, C6H5NH2(C2H5)2NH,C2H5NH2
ii) காரவலிமையின் ஏறுவரிசை
a) அனிலீன், p - டொலுடின் மற்றும் p - நைட்ரோ அனிலீன்
b) C6H5NH2, C6H5NHCH3, C6H5NH2, p-C1-C6H4-NH2
iii) வாயுநிலைமைகளில் காரவலிமையின் இறங்குவரிசை
(C2H5)NH2 (C2H5) NH, (C2H5),N மற்றும் NH3
iv) கொதிநிலையின் ஏறுவரிசை C6H5OH, (CH3)2NH,C2H5NH2
v) pKb மதிப்புகளின் இறங்கு வரிசை C2H5NH2, C6H5NHCH)3 (C2H5)2 NH மற்றும் CH3 NH2 PTA - 1
vi) கார வலிமையின் ஏறுவரிசை C6H5NH2, C6H5N(CH3)2 (C2H5)2 NH மற்றும் CH3 NH2 PTA - 1
vii) காரவலிமையின் இறங்கு வரிசை
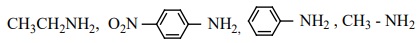
i) நீரில் கரைதிறனின் ஏறுவரிசை C6H5NH2 < (C2H5)2 NH< C2H5 -NH2
காரணம்: அரோமேட்டிக் அமீன் < அலிஃபாட்டிக் அமீன்
நீரில் கரைதிறன் ɑ = 1/மூலக்கூறு நிறை
ii) a) கார வலிமையின் ஏறுவரிசை
p - நைட்ரோ அனிலீன் < அனிலீன் <p-டொலுடின்
காரணம்: - p-நைட்ரோ தொகுதி (-I) எலக்ட்ரான் ஈர்க்கும் தொகுதி, எனவே காரத்தன்மை குறைவு.
p-மெத்தில் தொகுதி (+I) எலக்ட்ரான் விடுவிக்கும் தொகுதி, எனவே காரத்தன்மை அதிகம்.
b) p-CI-C6H4-NH2 < C6H5NH2 < C6H5NHCH3 < C6H5NH2
iii) வாயு நிலைமையில் கார வலிமையின் இறங்கு வரிசை
(C2H5)3N > (C2H5)2 NH > C2H5 NH2 > NH3
காரணம்: • வாயு நிலைமையில் கரைப்பானேற்ற விளைவு இல்லை.
• அதனால் காரத்தன்மை + 1 விளைவை சார்ந்துள்ளது.
• ஆல்கைல் தொகுதிகளின் எண்ணிக்கை உயரும்போது +1 விளைவும் அதிகரிக்கிறது. காரத்தன்மையும் அதிகரிக்கிறது.
iv. கொதிநிலையின் ஏறுவரிசை (CH3)2NH< C2H5NH2<C6H5OH
காரணம்: • அமீன்கள் வலிமை குறைந்த ஹைட்ரஜன் பிணைப்பை ஏற்படுத்துவதால் அவற்றின் கொதிநிலை ஆல்கஹால்களை விடக் குறைவு.
• மேலும் கொதிநிலை வரிசை 3° < 2° < 1° அமீன்கள்
v) pKb மதிப்புகளின் இறங்குவரிசை C6H5NHCH3 > C2H5NH2>CH3 NH2> (C2H5)2 NH - காரத்தன்மை அதிகரிக்கிறது → – pKb மதிப்பு குறைகிறது →
காரணம்: குறைந்த pKb மதிப்பு எனில் காரத்தன்மை அதிகம்.
vi) காரவலிமையின் ஏறுவரிசை : C6H5NH2 < C6H5N(CH3)2 < CH3 NH2 < (C2H5)2NH
vii) காரவலிமையின் இறங்குவரிசை
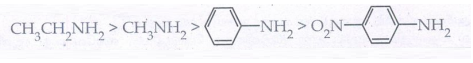
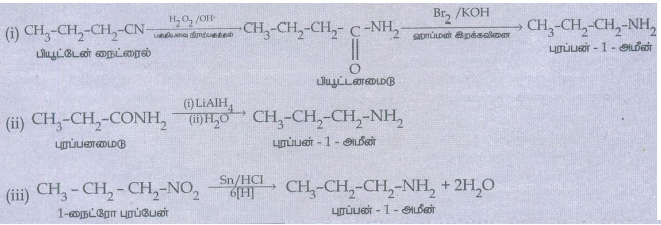
10. பின்வருவனவற்றிலிருந்து புரப்பேன் - 1 - அமீனை எவ்வாறு தயாரிப்பாய்?
1) பியூட்டேன்நைட்ரைல்
ii) புரப்பனமைடு
iii) 1-நைட்ரோ புரப்பேன்
11. A,B மற்றும் C ஐ கண்ட றிக 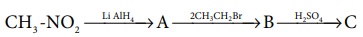
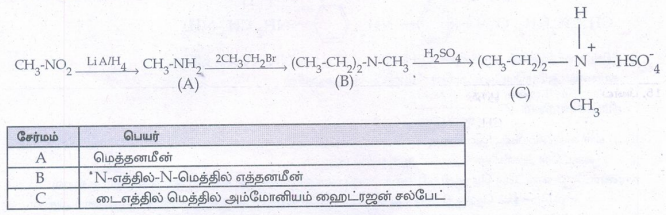
சேர்மம் : பெயர்
A - மெத்தனமீன்
B - *N-எத்தில்-N-மெத்தில் எத்தனமீன்
C - டைஎத்தில் மெத்தில் அம்மோனியம் ஹைட்ரஜன் சல்பேட்
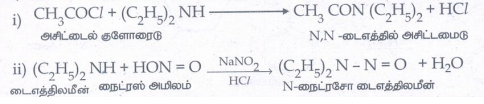
12. டைஎத்திலமீனை பின்வரும் சேர்மங்களாக எவ்வாறு மாற்றுவாய்?
i) N,N - டை எத்தில் அசிட்டமைடு
ii) N - நைட்ரசோடை எத்திலமீன்
விடை:
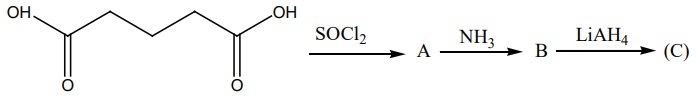
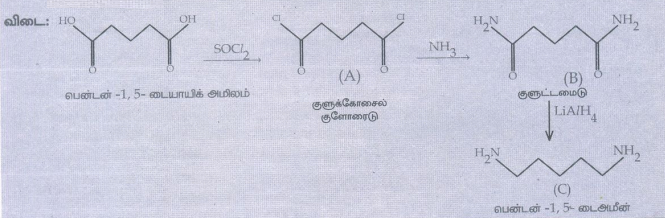
13. A, B மற்றும் C ஐ கண்ட றிக.
விடை:
14. A,B,C மற்றும் D ஐ கண்ட றிக.
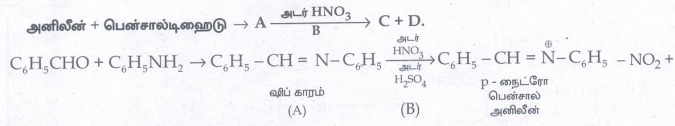
15. பின்வரும் வினைகளை பூர்த்தி செய்க.
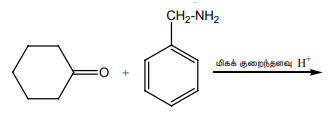
விடை:
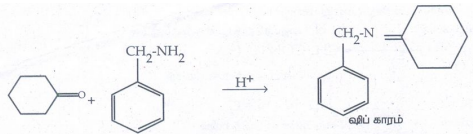
16. பின்வரும் வினையின் A,B, C மற்றும் D ஐக் கண்டறிக.
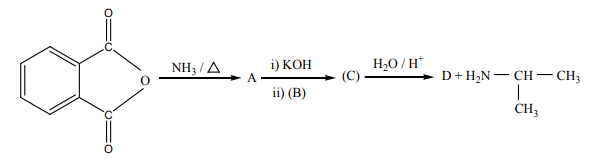
விடை:
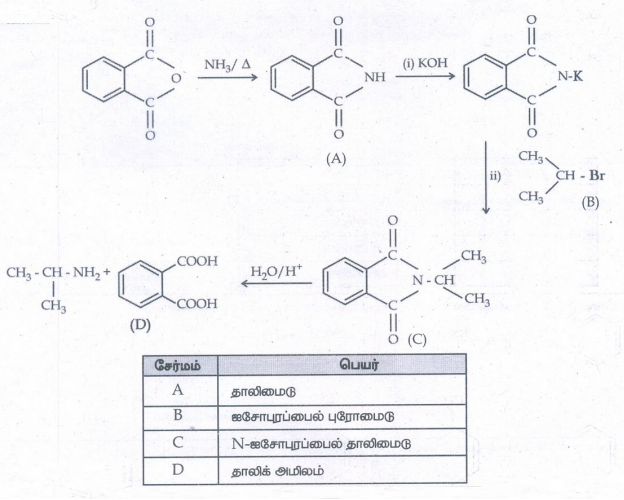
சேர்மம் : பெயர்
A - தாலிமைடு
B - ஐசோபுரப்பைல் புரோமைடு
C - N-ஐசோபுரப்பைல் தாலிமைடு
D - தாலிக் அமிலம்
17. 'A' என்ற சேர்மத்தின் டைபுரோமோ பெறுதியை KCN உடன் வினைப்படுத்தி அமில நீராற்பகுப்பிற்கு உட்படுத்தி வெப்பப்படுத்தும் போது CO2 ஐ வெளியிட்டு ஒரு காரத்துவ அமிலம் 'B' ஐ தருகிறது. "B" ஐ திரவ NH; உடன் வெப்பப்படுத்தி பிறகு Brz/KOH உடன் வினைப்படுத்த சேர்மம் "C" ஐ கொடுக்கிறது. "C" ஐ NaNO2 /HCI உடன் மிக்குறைந்த வெப்பநிலையில் வினைப்படுத்தி ஆக்சிஜனேற்றம் செய்யும் போது ஒரு காரத்துவ அமிலம் "D" ஐ தருகிறது. D-ன் மூலக்கூறு நிறை 74 எனில் A, B, C மற்றும் D ஐ கண்டுபிடி.
D ஆனது ஒரு காரத்துவ அமிலம். மூலக்கூறு நிறை 74.
D ன் வாய்பாடு CnH2n+1COOH எனில்
அதன் மூலக்கூறு நிறை 12 × n + 2n × 1 +1 × 1 + 12 + 2 × 16 + 1 × 1 = 74
14n + 46=74
14n = 28
n = 2
ஃD ஆனது C2 H5 COOH அதவாது CH3 – CH2 - COOH
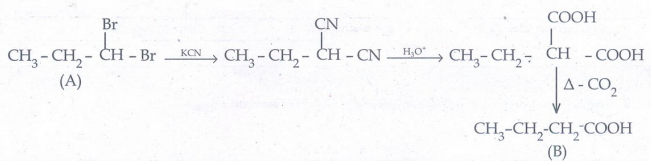
குறிப்பு: இரண்டு - COOH தொகுதிகள் ஒரே கார்பன் அணுவில் பிணைக்கப்பட்டிருந்தால், வெப்பப்படுத்தும் போது CO2 வெளியேறி ஒற்றை கார்பாக்சிலிக் அமிலம் கிடைக்கிறது.
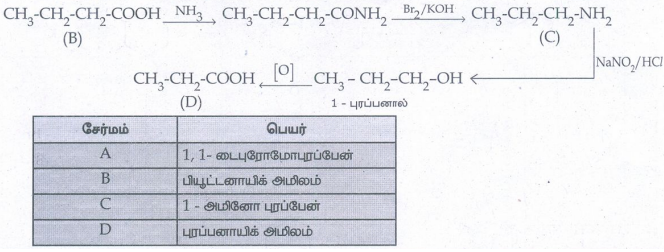
சேர்மம் : பெயர்
A - 1, 1- டைபுரோமோபுரப்பேன்
B - பியூட்டனாயிக் அமிலம்
C - 1- அமினோ புரப்பேன்
D - புரப்பனாயிக் அமிலம்
18. பின்வரும் வினைவரிசையில் உள்ள A முதல் E வரை உள்ள சேர்மங்களை கண்டறிக.
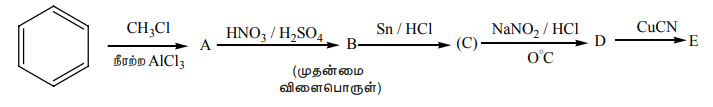
தீர்வு :
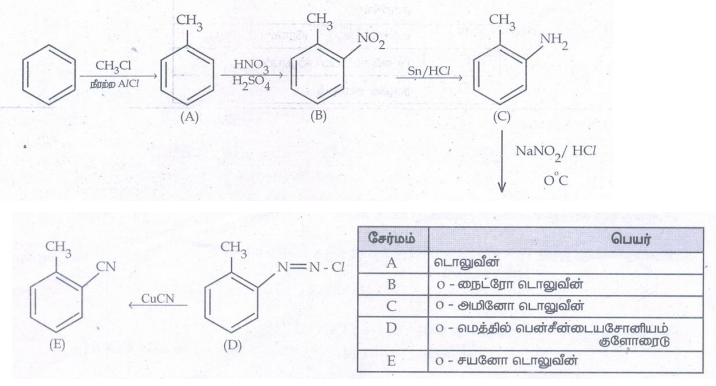
சேர்மம் : பெயர்
A - டொலுவீன்
B - o - நைட்ரோ டொலுவீன்
C - o - அமினோ டொலுவீன்
D - o - மெத்தில் பென்சீன்டையசோனியம் குளோரைடு
E - o - சயனோ டொலுவீன்