அறிமுகம் | வேதியியல் - இடைநிலை மற்றும் உள் இடைநிலைத் தனிமங்கள் | 12th Chemistry : UNIT 4 : Transition and Inner Transition Elements
12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 4 : இடைநிலை மற்றும் உள் இடைநிலைத் தனிமங்கள்
இடைநிலை மற்றும் உள் இடைநிலைத் தனிமங்கள்
அலகு 4
இடைநிலை மற்றும் உள் இடைநிலைத் தனிமங்கள்

மார்ட்டின் ஹெய்ன்ரிக் கிளாப்ரோத்,
(1743- 1817)
மார்ட்டின் ஹெய்ன் ரிக் கிளாப்ரோத், ஜெர்மன் வேதியியல் அறிஞர் ஆவர். யுரேனியம் சிர்கோனியம் மற்றும் சீரியம் ஆகிய தனிமங்களை இவர் - கண்டறிந்துள்ளார். தூய நிலைகளில் இத்தனிமங்களை இவர் பிரித்தெடுக்கவில்லையெனிலும் இவைகள் தனித்தன்மை உடைய தனிமங்கள் என வரையறுத்தார். மேலும் டைட்டேனியம் டெலூரியம் மற்றும் ஸ்டிரான்சியம் ஆகிய தனிமங்களின் கண்டுபிடிப்புகளை இவர் உறுதி செய்தார். கனிமவியல் மற்றும் பகுப்பாய்வு வேதியியல் பிரிவுகளை முறையாக நெறிப்படுத்தியதில் இவரது பங்களிப்பு முக்கியமானதாகும்.
கற்றலின் நோக்கங்கள்
இந்த பாடப் பகுதியைக் கற்றறிந்த பின்னர்
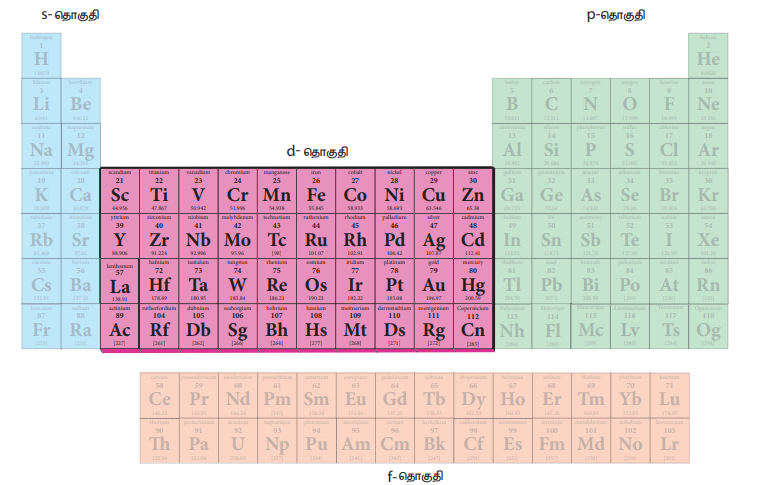
* தனிம வரிசை அட்டவணையில் d மற்றும் f தொகுதி தனிமங்களின் இடத்தினை மீட்டறிதல்.
* 3d வரிசை தனிமங்களின் பொதுப் பண்புகளை விவரித்தல்.
* 3d வரிசை தனிமங்களின் M"*/M திட்ட மின்முனை மின்அழுத்தத்தில் ஏற்படும் மாறுபாடுகளை விவாதித்தல்.
* E° மதிப்புகளிலிருந்து தனிமங்களின் ஆக்சிஜனேற்ற மற்றும் ஒடுக்க பண்புகளைத் தீர்மானித்தல்.
* d தொகுதி தனிமங்களின் அணைவுச் சேர்மங்கள், உலோகக் கலவைகள் மற்றும் இடைச்செருகல் சேர்மங்களை உருவாக்கும் பண்புகளை விளக்குதல்.
* பொட்டாசியம் பெர்மாங்கனேட் மற்றும் பொட்டாசியம் டைகுரோமேட் ஆகியனவற்றின் தயாரித்தல் மற்றும் பண்புகளை விவரித்தல்.
* f தொகுதி தனிமங்களின் பண்புகளை விளக்குதல்.
* லாந்தனாய்டுகள் மற்றும் ஆக்டீனாய்டுகளின் பண்புகளை ஒப்பிடுதல். ஆகிய திறன்களை மாணவர்கள் பெற இயலும்.
அறிமுகம்
உலோக தனிமங்கள் தங்களது நடுநிலை அல்லது நேர் அயனி நிலையில் பகுதியளவு நிரப்பப்பட்ட d அல்லது f உட்கூடுகளை பெற்றிருப்பின் அவைகள் பொதுவாக இடைநிலை உலோகங்கள் என அழைக்கப்படுகின்றன. இந்த வரையறையானது லாந்தனாய்டுகள் மற்றும் ஆக்டினாய்டுகளை உள்ளடக்கியது. எனினும் IUPAC வரையறையின்படி ஒரு தனிமத்தின் அணுவானது முழுவதும் நிரப்பப்படாத d உட்கூட்டினை பெற்றிருந்தாலோ அல்லது அத்தனிமம் உருவாக்கும் நேரயனியானது முழுவதும் நிரப்பப்படாத d உட்கூட்டினை பெற்றிருந்தாலோ அத்தனிமம் ஒரு இடைநிலை உலோகமாகும். இவைகள் தனிம வரிசை அட்டவணையில் மையப் பகுதியில் S மற்றும் p - தொகுதி தனிமங்களுக்கு இடையில் இடம்பெற்றுள்ளன. மேலும், இவைகளின் பண்புகள் அதிக வினைத்திறன் மிக்க S தொகுதி உலோகங்களுக்கும், பெரும்பாலும் அலோகங்கள் இடம்பெற்றுள்ள p தொகுதி தனிமங்களுக்கும் இடைப்பட்டு காணப்படுகிறது. 11வது தொகுதி தனிமங்களைத் தவிர்த்து பெரும்பாலான, இடைநிலை உலோகங்கள் கடினமானவை மற்றும் அதிக உருகுநிலையை உடையவை.
இடைநிலை உலோகங்களான இரும்பு மற்றும் தாமிரம் ஆகியன மனித நாகரீக வளர்ச்சியில் மிக முக்கியப் பங்காற்றியுள்ளன. மேலும், பெரும்பாலான இடைநிலை தனிமங்கள் பல முக்கிய பயன்களைக் கொண்டுள்ளன. எடுத்துக்காட்டாக, டங்ஸ்டன் ஆனது விளக்குகளில் காணப்படும் மின்னிழைகளிலும், டைட்டேனியம் செயற்கை மூட்டுகள் தயாரித்தலிலும், மாலிப்டினம் கொதிகலன்களிலும், பிளாட்டினம் வினைவேகவியலிலும் பயன்படுவதைக் குறிப்பிடலாம். மேலும் இவைகள் பல உயிரியல் அமைப்புகளில் முக்கியப் பங்காற்றுகின்றன. எடுத்துக்காட்டாக, ஹீமோகுளோபினில் காணப்படும் இரும்பு, வைட்டமின் B12 வில் காணப்படும் கோபால்ட் போன்றவற்றைக் குறிப்பிடலாம்.
இப்பாடப்பகுதியில், d தொகுதி தனிமங்களின் குறிப்பாக 3d வரிசை தனிமங்களின் பொது பண்புகள், அவைகளின் வேதி வினைதிறன் ஆகியனவற்றைக் கற்றறிவதுடன், பொட்டாசியம் பெர்மாங்கனேட் KMnO4 மற்றும் பொட்டாசியம் டைகுரோமேட் K2Cr2O7 ஆகிய முக்கியத்துவம் வாய்ந்த சேர்மங்களைப் பற்றியும் கற்றறிய உள்ளோம். மேலும் இப்பாடப் பகுதியின் இறுதியில், நாம் f தொகுதி தனிமங்களைப் பற்றி கற்றறியலாம்.