Я«ЁЯ«»Я«ЕЯ«┐Я«џЯ»Ї Я«џЯ««Я«еЯ«┐Я«▓Я»ѕ | Я«хЯ»ЄЯ«цЯ«┐Я«»Я«┐Я«»Я«▓Я»Ї - Я«ЅЯ«фЯ»ЇЯ«фЯ»Ђ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї | 12th Chemistry : UNIT 8 : Ionic Equilibrium
12 Я«єЯ««Я»Ї Я«хЯ«ЋЯ»ЂЯ«фЯ»ЇЯ«фЯ»Ђ Я«хЯ»ЄЯ«цЯ«┐Я«»Я«┐Я«»Я«▓Я»Ї : Я«ЁЯ«цЯ»ЇЯ«цЯ«┐Я«»Я«ЙЯ«»Я««Я»Ї 8 : Я«ЁЯ«»Я«ЕЯ«┐Я«џЯ»Ї Я«џЯ««Я«еЯ«┐Я«▓Я»ѕ
Я«ЅЯ«фЯ»ЇЯ«фЯ»Ђ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї
Я«ЅЯ«фЯ»ЇЯ«фЯ»Ђ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї
Я«њЯ«░Я»Ђ Я«ЁЯ««Я«┐Я«▓Я««Я»Ї, Я«њЯ«░Я»ЂЯ«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ»ЂЯ«ЪЯ«ЕЯ»ЇЯ«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«еЯ»ЇЯ«цЯ»Ђ Я«њЯ«░Я»Ђ Я«ЅЯ«фЯ»ЇЯ«фЯ»ѕЯ«»Я»ЂЯ««Я»Ї, Я«еЯ»ђЯ«░Я»ѕЯ«»Я»ЂЯ««Я»Ї Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я«ЙЯ«ЕЯ«цЯ»Ђ Я«еЯ«ЪЯ»ЂЯ«еЯ«┐Я«▓Я»ѕЯ«»Я«ЙЯ«ЋЯ»ЇЯ«ЋЯ«▓Я»Ї Я«хЯ«┐Я«ЕЯ»ѕ Я«јЯ«ЕЯ»ЇЯ«▒Я«┤Я»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«еЯ»ђЯ«░Я»ЇЯ«цЯ»ЇЯ«ц Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я»ЇЯ«ЋЯ«│Я«┐Я«▓Я»Ї Я«ЄЯ«еЯ»ЇЯ«ц Я«ЅЯ«фЯ»ЇЯ«фЯ»ЂЯ«ЋЯ«│Я»Ї Я««Я»ЂЯ«┤Я»ЂЯ««Я»ѕЯ«»Я«ЙЯ«Ћ Я«фЯ«┐Я«░Я«┐Я«ЋЯ»ѕЯ«»Я«ЪЯ»ѕЯ«еЯ»ЇЯ«цЯ»Ђ Я«ЁЯ«хЯ«▒Я»ЇЯ«▒Я«┐Я«ЕЯ»Ї Я«ЁЯ«»Я«ЕЯ«┐Я«ЋЯ«│Я»ѕ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ«ЋЯ«┐Я«ЕЯ»ЇЯ«▒Я«Е. Я«ЄЯ«хЯ»ЇЯ«хЯ«ЙЯ«▒Я»Ђ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«Е Я«ЁЯ«»Я«ЕЯ«┐Я«ЋЯ«│Я»Ї Я«еЯ»ђЯ«░Я»ЄЯ«▒Я»ЇЯ«▒Я««Я»Ї Я«ЁЯ«ЪЯ»ѕЯ«ЋЯ«┐Я«ЕЯ»ЇЯ«▒Я«Е. Я«џЯ«┐Я«▓ Я«ЋЯ»ЂЯ«▒Я«┐Я«фЯ»ЇЯ«фЯ«┐Я«ЪЯ»ЇЯ«Ъ Я«еЯ»ЄЯ«░Я»ЇЯ«хЯ»ЂЯ«ЋЯ«│Я«┐Я«▓Я»Ї, Я«еЯ»ЄЯ«░Я«»Я«ЕЯ«┐, Я«јЯ«цЯ«┐Я«░Я«»Я«ЕЯ«┐ Я«ЁЯ«▓Я»ЇЯ«▓Я«цЯ»Ђ Я«ЄЯ«░Я«БЯ»ЇЯ«ЪЯ»ЂЯ««Я»Ї Я«еЯ»ђЯ«░Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«ЋЯ«┐Я«ЕЯ»ЇЯ«▒Я«Е. Я«ЄЯ«еЯ»ЇЯ«ц Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я«ЙЯ«ЕЯ«цЯ»Ђ Я«ЅЯ«фЯ»ЇЯ«фЯ»Ђ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я«јЯ«ЕЯ»ЇЯ«▒Я«┤Я»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«ЁЯ«цЯ«ЙЯ«хЯ«цЯ»Ђ Я«ЅЯ«фЯ»ЇЯ«фЯ»Ђ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ»Ђ Я«еЯ«ЪЯ»ЂЯ«еЯ«┐Я«▓Я»ѕЯ«»Я«ЙЯ«ЋЯ»ЇЯ«ЋЯ«▓Я»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я«┐Я«ЕЯ»Ї Я««Я«▒Я»ЂЯ«цЯ«▓Я»ѕ Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї.
Я«хЯ«▓Я«┐Я««Я»ѕЯ««Я«┐Я«ЋЯ»Ђ Я«ЁЯ««Я«┐Я«▓Я««Я»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«хЯ«▓Я«┐Я««Я»ѕЯ««Я«┐Я«ЋЯ»Ђ Я«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЅЯ«фЯ»ЇЯ«фЯ»ЂЯ«ЋЯ«│Я»ѕ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї
NaOH Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«еЯ»ѕЯ«ЪЯ»ЇЯ«░Я«┐Я«ЋЯ»Ї Я«ЁЯ««Я«┐Я«▓Я««Я»Ї Я«єЯ«ЋЯ«┐Я«»Я«хЯ«▒Я»ЇЯ«▒Я«┐Я«▒Я»ЇЯ«ЋЯ«┐Я«ЪЯ»ѕЯ«»Я»Є Я«хЯ«┐Я«ЕЯ»ѕ Я«еЯ«┐Я«ЋЯ«┤Я»ЇЯ«еЯ»ЇЯ«цЯ»Ђ Я«џЯ»ІЯ«ЪЯ«┐Я«»Я««Я»Ї Я«еЯ»ѕЯ«ЪЯ»ЇЯ«░Я»ЄЯ«ЪЯ»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«еЯ»ђЯ«░Я»Ї Я«єЯ«ЋЯ«┐Я«»Я«хЯ»ѕ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЂЯ««Я»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я»ѕ Я«ЋЯ«░Я»ЂЯ«цЯ»ЂЯ«хЯ»ІЯ««Я»Ї.
NaOH(aq) (Я«еЯ»ђЯ«░Я»ЇЯ«ЋЯ»Ї Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я»Ї) + HNO3(aq) Рєњ NaNO3 (aq) + H2O (Я«еЯ»ђЯ«░Я»ЇЯ««Я««Я»Ї)
NaNO3 Я«ЅЯ«фЯ»ЇЯ«фЯ«ЙЯ«ЕЯ«цЯ»Ђ Я«еЯ»ђЯ«░Я«┐Я«▓Я»Ї Я««Я»ЂЯ«┤Я»ЂЯ««Я»ѕЯ«»Я«ЙЯ«Ћ Я«фЯ«┐Я«░Я«┐Я«ЋЯ»ѕЯ«»Я«ЪЯ»ѕЯ«еЯ»ЇЯ«цЯ»Ђ Na+ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї NO3- Я«ЁЯ«»Я«ЕЯ«┐Я«ЋЯ«│Я»ѕ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ«ЋЯ«┐Я«ЕЯ»ЇЯ«▒Я«Е.
NaNO3 (aq) Рєњ Na+ (aq) + NO3- (aq)
Я«еЯ»ђЯ«░Я«ЙЯ«ЕЯ«цЯ»Ђ Я««Я«┐Я«ЋЯ«ЋЯ»Ї Я«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«цЯ«│Я«хЯ»Є Я«фЯ«┐Я«░Я«┐Я«ЋЯ»ѕЯ«»Я«ЪЯ»ѕЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ
H2O (1) Рєћ H+(aq) + OH-(aq)
[H+ ] = [OH- ] Я«јЯ«ЕЯ«хЯ»Є, Я«еЯ»ђЯ«░Я»Ї Я«еЯ«ЪЯ»ЂЯ«еЯ«┐Я«▓Я»ѕЯ«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ««Я»ѕ Я«хЯ«ЙЯ«»Я»ЇЯ«еЯ»ЇЯ«цЯ«цЯ»Ђ
NO3- Я«ЁЯ«»Я«ЕЯ«┐Я«»Я«ЙЯ«ЕЯ«цЯ»Ђ, HNO3 Я«хЯ«▓Я«┐Я««Я»ѕЯ««Я«┐Я«ЋЯ»Ђ Я«ЁЯ««Я«┐Я«▓Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЄЯ«БЯ»ѕЯ«ЋЯ«ЙЯ«░Я««Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї. Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї, Я«ЄЯ«цЯ»Ђ H+ Я«ЁЯ«»Я«ЕЯ«┐Я«»Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«»Я»ЂЯ««Я»Ї Я«цЯ«┐Я«▒Я«ЕЯ«▒Я»ЇЯ«▒Я«цЯ»Ђ.
Я«ЄЯ«цЯ»ЄЯ«фЯ»ІЯ«▓, Na+ Я«ЁЯ«»Я«ЕЯ«┐Я«»Я«ЙЯ«ЕЯ«цЯ»Ђ, NaOH Я«јЯ«ЕЯ»ЂЯ««Я»Ї Я«хЯ«▓Я«┐Я««Я»ѕЯ««Я«┐Я«ЋЯ»Ђ Я«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЄЯ«БЯ»ѕ Я«ЁЯ««Я«┐Я«▓Я««Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї. Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї, Я«ЄЯ«цЯ»Ђ OH- Я«ЁЯ«»Я«ЕЯ«┐Я«»Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«»Я»ЂЯ««Я»Ї Я«цЯ«┐Я«▒Я«ЕЯ«▒Я»ЇЯ«▒Я«цЯ»Ђ.
Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я«еЯ«┐Я«ЋЯ«┤Я«хЯ«┐Я«▓Я»ЇЯ«▓Я»ѕ Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ»Є Я«ЄЯ«цЯ«ЕЯ»Ї Я«фЯ»іЯ«░Я»ЂЯ«│Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї. Я«ЄЯ«цЯ»ЇЯ«цЯ«ЋЯ»ѕЯ«» Я«еЯ»ЄЯ«░Я»ЇЯ«хЯ»ЂЯ«ЋЯ«│Я«┐Я«▓Я»Ї [H+] = [OH-] Я«јЯ«ЕЯ«хЯ»Є Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«┐Я«ЕЯ»Ї pH Я«фЯ«░Я«ЙЯ««Я«░Я«┐Я«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я»Ї Я«еЯ«ЪЯ»ЂЯ«еЯ«┐Я«▓Я»ѕЯ«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ««Я»ѕ Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ«цЯ»Ђ.
Я«хЯ«▓Я«┐Я««Я»ѕЯ««Я«┐Я«ЋЯ»Ђ Я«ЋЯ«ЙЯ«░Я««Я»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«хЯ«▓Я«┐Я««Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«ЁЯ««Я«┐Я«▓Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЅЯ«фЯ»ЇЯ«фЯ»ЂЯ«ЋЯ«│Я»ѕ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї (Я«јЯ«цЯ«┐Я«░Я»Ї Я«ЁЯ«»Я«ЕЯ«┐Я«»Я«┐Я«ЕЯ»Ї Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«фЯ»ЇЯ«фЯ»Ђ)
Я«џЯ»ІЯ«ЪЯ«┐Я«»Я««Я»Ї Я«╣Я»ѕЯ«ЪЯ»ЇЯ«░Я«ЙЯ«ЋЯ»ЇЯ«џЯ»ѕЯ«ЪЯ»Ђ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЁЯ«џЯ«┐Я«ЪЯ»ЇЯ«ЪЯ«┐Я«ЋЯ»Ї Я«ЁЯ««Я«┐Я«▓Я««Я»Ї Я«єЯ«ЋЯ«┐Я«»Я«хЯ«▒Я»ЇЯ«▒Я«┐Я«▒Я»ЇЯ«ЋЯ«┐Я«ЪЯ»ѕЯ«»Я»Є Я«хЯ«┐Я«ЕЯ»ѕ Я«еЯ«┐Я«ЋЯ«┤Я»ЇЯ«еЯ»ЇЯ«цЯ»Ђ Я«џЯ»ІЯ«ЪЯ«┐Я«»Я««Я»Ї Я«ЁЯ«џЯ«┐Я«ЪЯ»ЇЯ«ЪЯ»ЄЯ«ЪЯ»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«еЯ»ђЯ«░Я»Ї Я«єЯ«ЋЯ«┐Я«»Я«хЯ»ѕ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЂЯ««Я»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я»ѕ Я«ЋЯ«░Я»ЂЯ«цЯ»ЂЯ«хЯ»ІЯ««Я»Ї.
NaOH (aq) + CH3COOH(aq) Рєћ CH3COONa(aq) + H2O (l)
Я«еЯ»ђЯ«░Я»ЇЯ«ЋЯ»ЇЯ«ЋЯ«░Я»ѕЯ«џЯ«▓Я»ЇЯ«ЋЯ«│Я«┐Я«▓Я»Ї, Я«ЋЯ»ђЯ«┤Я»Є Я«ЋЯ»ЂЯ«▒Я«┐Я«фЯ»ЇЯ«фЯ«┐Я«ЪЯ»ЇЯ«ЪЯ»ЂЯ«│Я»ЇЯ«│Я«хЯ«ЙЯ«▒Я»Ђ CH3COONa Я««Я»ЂЯ«┤Я»ЂЯ««Я»ѕЯ«»Я«ЙЯ«Ћ Я«фЯ«┐Я«░Я«┐Я«ЋЯ»ѕЯ«»Я«ЪЯ»ѕЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
CH3COONa(aq) Рєњ CH3COO- (aq) + Na+ (aq)
CH3COO- Я«ЁЯ«»Я«ЕЯ«┐Я«»Я«ЙЯ«ЕЯ«цЯ»Ђ, CH3COOH Я«јЯ«ЕЯ»ЂЯ««Я»Ї Я«хЯ«▓Я«┐Я««Я»ѕЯ«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«ЁЯ««Я«┐Я«▓Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЄЯ«БЯ»ѕ Я«ЋЯ«ЙЯ«░Я««Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї. Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї, Я«ЄЯ«цЯ»Ђ Я«еЯ»ђЯ«░Я«┐Я«▓Я«┐Я«░Я»ЂЯ«еЯ»ЇЯ«цЯ»Ђ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ H+ Я«ЁЯ«»Я«ЕЯ«┐Я«»Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«еЯ»ЇЯ«цЯ»Ђ Я«ЁЯ«»Я«ЕЯ«┐Я«»Я»ЂЯ«▒Я«Й Я«ЁЯ««Я«┐Я«▓Я«цЯ»ЇЯ«цЯ»ѕ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«цЯ«┐Я«▒Я«ЕЯ»ѕЯ«фЯ»Ї Я«фЯ»єЯ«▒Я»ЇЯ«▒Я»ЂЯ«│Я»ЇЯ«│Я«цЯ»Ђ.
Na+ Я«ЁЯ«»Я«ЕЯ«┐Я«»Я«ЙЯ«ЕЯ«цЯ»Ђ OH- Я«ЁЯ«»Я«ЕЯ«┐Я«ЋЯ«│Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«»Я»ЂЯ««Я»Ї Я«цЯ«┐Я«▒Я«ЕЯ«▒Я»ЇЯ«▒Я«цЯ»Ђ.
CH3COO- (aq) + H2O(1) Рєћ CH3COOH (aq) + OH- (aq) Я«јЯ«ЕЯ«хЯ»Є [OH-] > [H+], Я«ЄЯ«цЯ»ЇЯ«цЯ«ЋЯ»ѕЯ«» Я«еЯ»ЄЯ«░Я»ЇЯ«хЯ»ЂЯ«ЋЯ«│Я«┐Я«▓Я»Ї, Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я«┐Я«ЕЯ»Ї Я«ЋЯ«ЙЯ«░Я«БЯ««Я«ЙЯ«Ћ Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«ЙЯ«ЕЯ«цЯ»Ђ Я«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ««Я»ѕЯ«»Я»ѕ Я«фЯ»єЯ«▒Я»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ, Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«┐Я«ЕЯ»Ї pH Я««Я«цЯ«┐Я«фЯ»ЇЯ«фЯ»Ђ 7 Я«љЯ«хЯ«┐Я«Ъ Я«ЁЯ«цЯ«┐Я«ЋЯ««Я«ЙЯ«Ћ Я«ЅЯ«│Я»ЇЯ«│Я«цЯ»Ђ. Я«ЄЯ«еЯ»ЇЯ«ц Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«ЋЯ»ЇЯ«ЋЯ«ЙЯ«Е Я«џЯ««Я«еЯ«┐Я«▓Я»ѕ Я««Я«ЙЯ«▒Я«┐Я«▓Я«┐Я«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї (Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я««Я«ЙЯ«▒Я«┐Я«▓Я«┐) Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЁЯ««Я«┐Я«▓Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«фЯ«┐Я«░Я«┐Я«ЋЯ»ѕ Я««Я«ЙЯ«▒Я«┐Я«▓Я«┐Я«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«ЄЯ«ЪЯ»ѕЯ«»Я»Є Я«ЅЯ«│Я»ЇЯ«│ Я«цЯ»іЯ«ЪЯ«░Я»ЇЯ«фЯ»ѕ Я«ЋЯ«ЙЯ«БЯ»ЇЯ«фЯ»ІЯ««Я»Ї.
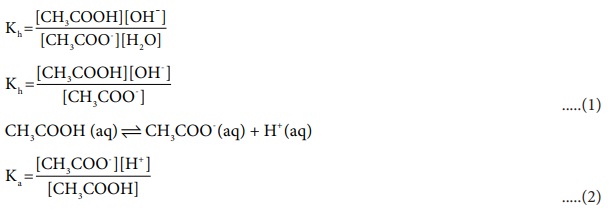
(1) ├Ќ (2)
РЄњ Kh, Ka = [H+] [OH-]
[H+] [OH-] = Kw Я«јЯ«Е Я«еЯ«ЙЯ««Я»Ї Я«ЁЯ«▒Я«┐Я«хЯ»ІЯ««Я»Ї
Kh, Ka = Kw
Я«єЯ«ИЯ»ЇЯ«хЯ«ЙЯ«▓Я»ЇЯ«ЪЯ»Ї Я«еЯ»ђЯ«░Я»ЇЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я«хЯ«┐Я«цЯ«┐Я«»Я«┐Я«▓Я»Ї Я«фЯ»єЯ«▒Я«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«ЪЯ«цЯ»ѕЯ«фЯ»Ї Я«фЯ»ІЯ«▓Я«хЯ»Є, Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я«хЯ»ђЯ«цЯ««Я»Ї (h) Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЅЯ«фЯ»ЇЯ«фЯ«┐Я«ЕЯ»Ї Я«џЯ»єЯ«▒Я«┐Я«хЯ»Ђ (C) Я«єЯ«ЋЯ«┐Я«»Я«хЯ«▒Я»ЇЯ«▒Я«┐Я«ЕЯ«ЙЯ«▓Я»Ї Kh Я««Я«цЯ«┐Я«фЯ»ЇЯ«фЯ»ѕ Я«хЯ«░Я»ЂЯ«хЯ«┐Я«ЋЯ»ЇЯ«Ћ Я««Я»ЂЯ«ЪЯ«┐Я«»Я»ЂЯ««Я»Ї. Kh = h2C. Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї
i.e [OH-] = РѕџKaC
Ka Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я««Я«┐Я«ЕЯ»ЇЯ«фЯ«ЋЯ»ЂЯ«│Я«┐Я«»Я«┐Я«ЕЯ»Ї Я«џЯ»єЯ«▒Я«┐Я«хЯ»ЂЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«ЁЯ«ЪЯ«┐Я«фЯ»ЇЯ«фЯ«ЪЯ»ѕЯ«»Я«┐Я«▓Я»Ї Я«ЅЯ«фЯ»ЇЯ«фЯ»Ђ Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«┐Я«ЕЯ»Ї pH.
pH + pOH = 14
pH = 14 - p OH = 14 - {- log [OH-]}
= 14+ log [OH-]
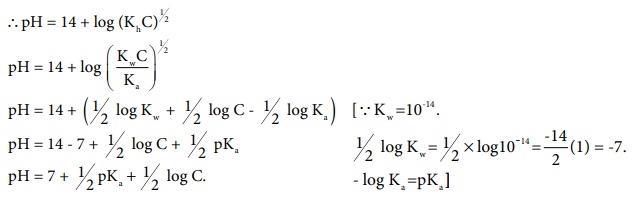
Я«хЯ«▓Я«┐Я««Я»ѕЯ««Я«┐Я«ЋЯ»Ђ Я«ЁЯ««Я«┐Я«▓Я««Я»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«хЯ«▓Я«┐Я««Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЅЯ«фЯ»ЇЯ«фЯ»ЂЯ«ЋЯ«│Я»ѕ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї. (Я«еЯ»ЄЯ«░Я»Ї Я«ЁЯ«»Я«ЕЯ«┐Я«»Я«┐Я«ЕЯ»Ї Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«фЯ»ЇЯ«фЯ»Ђ)
Я«њЯ«░Я»Ђ Я«хЯ«▓Я«┐Я««Я»ѕ Я««Я«┐Я«ЋЯ»Ђ Я«ЁЯ««Я«┐Я«▓Я««Я»Ї HCl Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«њЯ«░Я»Ђ Я«хЯ«▓Я«┐Я««Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«ЋЯ«ЙЯ«░Я««Я»Ї NH4OH Я«єЯ«ЋЯ«┐Я«»Я«хЯ»ѕ Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«еЯ»ЇЯ«цЯ»Ђ NH4Cl Я«ЅЯ«фЯ»ЇЯ«фЯ»Ђ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«еЯ»ђЯ«░Я»Ї Я«єЯ«ЋЯ«┐Я«»Я«хЯ»ѕ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЂЯ««Я»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я»ѕ Я«ЋЯ«░Я»ЂЯ«цЯ»ЂЯ«хЯ»ІЯ««Я»Ї.
HCl (aq) + NH4OH (aq) Рєћ NH4C1(aq)+H2O(l)
NH4Cl (aq) Рєњ NH4+ + Cl- (aq)
NH4+ Я«ЁЯ«»Я«ЕЯ«┐Я«»Я«ЙЯ«ЕЯ«цЯ»Ђ, NH4OH Я«јЯ«ЕЯ»ЂЯ««Я»Ї Я«хЯ«▓Я«┐Я««Я»ѕЯ«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЄЯ«БЯ»ѕ Я«ЁЯ««Я«┐Я«▓Я««Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї. Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї, Я«ЄЯ«цЯ»Ђ Я«еЯ»ђЯ«░Я«┐Я«▓Я«┐Я«░Я»ЂЯ«еЯ»ЇЯ«цЯ»Ђ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ OH- Я«ЁЯ«»Я«ЕЯ«┐Я«»Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«еЯ»ЇЯ«цЯ»Ђ Я«ЁЯ«»Я«ЕЯ«┐Я«»Я»ЂЯ«▒Я«Й NH4OH Я«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ»ѕ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«цЯ«┐Я«▒Я«ЕЯ»ѕЯ«фЯ»Ї Я«фЯ»єЯ«▒Я»ЇЯ«▒Я»ЂЯ«│Я»ЇЯ«│Я«цЯ»Ђ.
NH4+ (aq) + H2O(l) Рєћ NH4OH (aq) + H+ (aq)
Я«ЄЯ«цЯ»ЇЯ«цЯ«ЋЯ»ѕЯ«» Я«цЯ«┐Я«▒Я«ЕЯ»ѕ Cl- Я«ЁЯ«»Я«ЕЯ«┐ Я«фЯ»єЯ«▒Я«хЯ«┐Я«▓Я»ЇЯ«▓Я»ѕ , Я«јЯ«ЕЯ«хЯ»Є [H+] > [OH-]; Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«ЙЯ«ЕЯ«цЯ»Ђ Я«ЁЯ««Я«┐Я«▓Я«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ««Я»ѕЯ«»Я»ѕ Я«фЯ»єЯ«▒Я»ЇЯ«▒Я»ЂЯ«│Я»ЇЯ«│Я«цЯ»Ђ, Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї Я«ЁЯ«цЯ«ЕЯ»Ї pH Я««Я«цЯ«┐Я«фЯ»ЇЯ«фЯ»Ђ 7 Я«љЯ«хЯ«┐Я«Ъ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«хЯ«ЙЯ«Ћ Я«ЅЯ«│Я»ЇЯ«│Я«цЯ»Ђ.
Я«хЯ«▓Я«┐Я««Я»ѕЯ««Я«┐Я«ЋЯ»Ђ Я«ЋЯ«ЙЯ«░Я««Я»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«хЯ«▓Я«┐Я««Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«ЁЯ««Я«┐Я«▓Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЅЯ«фЯ»ЇЯ«фЯ»Ђ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я«┐Я«▓Я»Ї Я«хЯ«┐Я«хЯ«ЙЯ«цЯ«┐Я«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«ЪЯ«цЯ»ѕЯ«фЯ»Ї Я«фЯ»ІЯ«ЕЯ»ЇЯ«▒Я»Є, Я«ЄЯ«еЯ»ЇЯ«ц Я«еЯ»ЄЯ«░Я»ЇЯ«хЯ«┐Я«▓Я»ЂЯ««Я»Ї, Kh Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Kb Я«ЋЯ»ЇЯ«ЋЯ»Ђ Я«ЄЯ«ЪЯ»ѕЯ«»Я»ЄЯ«»Я»ЂЯ«│Я»ЇЯ«│ Я«цЯ»іЯ«ЪЯ«░Я»ЇЯ«фЯ»ѕ Я«еЯ««Я»ЇЯ««Я«ЙЯ«▓Я»Ї Я«еЯ«┐Я«▒Я»ЂЯ«х Я««Я»ЂЯ«ЪЯ«┐Я«»Я»ЂЯ««Я»Ї.
Kh . Kb = Kw
Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я«хЯ»ђЯ«цЯ««Я»Ї (h) Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЅЯ«фЯ»ЇЯ«фЯ«┐Я«ЕЯ»Ї Я«џЯ»єЯ«▒Я«┐Я«хЯ»Ђ Я«єЯ«ЋЯ«┐Я«»Я«хЯ«▒Я»ЇЯ«▒Я«┐Я«ЕЯ»Ї Я«ЁЯ«ЪЯ«┐Я«фЯ»ЇЯ«фЯ«ЪЯ»ѕЯ«»Я«┐Я«▓Я»Ї Kh Я««Я«цЯ«┐Я«фЯ»ЇЯ«фЯ»ѕ Я«еЯ«ЙЯ««Я»Ї Я«ЋЯ«БЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«ЪЯ»ЂЯ«хЯ»ІЯ««Я»Ї.
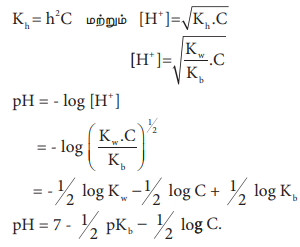
Я«хЯ«▓Я«┐Я««Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«ЁЯ««Я«┐Я«▓Я««Я»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«хЯ«▓Я«┐Я««Я»ѕ Я«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЅЯ«фЯ»ЇЯ«фЯ»ЂЯ«ЋЯ«│Я»ѕ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї. (Я«јЯ«цЯ«┐Я«░Я»Ї Я«ЁЯ«»Я«ЕЯ«┐ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«еЯ»ЄЯ«░Я»Ї Я«ЁЯ«»Я«ЕЯ«┐Я«»Я«┐Я«ЕЯ»Ї Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«фЯ»ЇЯ«фЯ»Ђ)
Я«ЁЯ««Я»ЇЯ««Я»ІЯ«ЕЯ«┐Я«»Я««Я»Ї Я«ЁЯ«џЯ«┐Я«ЪЯ»ЇЯ«ЪЯ»ЄЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«ЕЯ»Ї Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»ѕ Я«ЋЯ«░Я»ЂЯ«цЯ»ЂЯ«хЯ»ІЯ««Я»Ї.
CH3COONH4 (aq) Рєњ CH3COO- (aq) + NH4 + (aq)
Я«ЄЯ«еЯ»ЇЯ«ц Я«еЯ»ЄЯ«░Я»ЇЯ«хЯ«┐Я«▓Я»Ї, Я«еЯ»ЄЯ«░Я«»Я«ЕЯ«┐ (NH4 +) Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«јЯ«цЯ«┐Я«░Я«»Я«ЕЯ«┐ (CH3COO-) Я«ЄЯ«░Я«БЯ»ЇЯ«ЪЯ»ЂЯ««Я»Є Я«еЯ»ђЯ«░Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«»Я»ЂЯ««Я»Ї Я«цЯ«┐Я«▒Я«ЕЯ»ѕЯ«фЯ»Ї Я«фЯ»єЯ«▒Я»ЇЯ«▒Я»ЂЯ«│Я»ЇЯ«│Я«Е.
CH3COO- + H2O Рєћ CH3COOH + OH-
NH4 + + H2O Рєћ NH4OH + H+
Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«┐Я«ЕЯ»Ї Я«цЯ«ЕЯ»ЇЯ««Я»ѕЯ«»Я«ЙЯ«ЕЯ«цЯ»Ђ Я«ЁЯ«цЯ«┐Я«▓Я»ЂЯ«│Я»ЇЯ«│ Я«ЁЯ««Я«┐Я«▓Я««Я»Ї (Я«ЁЯ«▓Я»ЇЯ«▓Я«цЯ»Ђ) Я«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«хЯ«▓Я«┐Я««Я»ѕЯ«»Я»ѕ Я«џЯ«ЙЯ«░Я»ЇЯ«еЯ»ЇЯ«цЯ»Ђ Я«ЁЯ««Я»ѕЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«ЁЯ«цЯ«ЙЯ«хЯ«цЯ»Ђ, Ka > Kb Я«јЯ«ЕЯ«┐Я«▓Я»Ї Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я»Ї Я«ЁЯ««Я«┐Я«▓Я«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ««Я»ѕ Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ«цЯ»Ђ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЁЯ«цЯ«ЕЯ»Ї pH < 7,
Ka < Kb Я«јЯ«ЕЯ«┐Я«▓Я»Ї Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я»Ї Я«ЋЯ«ЙЯ«░Я«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ««Я»ѕ Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ«цЯ»Ђ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЁЯ«цЯ«ЕЯ»Ї pH > 7, Ka = Kb Я«јЯ«ЕЯ«┐Я«▓Я»Ї Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я»Ї Я«еЯ«ЪЯ»ЂЯ«еЯ«┐Я«▓Я»ѕЯ«цЯ»Ї Я«цЯ«ЕЯ»ЇЯ««Я»ѕ Я«хЯ«ЙЯ«»Я»ЇЯ«еЯ»ЇЯ«цЯ«цЯ»Ђ. Я«фЯ«┐Я«░Я«┐Я«ЋЯ»ѕ Я««Я«ЙЯ«▒Я«┐Я«▓Я«┐Я«ЋЯ«│Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї (Ka, Kb) Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я««Я«ЙЯ«▒Я«┐Я«▓Я«┐Я«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«ЄЯ«ЪЯ»ѕЯ«»Я»Є Я«ЅЯ«│Я»ЇЯ«│ Я«цЯ»іЯ«ЪЯ«░Я»ЇЯ«фЯ»ѕ Я«фЯ«┐Я«ЕЯ»ЇЯ«хЯ«░Я»ЂЯ««Я»Ї Я«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»Ђ Я«цЯ«░Я»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
Ka . Kb . Kh = Kw
Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«┐Я«ЕЯ»Ї pH Я««Я«цЯ«┐Я«фЯ»ЇЯ«фЯ»Ђ
Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«┐Я«ЕЯ»Ї pH Я««Я«цЯ«┐Я«фЯ»ЇЯ«фЯ»ѕ Я«фЯ«┐Я«ЕЯ»ЇЯ«хЯ«░Я»ЂЯ««Я»Ї Я«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ»ѕ Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐ Я«ЋЯ«БЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«Ъ Я««Я»ЂЯ«ЪЯ«┐Я«»Я»ЂЯ««Я»Ї.
pH =7+ 1/2 pKa -1/2 PKb.
Я«јЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ»Ђ 8.8
0.1M Я«цЯ«┐Я«▒Я«ЕЯ»ЂЯ«ЪЯ»ѕЯ«» CH3COONa Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«┐Я«ЕЯ»Ї i) Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я«хЯ»ђЯ«цЯ««Я»Ї, ii) Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я««Я«ЙЯ«▒Я«┐Я«▓Я«┐, Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї iii) pH Я«єЯ«ЋЯ«┐Я«»Я«хЯ«▒Я»ЇЯ«▒Я»ѕЯ«ЋЯ»Ї Я«ЋЯ«БЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«ЪЯ»ЂЯ«Ћ. (CH3COOH Я«ЁЯ««Я«┐Я«▓Я«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї pKa Я««Я«цЯ«┐Я«фЯ»ЇЯ«фЯ»Ђ 4.74).
Я«цЯ»ђЯ«░Я»ЇЯ«хЯ»Ђ : (a) CH3COONa Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ»Ђ, Я«њЯ«░Я»Ђ Я«хЯ«▓Я«┐Я««Я»ѕЯ«ЋЯ»ЂЯ«▒Я»ѕЯ«еЯ»ЇЯ«ц Я«ЁЯ««Я«┐Я«▓Я««Я»Ї (CH3COOH) Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«њЯ«░Я»Ђ Я«хЯ«▓Я«┐Я««Я»ѕЯ««Я«┐Я«ЋЯ»Ђ Я«ЋЯ«ЙЯ«░Я««Я»Ї (NaOH) Я«єЯ«ЋЯ«┐Я«»Я«хЯ«▒Я»ЇЯ«▒Я«┐Я«ЕЯ»Ї Я«ЅЯ«фЯ»ЇЯ«фЯ«ЙЯ«ЋЯ»ЂЯ««Я»Ї.Я«јЯ«ЕЯ«хЯ»Є, Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я«┐Я«ЕЯ»Ї Я«ЋЯ«ЙЯ«░Я«БЯ««Я«ЙЯ«Ћ Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«ЙЯ«ЕЯ«цЯ»Ђ Я«ЋЯ«ЙЯ«░Я«цЯ»Ї Я«цЯ«ЕЯ»ЇЯ««Я»ѕЯ«»Я»ѕ Я«фЯ»єЯ«▒Я»ЇЯ«▒Я»ЂЯ«│Я»ЇЯ«│Я«цЯ»Ђ.
CH3COO- (aq) + H2O (aq) Рєћ CH3COOH (aq) + OH+ (aq)
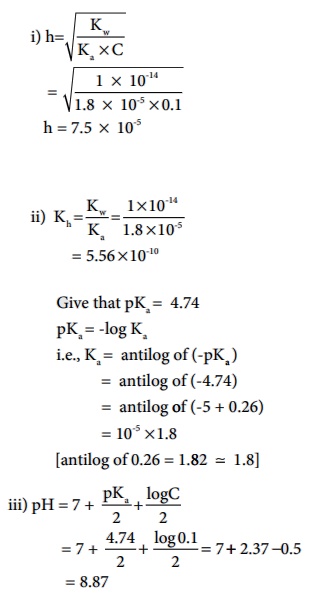
Я«цЯ«ЕЯ»ЇЯ««Я«цЯ«┐Я«фЯ»ЇЯ«фЯ»ђЯ«ЪЯ»Ђ - 10
HCO3- Я«ЁЯ«»Я«ЕЯ«┐Я«»Я«┐Я«ЕЯ»Ї pKa Я««Я«цЯ«┐Я«фЯ»ЇЯ«фЯ»Ђ 10.26 Я«јЯ«ЕЯ«┐Я«▓Я»Ї, 0.05M Я«цЯ«┐Я«▒Я«ЕЯ»ЂЯ«ЪЯ»ѕЯ«» Я«џЯ»ІЯ«ЪЯ«┐Я«»Я««Я»Ї Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»ЄЯ«ЪЯ»Ї Я«ЋЯ«░Я»ѕЯ«џЯ«▓Я«┐Я«ЕЯ»Ї i) Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я««Я«ЙЯ«▒Я«┐Я«▓Я«┐, ii) Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»Ї Я«хЯ»ђЯ«цЯ««Я»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї iii) pH Я«єЯ«ЋЯ«┐Я«»Я«хЯ«▒Я»ЇЯ«▒Я»ѕЯ«ЋЯ»Ї Я«ЋЯ«БЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«ЪЯ»ЂЯ«Ћ.