11Я«хЯ«цЯ»Ђ Я«ЄЯ«»Я«▒Я»ЇЯ«фЯ«┐Я«»Я«▓Я»Ї : Я«ЁЯ«▓Я«ЋЯ»Ђ 8 : Я«хЯ»єЯ«фЯ»ЇЯ«фЯ««Я»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЄЯ«»Я«ЋЯ»ЇЯ«ЋЯ«хЯ«┐Я«»Я«▓Я»ЂЯ««Я»Ї
Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї
Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї
Я«ЋЯ»іЯ«ЪЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ Я«ЁЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ«┐Я«ЕЯ»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї Я«ЁЯ«хЯ»ЇЯ«хЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ«┐Я«ЕЯ»Ї Я«ЋЯ«ЪЯ»ЇЯ«ЪЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я««Я»ѓЯ«▓Я«ЋЯ»ЇЯ«ЋЯ»ѓЯ«▒Я»ЂЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«цЯ«ЕЯ»ЇЯ««Я»ѕЯ«»Я»ѕЯ«ЋЯ»Ї Я«ЋЯ«БЯ»ЇЯ«ЪЯ«▒Я«┐Я«хЯ«цЯ«┐Я«▓Я»Ї Я««Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«»Я«фЯ»Ї Я«фЯ«ЎЯ»ЇЯ«ЋЯ«ЙЯ«▒Я»ЇЯ«▒Я»ЂЯ«ЋЯ«┐Я«ЕЯ»ЇЯ«▒Я«цЯ»Ђ. Я«цЯ«┐Я«ЪЯ«фЯ»ЇЯ«фЯ»іЯ«░Я»ЂЯ«│Я»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«цЯ«┐Я«░Я«хЯ«ЎЯ»ЇЯ«ЋЯ«│Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ»Ђ Я««Я«ЙЯ«▒Я«ЙЯ«Ћ Я«хЯ«ЙЯ«»Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ«│Я»Ї Я«ЄЯ«░Я«БЯ»ЇЯ«ЪЯ»Ђ Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»ЇЯ«ЋЯ«│Я»ѕЯ«фЯ»Ї Я«фЯ»єЯ«▒Я»ЇЯ«▒Я»ЂЯ«│Я»ЇЯ«│Я«Е. Я«ЁЯ«хЯ»ѕ, Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ««Я»Ї Я««Я«ЙЯ«▒Я«ЙЯ«цЯ»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї (Sp) Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї Я««Я«ЙЯ«▒Я«ЙЯ«цЯ»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї (Sv)
Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї
Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ««Я»Ї Я««Я«ЙЯ«▒Я«ЙЯ«цЯ»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї (Sp)
Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ««Я»Ї Я««Я«ЙЯ«▒Я«Й Я«еЯ«┐Я«▓Я»ѕЯ«»Я«┐Я«▓Я»Ї 1 kg Я«еЯ«┐Я«▒Я»ѕЯ«»Я»ЂЯ«ЪЯ»ѕЯ«» Я«фЯ»іЯ«░Я»ЂЯ«│Я«┐Я«ЕЯ»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕЯ«»Я»ѕ 1 K Я«ЁЯ«▓Я»ЇЯ«▓Я«цЯ»Ђ 1┬░C Я«ЅЯ«»Я«░Я»ЇЯ«цЯ»ЇЯ«цЯ«цЯ»Ї Я«цЯ»ЄЯ«хЯ»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЁЯ«│Я«хЯ»Ђ Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ««Я»Ї Я««Я«ЙЯ«▒Я«ЙЯ«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї Я«јЯ«Е Я«ЁЯ«┤Я»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї. Я«ЁЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ«┐Я«ЕЯ»ѕ Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ»ЂЯ««Я»ЇЯ«фЯ»ІЯ«цЯ»Ђ Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«▒Я»ЇЯ«ЋЯ»Ђ Я«хЯ»єЯ«фЯ»ЇЯ«фЯ««Я»Ї Я«ЁЯ«│Я«┐Я«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«фЯ«ЪЯ««Я»Ї 8.23 Я«ЄЯ«▓Я»Ї Я«ЋЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«»Я»ЂЯ«│Я»ЇЯ«│Я«хЯ«ЙЯ«▒Я»Ђ Я««Я«ЙЯ«▒Я«Й Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ«цЯ»ЇЯ«цЯ«┐Я«▓Я»Ї Я«хЯ«ЙЯ«»Я»Ђ Я«хЯ«┐Я«░Я«┐Я«хЯ«ЪЯ»ѕЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
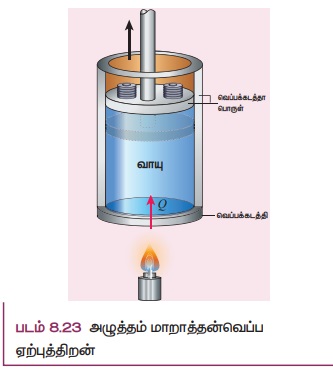
Я«ЄЯ«еЯ»ЇЯ«еЯ«┐Я«ЋЯ«┤Я»ЇЯ«хЯ«┐Я«▓Я»Ї Я«ЋЯ»іЯ«ЪЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«њЯ«░Я»Ђ Я«фЯ«ЋЯ»ЂЯ«цЯ«┐ Я«хЯ»ЄЯ«▓Я»ѕ Я«џЯ»єЯ«»Я»ЇЯ«» (Я«хЯ«┐Я«░Я«┐Я«хЯ«ЪЯ»ѕЯ«») Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї Я««Я»ђЯ«цЯ««Я»Ї Я«ЅЯ«│Я»ЇЯ«│ Я«фЯ«ЋЯ»ЂЯ«цЯ«┐ Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«ЁЯ«Ћ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ѕ Я«ЁЯ«цЯ«┐Я«ЋЯ«░Я«┐Я«фЯ»ЇЯ«фЯ«цЯ«▒Я»ЇЯ«ЋЯ»ЂЯ«фЯ»Ї Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї Я««Я«ЙЯ«▒Я«ЙЯ«цЯ»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї (SV)
Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї Я««Я«ЙЯ«▒Я«ЙЯ«еЯ«┐Я«▓Я»ѕЯ«»Я«┐Я«▓Я»Ї 1kg Я«еЯ«┐Я«▒Я»ѕЯ«»Я»ЂЯ«ЪЯ»ѕЯ«» Я«фЯ»іЯ«░Я»ЂЯ«│Я«┐Я«ЕЯ»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕЯ«»Я»ѕ 1 K Я«ЁЯ«▓Я»ЇЯ«▓Я«цЯ»Ђ 1┬░C Я«ЅЯ«»Я«░Я»ЇЯ«цЯ»ЇЯ«цЯ«цЯ»Ї Я«цЯ»ЄЯ«хЯ»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЁЯ«│Я«хЯ»Ђ, Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї Я««Я«ЙЯ«▒Я«Й Я«цЯ«ЕЯ»Ї Я«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї Я«јЯ«ЕЯ»ЇЯ«▒Я»Ђ Я«ЁЯ«┤Я»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї. Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї Я««Я«ЙЯ«▒Я«ЙЯ«ц Я«еЯ«┐Я«▓Я»ѕЯ«»Я«┐Я«▓Я»Ї Я«ЋЯ»іЯ«ЪЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ««Я»Ї Я«ЁЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ«┐Я«ЕЯ»Ї Я«ЁЯ«Ћ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»Ї Я«ЁЯ«цЯ«┐Я«ЋЯ«░Я«┐Я«фЯ»ЇЯ«фЯ«цЯ«▒Я»ЇЯ«ЋЯ»Ђ Я««Я«ЪЯ»ЇЯ«ЪЯ»ЂЯ««Я»Є Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«фЯ«ЪЯ««Я»Ї 8.24 Я«ЄЯ«▓Я»Ї Я«ЋЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ«┐Я«»Я»ЂЯ«│Я»ЇЯ«│Я«хЯ«ЙЯ«▒Я»Ђ Я«јЯ«хЯ»ЇЯ«хЯ«┐Я«ц Я«хЯ»ЄЯ«▓Я»ѕЯ«»Я»ЂЯ««Я»Ї Я«џЯ»єЯ«»Я»ЇЯ«»Я«фЯ»ЇЯ«фЯ«ЪЯ«ЙЯ«цЯ»Ђ.
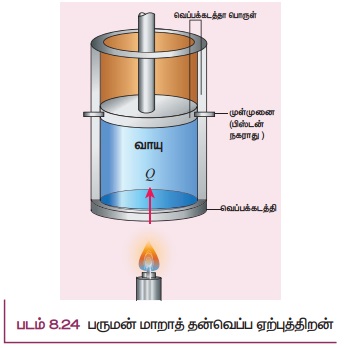
Я««Я«ЙЯ«▒Я«Й Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ«цЯ»ЇЯ«цЯ«┐Я«▓Я»Ї Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕЯ«»Я»ѕ Я«ЅЯ«»Я«░Я»ЇЯ«цЯ»ЇЯ«цЯ»ЂЯ«хЯ«цЯ«▒Я»ЇЯ«ЋЯ»ЂЯ«цЯ»Ї Я«цЯ»ЄЯ«хЯ»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«цЯ»ЇЯ«цЯ»ѕ Я«хЯ«┐Я«Ъ, Я««Я«ЙЯ«▒Я«Й Я«фЯ«░Я»ЂЯ««Я«ЕЯ«┐Я«▓Я»Ї Я«ЅЯ«│Я»ЇЯ«│ Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕЯ«»Я»ѕ Я«ЅЯ«»Я«░Я»ЇЯ«цЯ»ЇЯ«цЯ»ЂЯ«хЯ«цЯ«▒Я»ЇЯ«ЋЯ»ЂЯ«цЯ»Ї Я«цЯ»ЄЯ«хЯ»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ««Я»Ї Я«ЋЯ»ЂЯ«▒Я»ѕЯ«хЯ«ЙЯ«ЕЯ«цЯ»Ђ. Я«хЯ»ЄЯ«▒Я»ЂЯ«хЯ«ЋЯ»ѕЯ«»Я«┐Я«▓Я»Ї Я«ЋЯ»ѓЯ«▒Я»ЂЯ«хЯ»ІЯ««Я«ЙЯ«»Я«┐Я«ЕЯ»Ї Sp Я«јЯ«фЯ»ЇЯ«фЯ»ІЯ«цЯ»ЂЯ««Я»Ї Sv Я«љ Я«хЯ«┐Я«Ъ Я«ЁЯ«цЯ«┐Я«ЋЯ««Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї.
Я««Я»ІЯ«▓Я«ЙЯ«░Я»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»ЇЯ«ЋЯ«│Я»Ї
Я«џЯ«┐Я«▓ Я«еЯ»ЄЯ«░Я«ЎЯ»ЇЯ«ЋЯ«│Я«┐Я«▓Я»Ї Я««Я»ІЯ«▓Я«ЙЯ«░Я»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»ЇЯ«ЋЯ«│Я»ѕЯ«ЋЯ»Ї (Cp , Cv). Я«ЋЯ«БЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«ЪЯ»ЂЯ«хЯ«цЯ»Ђ, Я«еЯ««Я«ЋЯ»ЇЯ«ЋЯ»Ђ Я««Я«┐Я«ЋЯ«хЯ»ЂЯ««Я»Ї Я«фЯ«»Я«ЕЯ»ЂЯ«│Я»ЇЯ«│Я«цЯ«ЙЯ«Ћ Я«ЁЯ««Я»ѕЯ«»Я»ЂЯ««Я»Ї.
Я««Я«ЙЯ«▒Я«ЙЯ«фЯ»ЇЯ«фЯ«░Я»ЂЯ««Я«ЕЯ«┐Я«▓Я»Ї 1 Я««Я»ІЯ«▓Я»Ї Я«ЁЯ«│Я«хЯ»ЂЯ«│Я»ЇЯ«│ Я«фЯ»іЯ«░Я»ЂЯ«│Я«┐Я«ЕЯ»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕЯ«»Я»ѕ 1K Я«ЁЯ«▓Я»ЇЯ«▓Я«цЯ»Ђ 1┬░C Я«ЅЯ«»Я«░Я»ЇЯ«цЯ»ЇЯ«цЯ»ЂЯ«хЯ«цЯ«▒Я»ЇЯ«ЋЯ»ЂЯ«цЯ»Ї Я«цЯ»ЄЯ«хЯ»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЁЯ«│Я«хЯ»Є, Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї Я««Я«ЙЯ«▒Я«Й Я««Я»ІЯ«▓Я«ЙЯ«░Я»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї (Cv) Я«єЯ«ЋЯ»ЂЯ««Я»Ї. Я««Я«ЙЯ«▒Я«Й Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ«цЯ»ЇЯ«цЯ«┐Я«▓Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕЯ«»Я»ѕ Я«ЅЯ«»Я«░Я»ЇЯ«цЯ»ЇЯ«цЯ»ЂЯ«хЯ«цЯ«▒Я»ЇЯ«ЋЯ»ЂЯ«цЯ»Ї Я«цЯ»ЄЯ«хЯ»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЁЯ«│Я«хЯ»Ђ Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ««Я»Ї Я««Я«ЙЯ«▒Я«Й Я««Я»ІЯ«▓Я«ЙЯ«░Я»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї (CP).
Я««Я«ЙЯ«▒Я«ЙЯ«фЯ»ЇЯ«фЯ«░Я»ЂЯ««Я«ЕЯ«┐Я«▓Я»Ї ┬х Я««Я»ІЯ«▓Я»Ї Я«ЁЯ«│Я«хЯ»ЂЯ«│Я»ЇЯ«│ Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«▒Я»ЇЯ«ЋЯ»ЂЯ«ЋЯ»Ї Я«ЋЯ»іЯ«ЪЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«цЯ»ЇЯ«цЯ»ѕ Q Я«јЯ«ЕЯ»ЇЯ«▒Я»ЂЯ««Я»Ї, Я«ЁЯ«цЯ«ЕЯ«ЙЯ«▓Я»Ї Я«ЈЯ«▒Я»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕ Я«хЯ»ЄЯ«▒Я»ЂЯ«фЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ»ѕ ╬ћT Я«јЯ«ЕЯ«хЯ»ЂЯ««Я»Ї Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ«ЙЯ«▓Я»Ї

Я«јЯ«Е Я«јЯ«┤Я»ЂЯ«цЯ«▓Я«ЙЯ««Я»Ї.
Я«ЄЯ««Я»Ї Я««Я«ЙЯ«▒Я«ЙЯ«фЯ«░Я»ЂЯ««Я»Ї Я«еЯ«┐Я«ЋЯ«┤Я»ЇЯ«хЯ«┐Я«▒Я»ЇЯ«ЋЯ»Ђ Я«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЄЯ«»Я«ЋЯ»ЇЯ«ЋЯ«хЯ«┐Я«»Я«▓Я«┐Я«ЕЯ»Ї Я««Я»ЂЯ«цЯ«▓Я»Ї Я«хЯ«┐Я«цЯ«┐Я«»Я»ѕЯ«фЯ»Ї Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ«ЙЯ«▓Я»Ї (W = 0, Я«ЈЯ«ЕЯ»єЯ«ЕЯ«┐Я«▓Я»Ї dV = 0),

Я«јЯ«ЕЯ«ЋЯ»Ї Я«ЋЯ«┐Я«ЪЯ»ѕЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї.
(8.18) Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї (8.19) Я«ЄЯ«хЯ«▒Я»ЇЯ«▒Я»ѕ Я«њЯ«фЯ»ЇЯ«фЯ«┐Я«ЪЯ»ЂЯ««Я»ЇЯ«фЯ»ІЯ«цЯ»Ђ
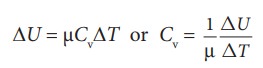
╬ћT Я«»Я«┐Я«ЕЯ»Ї Я«јЯ«▓Я»ЇЯ«▓Я»ѕ Я«џЯ»ЂЯ«┤Я«┐Я«»Я«┐Я«ЕЯ»ѕ Я«ЁЯ«ЪЯ»ѕЯ«»Я»ЂЯ««Я»ЇЯ«фЯ»ІЯ«цЯ»Ђ (╬ћTРєњ0), Я«еЯ«ЙЯ««Я»Ї

Я«јЯ«Е Я«јЯ«┤Я»ЂЯ«цЯ«▓Я«ЙЯ««Я»Ї.
Я«ЄЯ«ЎЯ»ЇЯ«ЋЯ»Ђ Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЁЯ«Ћ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»Ї Я«ЄЯ«░Я«БЯ»ЇЯ«ЪЯ»ЂЯ««Я»Є Я«еЯ«┐Я«▓Я»ѕ Я««Я«ЙЯ«▒Я«┐Я«ЋЯ«│Я»Ї. Я«јЯ«ЕЯ«хЯ»Є, Я««Я»ЄЯ«▒Я»ЇЯ«ЋЯ«БЯ»ЇЯ«Ъ Я«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»Ђ Я«ЁЯ«ЕЯ»ѕЯ«цЯ»ЇЯ«цЯ»Ђ Я«еЯ«┐Я«ЋЯ«┤Я»ЇЯ«хЯ»ЂЯ«ЋЯ«│Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї Я«фЯ»іЯ«░Я»ЂЯ«цЯ»ЇЯ«цЯ««Я«ЙЯ«ЕЯ«цЯ«ЙЯ«ЋЯ»ЂЯ««Я»Ї.
Я««Я»ЄЯ«»Я«░Я»Ї Я«цЯ»іЯ«ЪЯ«░Я»ЇЯ«фЯ»Ђ (Meyer's Relation):
┬х Я««Я»ІЯ«▓Я»Ї Я«ЁЯ«│Я«хЯ»ЂЯ«ЪЯ»ѕЯ«» Я«еЯ«▓Я»ЇЯ«▓Я«┐Я«»Я«▓Я»ЇЯ«фЯ»Ђ Я«хЯ«ЙЯ«»Я»Ђ Я«ЋЯ»іЯ«│Я»ЇЯ«ЋЯ«▓Я«ЕЯ»Ї Я«њЯ«ЕЯ»ЇЯ«▒Я«┐Я«▓Я»Ї Я«ЁЯ«ЪЯ»ѕЯ«цЯ»ЇЯ«цЯ»Ђ Я«хЯ»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«ЪЯ»ЂЯ«│Я»ЇЯ«│Я«цЯ»Ђ. Я«ЁЯ«хЯ»ЇЯ«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї V, Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ««Я»Ї P Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕ T Я«јЯ«ЕЯ»ЇЯ«Ћ. Я««Я«ЙЯ«▒Я«ЙЯ«фЯ»ЇЯ«фЯ«░Я»ЂЯ««Я«ЕЯ«┐Я«▓Я»Ї Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕ dT Я«ЁЯ«│Я«хЯ»Ђ Я«ЅЯ«»Я«░Я»ЇЯ«цЯ»ЇЯ«цЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«ЄЯ«ЎЯ»ЇЯ«ЋЯ»Ђ Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«ЙЯ«▓Я»Ї Я«јЯ«хЯ»ЇЯ«хЯ«┐Я«ц Я«хЯ»ЄЯ«▓Я»ѕЯ«»Я»ЂЯ««Я»Ї Я«џЯ»єЯ«»Я»ЇЯ«»Я«фЯ»ЇЯ«фЯ«ЪЯ«хЯ«┐Я«▓Я»ЇЯ«▓Я»ѕ. Я«јЯ«ЕЯ«хЯ»Є Я«ЁЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ«┐Я«▒Я»ЇЯ«ЋЯ»ЂЯ«ЋЯ»Ї Я«ЋЯ»іЯ«ЪЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ Я«хЯ»єЯ«фЯ»ЇЯ«фЯ««Я»Ї Я«ЁЯ«Ћ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я»ѕ Я««Я«ЪЯ»ЇЯ«ЪЯ»ЂЯ««Я»Є Я«ЁЯ«цЯ«┐Я«ЋЯ«░Я«┐Я«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї. Я«ЁЯ«Ћ Я«єЯ«▒Я»ЇЯ«▒Я«▓Я«┐Я«▓Я»Ї Я«ЈЯ«▒Я»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ Я««Я«ЙЯ«▒Я»ЇЯ«▒Я«цЯ»ЇЯ«цЯ»ѕ dU Я«јЯ«ЕЯ»ЇЯ«Ћ.
CV Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ»Ђ Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї Я««Я«ЙЯ«▒Я«Й Я««Я»ІЯ«▓Я«ЙЯ«░Я»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї Я«јЯ«ЕЯ«┐Я«▓Я»Ї Я«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»Ђ (8.20) Я«љ Я«фЯ«┐Я«ЕЯ»ЇЯ«хЯ«░Я»ЂЯ««Я«ЙЯ«▒Я»Ђ Я«јЯ«┤Я»ЂЯ«цЯ«▓Я«ЙЯ««Я»Ї.

Я««Я«ЙЯ«▒Я«Й Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ«цЯ»ЇЯ«цЯ«┐Я«▓Я»Ї Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ»ѕ Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ»ЂЯ««Я»ЇЯ«фЯ»ІЯ«цЯ»Ђ, Я«ЁЯ«хЯ»ЇЯ«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕ Я«ЅЯ«»Я«░Я»ЇЯ«хЯ»Ђ dT Я«јЯ«ЕЯ«хЯ»ЂЯ««Я»Ї, Я«ЁЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ«┐Я«▒Я»ЇЯ«ЋЯ»ЂЯ«ЋЯ»Ї Я«ЋЯ»іЯ«ЪЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«цЯ»ЇЯ«цЯ«┐Я«ЕЯ»Ї Я«ЁЯ«│Я«хЯ»Ђ РђўQРђЎ Я«јЯ«ЕЯ«хЯ»ЂЯ««Я»Ї, Я«ЄЯ«еЯ»ЇЯ«еЯ«┐Я«ЋЯ«┤Я»ЇЯ«хЯ«┐Я«ЕЯ«ЙЯ«▓Я»Ї Я«фЯ«░Я»ЂЯ««Я«ЕЯ«┐Я«▓Я»Ї Я«ЈЯ«▒Я»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ Я««Я«ЙЯ«▒Я»ЇЯ«▒Я««Я»Ї 'dv' Я«јЯ«ЕЯ«хЯ»ЂЯ««Я»Ї Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ«ЙЯ«▓Я»Ї

Я«ЄЯ«еЯ»ЇЯ«еЯ«┐Я«ЋЯ«┤Я»ЇЯ«хЯ«┐Я«ЕЯ«ЙЯ«▓Я»Ї Я«џЯ»єЯ«»Я»ЇЯ«»Я«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«Ъ Я«хЯ»ЄЯ«▓Я»ѕ

Я«єЯ«ЕЯ«ЙЯ«▓Я»Ї, Я«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЄЯ«»Я«ЋЯ»ЇЯ«ЋЯ«хЯ«┐Я«»Я«▓Я«┐Я«ЕЯ»Ї Я««Я»ЂЯ«цЯ«▓Я»Ї Я«хЯ«┐Я«цЯ«┐Я«фЯ»ЇЯ«фЯ«ЪЯ«┐

Я«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»ЂЯ«ЋЯ«│Я»Ї (8.21), (8.22) Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї (8.23) Я«ЄЯ««Я»ЇЯ««Я»ѓЯ«ЕЯ»ЇЯ«▒Я»ѕЯ«»Я»ЂЯ««Я»Ї (8.24) Я«ЄЯ«▓Я»Ї Я«фЯ«┐Я«░Я«цЯ«┐Я«»Я«┐Я«ЪЯ»ЂЯ««Я»Ї Я«фЯ»ІЯ«цЯ»Ђ,
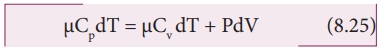
Я«јЯ«ЕЯ«ЋЯ»Ї Я«ЋЯ«┐Я«ЪЯ»ѕЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ««Я»Ї.
┬х Я««Я»ІЯ«▓Я»Ї Я«еЯ«▓Я»ЇЯ«▓Я«┐Я«»Я«▓Я»ЇЯ«фЯ»Ђ Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«▒Я»ЇЯ«ЋЯ»Ђ Я«еЯ«┐Я«▓Я»ѕЯ«џЯ»ЇЯ«џЯ««Я«ЕЯ»ЇЯ«фЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ»ѕ Я«фЯ«┐Я«ЕЯ»ЇЯ«хЯ«░Я»ЂЯ««Я«ЙЯ«▒Я»Ђ Я«јЯ«┤Я»ЂЯ«цЯ«▓Я«ЙЯ««Я»Ї.
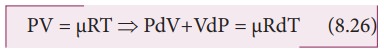
Я«ЄЯ«ЎЯ»ЇЯ«ЋЯ»Ђ Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ««Я»Ї Я««Я«ЙЯ«▒Я«ЙЯ«цЯ»Ђ, Я«јЯ«ЕЯ«хЯ»Є dP = 0, PdV = ┬хRdT
Рѕ┤ CpdT = CvdT +RdT
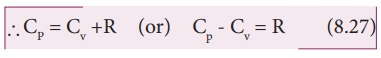
Я«ЄЯ«цЯ»ЇЯ«цЯ»іЯ«ЪЯ«░Я»ЇЯ«фЯ«┐Я«▒Я»ЇЯ«ЋЯ»Ђ Я««Я»ЄЯ«»Я«░Я»Ї Я«цЯ»іЯ«ЪЯ«░Я»ЇЯ«фЯ»Ђ Я«јЯ«ЕЯ»ЇЯ«▒Я»Ђ Я«фЯ»єЯ«»Я«░Я»Ї.
Я««Я«ЙЯ«▒Я«Й Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ«цЯ»ЇЯ«цЯ«┐Я«▓Я»Ї Я«еЯ«▓Я»ЇЯ«▓Я«┐Я«»Я«▓Я»ЇЯ«фЯ»Ђ Я«хЯ«ЙЯ«»Я»ЂЯ«хЯ«┐Я«ЕЯ»Ї Я««Я»ІЯ«▓Я«ЙЯ«░Я»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї, Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї Я««Я«ЙЯ«▒Я«Й Я««Я»ІЯ«▓Я«ЙЯ«░Я»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї R Я«єЯ«ЋЯ«┐Я«»Я«хЯ«▒Я»ЇЯ«▒Я«┐Я«ЕЯ»Ї Я«ЋЯ»ѓЯ«ЪЯ»ЂЯ«цЯ«▓Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ»ЂЯ«џЯ»Ї Я«џЯ««Я««Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ»ѕ Я«ЄЯ«цЯ»ЇЯ«цЯ»іЯ«ЪЯ«░Я»ЇЯ«фЯ»Ђ Я«еЯ««Я«ЋЯ»ЇЯ«ЋЯ»ЂЯ«ЋЯ»Ї Я«ЋЯ«ЙЯ«ЪЯ»ЇЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.
Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї Я«ЄЯ«цЯ»ЇЯ«цЯ»іЯ«ЪЯ«░Я»ЇЯ«фЯ«┐Я«▓Я«┐Я«░Я»ЂЯ«еЯ»ЇЯ«цЯ»Ђ, Я«ЁЯ«┤Я»ЂЯ«цЯ»ЇЯ«цЯ««Я»Ї Я««Я«ЙЯ«▒Я«Й Я««Я»ІЯ«▓Я«ЙЯ«░Я»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»Ї (CP), Я«фЯ«░Я»ЂЯ««Я«ЕЯ»Ї Я««Я«ЙЯ«▒Я«Й Я««Я»ІЯ«▓Я«ЙЯ«░Я»Ї Я«цЯ«ЕЯ»ЇЯ«хЯ»єЯ«фЯ»ЇЯ«ф Я«ЈЯ«▒Я»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«▒Я«ЕЯ»ѕЯ«хЯ«┐Я«Ъ (CV) Я«јЯ«фЯ»ЇЯ«фЯ»ІЯ«цЯ»ЂЯ««Я»Ї Я«ЁЯ«цЯ«┐Я«ЋЯ««Я»Ї Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ»ѕ Я«еЯ«ЙЯ««Я»Ї Я«фЯ»ЂЯ«░Я«┐Я«еЯ»ЇЯ«цЯ»Ђ Я«ЋЯ»іЯ«│Я»ЇЯ«│Я«▓Я«ЙЯ««Я»Ї.