கேள்விகளுக்கான பதில்கள் - சரியான விடையினைத் தெரிவு செய்க | 11th Chemistry : UNIT 4 : Hydrogen
11 வது வேதியியல் : அலகு 4 : ஹைட்ரஜன்
சரியான விடையினைத் தெரிவு செய்க
மதிப்பீடு
I. சரியான விடையினைத் தெரிவு செய்க
1. கீழ்க்கண்ட கூற்றுகளில் ஹைட்ரஜன் பற்றிய தவறான கூற்று எது (NEET 2006)
(அ) ஹைட்ரஜன் அயனி, H3O+ கரைசலில் தனித்து உள்ளது
(ஆ) டைஹைட்ரஜன் ஒடுக்க வினைபொருளாக செயல்படுகிறது
(இ) ஹைட்ரஜன் மூன்று ஐசோடோப்புகளைக் கொண்டுள்ளது. அவற்றுள் டிரிட்டியம் அதிக அளவில் காணப்படுகிறது.
(ஈ) அயனி உப்புகளில், எப்போதும் ஹைட்ரஜன் நேர் அயனியாகக் காணப்படுவதில்லை.
[விடை: (இ) ஹைட்ரஜன் மூன்று ஐசோடோப்புகளைக் கொண்டுள்ளது. அவற்றுள் டிரிட்டியம் அதிக அளவில் காணப்படுகிறது.]
2. நீர் வாயு என்பது
(அ) H2O (g)
(ஆ) CO + H2O
(இ) CO + H2
(ஈ) CO + N2
[விடை: இ) CO + H2 நீர் வாயு]
3. ஆர்த்தோ, பாரா டைஹைட்ரஜன் குறித்து கீழ்க்கண்டுள்ள கூற்றுகளில் எது தவறானது.
(அ) அவைகள் உட்கரு சுழற்சி ஐசோடோப்புகள் (மாற்றியங்கள்)
(ஆ) ஆர்த்தோ மாற்றியம் பூஜ்ஜிய உட்கரு சுழற்சியையும், பாரா மாற்றியம் ஒரு உட்கரு சுழற்சியும் கொண்டுள்ளது.
(இ) குறைந்த வெப்பநிலை, பாரா மாற்றியத்திற்கு சாதகமாக உள்ளது.
(ஈ) பாரா மாற்றியத்தின் வெப்ப கடத்துதிறன், அதன் ஆர்த்தோ மாற்றியத்தை விட 50% அதிகம்
[விடை: ஆ) சரியானக் கூற்று : ஆர்த்தோ மாற்றியம் பூஜ்ஜிய உட்கரு சுழற்சியையும், பாரா மாற்றியம் ஒரு உட்கரு சுழற்சியும் கொண்டுள்ளது.]
4. அயனி ஹைட்ரைடுகளை உருவாக்குபவை.
(அ) ஹேலஜன்கள்
(ஆ) சால்கோஜென்கள்
(இ) மந்த வாயுக்கள்
(ஈ) தொகுதி 1 - தனிமங்கள்
[விடை: (ஈ) தொகுதி 1 - தனிமங்கள்]
எ.கா: சோடியம் ஹைட்ரைடு (Na+ H−)
5. டிரிட்டியம் உட்கரு கொண்டுள்ளது --------------------
(அ) 1p + 0n
(ஆ) 2p + 1n
(இ) 1p + 2n
(ஈ) இவற்றில் ஏதும் இல்லை
[விடை: இ) 1p + 2n]
குறிப்பு : 1T3(1e, 1p , 2n)
6. வேதிவினைக்கூறு விகிதத்தின் அடிப்படையில் அமையாத (non – stoichiometric) ஹைட்ரைடுகளை உருவாக்குபவை
(அ) பெலேடியம், வெனேடியம்
(ஆ) கார்பன், நிக்கல்
(இ) மாங்கனீசு, லித்தியம்
(ஈ) நைட்ரஜன், குளோரின்
[விடை: ஆ) கார்பன், நிக்கல்]
7. கூற்று: கடின நீரை சலவைச் சோடாவுடன் வினைப்படுத்துவதன் மூலம், அதன் நிரந்தரக் கடினத் தன்மையினை நீக்கலாம்.
காரணம்: சலவைச்சோடா, கடின நீரில் கரைந்துள்ள கால்சியம் மற்றும் மெக்னீசியம் குளோரைடு மற்றும் சல்பேட்டுகளுடன் வினைபுரிந்து கரையாத கார்பனேட்டுகளை உருவாக்குகிறது.
(அ) கூற்று மற்றும் காரணம் இரண்டும் சரி, மற்றும் காரணம், கூற்றிற்கு சரியான விளக்கமாகும்
(ஆ) கூற்று மற்றும் காரணம் இரண்டும் சரி, ஆனால் காரணம், கூற்றிற்கு சரியான விளக்கமல்ல.
(இ) கூற்று சரியானது ஆனால் காரணம் தவறானது
(ஈ) கூற்று மற்றும் காரணம் இரண்டும் தவறானவை
[விடை: அ) கூற்று மற்றும் காரணம் இரண்டும் சரி, மற்றும் காரணம், கூற்றிற்கு சரியான விளக்கமாகும்.]
குறிப்பு : Ca2+ + Na2CO3 → CaCO3 ↓+ 2Na+
8. ஒரு மீனின் உடலில், அதன் மொத்த உடல் நிறையில் 1.2g ஹைட்ரஜன் உள்ளது. அனைத்து ஹைட்ரஜனும், டியூட்டிரியத்தால் பதிலீடு செய்யப்படும் போது மீனின் நிறை அதிகரிப்பு.
(அ) 1.2 g
(ஆ) 2.4 g
(இ) 3.6 g
(ஈ) √4.8 g
[விடை: அ) 1.2g ]
தீர்வு: டியூட்ரியத்தின் நிறை = 2 × புரோட்டியத்தின் நிறை அனைத்து 1.2g ஹைட்ரஜனும் டியூட்ரியத்தால் பதிலீடு செய்யப்படும் போது அதன் நிறையானது 2.4g ஆகிறது. எனவே உடல்நிறை அதிகரிப்பு (2.4 − 1.2 = 1.2g)
9. நீரின் கடினத்தன்மையை பருமனறி பகுப்பாய்வின் மூலம் தீர்மானிக்கப் பயன்படும் காரணி
(அ) சோடியம் தயோ சல்பேட்
(ஆ) பொட்டாசியம் பெர்மாங்கனேட்
(இ) ஹைட்ரஜன் பெராக்சைடு
(ஈ) EDTA
[விடை: ஈ) EDTA]
10. நீரின் நிரந்தர கடினத்தன்மைக்கு காரணம்
(அ) Ca (HCO3)2
(ஆ) Mg (HCO3)2
(இ) CaCl2
(ஈ) MgCO3
[விடை: இ) CaCl2]
குறிப்பு : நீரில் Ca2+மற்றும் Mg2+ அயனிகளின் குளோரைடுகள், நைட்ரேட்டுகள் மற்றும் சல்பேட்டுகள் காணப்படுவதால் நீருக்கு நிரந்தர கடினத்தன்மை ஏற்படுகிறது.
11. நீரின் கடினத்தன்மையை மென்மையாக்கப் பயன்படும் சியோலைட்டானது, நீரேற்றம் அடைந்த
(அ) சோடியம் அலுமினியம் சிலிகேட்
(ஆ) கால்சியம் அலுமினியம் சிலிகேட்
(இ) ஜிங்க் அலுமினியம் போரேட்
(ஈ) லித்தியம் அலுமினியம் ஹைட்ரைடு
[விடை: அ) சோடியம் அலுமினியம் சிலிகேட்]
குறிப்பு : சியோலைட் என்பது சோடியம் அலுமினியம் சிலிகேட் ஆகும். (Na AlSi2 O6 .H2O)
12. வணிக ரீதியான ஹைட்ரஜன் பெராக்சைடில் (H2O2) 100 - கனஅளவு எனக் குறிப்பிடப்பட்டுள்ளது. இதன் பொருள்
(அ) திட்டவெப்ப அழுத்த நிலையில் (STPல்), 1mL H2O2 ஆனது 100mL O2ஐத் தரும்.
(ஆ) திட்டவெப்ப அழுத்த நிலையில் (STPல்), 1L H2O2 ஆனது 100mL O2 ஐத் தரும்.
(இ) 1L H2O2 ஆனது 22.4L O2ஐத் தரும்.
(ஈ) திட்டவெப்ப அழுத்த நிலையில் (STPல்), 1mL H2O2 ஆனது ஒரு மோல் O2 ஐத் தரும்.
[விடை: அ) திட்டவெப்ப அழுத்த நிலையில் (STPல்), 1ml H2O2 ஆனது 100ml O2ஐத் தரும்.]
13. ஈதரின் முன்னிலையில், பொட்டாசியம் டைகுரோமேட் கரைசலுடன் ஹைட்ரஜன் பெராக்சைடு சேர்த்து குலுக்கப்படும்போது, ஈதர் அடுக்கானது நீலநிறமாக மாறுவதற்குக் காரணமாக, உருவாவது
(அ) Cr2O3
(ஆ) CrO42-
(இ) CrO(O2)2
(ஈ) இவற்றில் ஏதும் இல்லை
[விடை: இ) CrO(O2)2]
தீர்வு : Cr2O72− + 2H+ + 4H2O2 → 2CrO(O2) 2 + 5H2O
14. ஒரு மோல் அமிலம் கலந்த KMnO4 யை நிறமிழக்கச் செய்யத் தேவைப்படும் H2O2ன் மோல்களின் எண்ணிக்கை.
(அ) 1 / 2
(ஆ) 3 / 2
(இ) 5 / 2
(ஈ) 7 / 2
[விடை: இ) 5/2]
குறிப்பு : 2MnO4− + 5H2O2(aq) + 6H+ → 2Mn2+ + 5O2 + 8H2O
15. 1.5 N H2 O2ன் கனஅளவுச் செறிவு
(அ) 1.5
(ஆ) 4.5
(இ) 16.8
(ஈ) 8.4
[விடை: ஈ) 8.4]
தீர்வு : ஹைட்ரஜன் பெராக்ஸைடின் கனஅளவுச் செறிவு ஹைட்ரஜன் பெராக்ஸைடின் நார்மாலிட்டி × 5.6
= 1.5 × 5.6 = 8.4
2H2O2 → 2H2O + O2↑
(2 × 34g) (22.4 litres)
ஹைட்ரஜன் பெராக்ஸைடின் கனஅளவுச் செறிவு = நார்மாலிட்டி × H2O2 ன் சமமான நிறை × (22.4/68)
= நார்மாலிட்டி × (17 × 22.4)/68
ஹைட்ரஜன் பெராக்ஸைடின் கனஅளவுச் செறிவு = நார்மாலிட்டி × 5.6.
16. H2O மற்றும் H2O2 மூலக்கூறுகளில் உள்ள ஆக்ஸிஜன் அணுவின் இனக்கலப்பாதல் முறையே
(அ) SP மற்றும் SP3
(ஆ) SP மற்றும் SP
(இ) SP மற்றம் SP2
(ஈ) SP3 மற்றும் SP3
[விடை: ஈ) sp3 மற்றும் sp3]
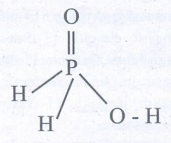
17. H3PO2 + D2O → H2DPO2 + HDO என்ற வினையிலிருந்து ஹைப்போ பாஸ்பரஸ் அமிலம் ஒரு
(அ) முக்காரத்துவ அமிலம்
(ஆ) இருகாரத்துவ அமிலம்
(இ) ஒரு காரத்துவ அமிலம்
(ஈ) இவற்றுள் ஏதுமில்லை
[விடை: இ) ஒரு காரத்துவ அமிலம்]
தீர்வு : ஹைப்போ பாஸ்பரஸ் அமிலமானது D2O2 உடன் வினைபுரியும் போது ஒரே ஒரு ஹைட்ரஜன் மட்டும் டியூட்ரியத்தால் பதிலீடு செய்யப்படுகிறது. எனவே இது ஒரு காரத்துவ அமிலம்.
18. திட பனிக்கட்டியில், ஆக்சிஜன் அணுவானது
(அ) 4 ஹைட்ரஜன் அணுக்களால் நான்முகி வடிவில் சூழப்பட்டுள்ளது
(ஆ) 2 ஹைட்ரஜன் அணுக்கள் மற்றும் நான்கு ஹைட்ரஜன் அணுக்களால் எண்முகி வடிவில் சூழப்பட்டுள்ளது.
(இ) 2 ஹைட்ரஜன் மற்றும் 2 ஆக்ஸிஜன் அணுக்களால் நான்முகி வடிவில் சூழப்பட்டுள்ளது
(ஈ) 6 ஹைட்ரஜன் அணுக்களால் எண்முகி வடிவில் சூழப்பட்டுள்ளது.
[விடை: அ) 4 ஹைட்ரஜன் அணுக்களால் நான்முகி வடிவில் சூழப்பட்டுள்ளது.]
(படம் 4.6 பனிக்கட்டியின் வடிவம் பார்க்க)
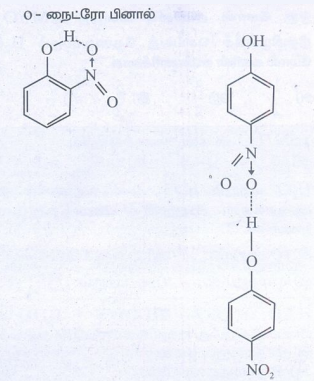
19. ஆர்த்தோ நைட்ரோபீனால் மற்றும் பாரா நைட்ரோ பீனாலில் காணப்படும் H- பிணைப்புகள் முறையே,
(அ) மூலக்கூறுகளுக்கிடையேயான H- பிணைப்பு மற்றும் மூலக்கூறினுள் நிகழும் H- பிணைப்பு
(ஆ) மூலக்கூறினுள் நிகழும் H-பிணைப்பு மற்றும் மூலக்கூறுகளுக்கிடையேயான H- பிணைப்பு
(இ) மூலக்கூறினுள் நிகழும் H- பிணைப்பு
(ஈ) மூலக்கூறினுள் நிகழும் H- பிணைப்பு மற்றும் H-பிணைப்பு இல்லை.
[விடை: ஆ) மூலக்கூறினுள் நிகழும் H−பிணைப்பு மற்றும் மூலக்கூறுகளுக்கிடையேயான H−பிணைப்பு ]
20. கனநீர் பயன்படுவது
(அ) அணுக்கரு வினைகளில் மட்டுப்படுத்தி
(ஆ) அணுக்கரு வினைகளின் குளிர்விப்பான்
(இ) (அ) மற்றும் (ஆ)
(ஈ) எதுவும் இல்லை
[விடை: இ) (அ) மற்றும் (ஆ) ]
குறிப்பு : கனநீரானது அணுக்கரு வினைகளில் மட்டுப் படுத்தியாகவும், குளிர்விப்பானாகவும் செயல்பட வல்லது.
21. நீரானது.
(அ) கார ஆக்ஸைடு
(ஆ) அமில ஆக்ஸைடு
(இ) ஈரியில்பு ஆக்ஸைடு
(ஈ) இவை எதுவுமில்லை
[விடை: இ) ஈரியல்பு ஆக்ஸைடு]
குறிப்பு : நீரானது ஒரு ஈரியல்பு ஆக்ஸைடாகும்.