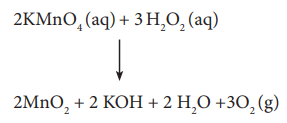11 வது வேதியியல் : அலகு 4 : ஹைட்ரஜன்
ஹைட்ரஜன் பெராக்சைடின் இயற் மற்றும் வேதிப்பண்புகள்
இயற்பண்புகள்
தூய்மையான ஹைட்ரஜன் பெராக்சைடு ஏறத்தாழ நிறமற்ற திரவமாகும். (வெளிர்ந்த நீல நிறம்), நீரைவிட அதிக பாகுநிலைத் தன்மையும், குறைவாக ஆவியாகும் தன்மையினையும் கொண்டுள்ளது.
ஹைட்ரஜன் பெராக்சைடின் 30% கரைசலானது '100-கனஅளவு' ஹைட்ரஜன் பெராக்சைடு எனக் குறிப்பிடப்படுகிறது. திட்டவெப்ப அழுத்த நிலையில் (S.T.P.ல்) 1 mL அளவுள்ள இந்த ஹைட்ரஜன் பெராக்சைடை சூடுபடுத்தும்போது 100 mL ஆக்சிஜன் வெளியேறுகிறது.
வேதிப்பண்புகள்
ஹைட்ரஜன் பெராக்சைடு மிகவும் நிலைப்புத்தன்மை அற்றது. இதன் நீர்க்கரைசல் தானாகவே, விகித சிதைவடைந்து ஆக்சிஜன் மற்றும் நீரைத்தருகிறது. இவ்வினை மெதுவாக நிகழ்வதாக இருந்த போதிலும், உலோகம் வினையூக்கியாக பயன்படுத்தப்படும் நிலையில் வெடிக்கும் தன்மையுடையதாகும். இதனைக் கண்ணாடி கலன்களில் சேகரித்து வைக்கும் போது, கண்ணாடியில் உள்ள கார உலோகங்களை இது கரைக்கிறது. இது விகிதச் சிதைவு வினைக்கு வினையூக்கியாகிறது. இக்காரணத்தினால் தான் H2O2 கரைசலானது நெகிழி கலன்களில் சேமித்து வைக்கப்படுகிறது.
H2O2 → H2O + 1/2 O2
ஹைட்ரஜன் பெராக்சைடு, ஆக்சிஜனேற்றி மற்றும் ஆக்சிஜன் ஒடுக்கி ஆகிய இரண்டு வினைபொருட்களாகவும் செயல்படும் தன்மையுடையது. வழக்கமாக ஆக்சிஜனேற்ற வினைகள் அமில ஊடகத்திலும், ஆக்சிஜன் ஒடுக்க வினைகள் கார ஊடகத்திலும் நிகழ்த்தப்படுகின்றன.
அமில ஊடகத்தில்
H2O2 + 2 H+ + 2 e- → 2 H2O (E0 = +1.77 V)
எடுத்துக்காட்டாக,
2 FeSO4 + H2SO4 + H2O2 → Fe2 (SO4)3 + 2 H2O
கார ஊடகத்தில்,
HO2- + OH- → O2 + H2O + 2 e-
(E0 = + 0.08 V)
எடுத்துக்காட்டாக,