எடுத்துக்காட்டுகள், தயாரித்தல், பண்புகள், அமைப்பு, பயன்கள் - படிகாரங்கள் | 12th Chemistry : UNIT 2 : p-Block Elements-I
12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 2 : p-தொகுதி தனிமங்கள்-I
படிகாரங்கள்
படிகாரங்கள்:
பொட்டாசியம், அலுமினியம் சல்பேட்டின் இரட்டை உப்பானது [K2SO4-A12 (SO4)3 24.H2O] படிகாரம் என பெயரிடப்பட்டுள்ளது. தற்போது, M'2SO4M"2 (SO4)3 24H2O,வாய்ப்பாடு கொண்ட அனைத்து இரட்டை உப்புக்களுக்கும் இப்பெயர் பயன்படுத்தப்படுகிறது. இங்கு M' என்பது ஒற்றை நேர்மின் கொண்ட உலோக அயனி அல்லது (NH4]+ மற்றும் M" என்பது மூன்று நேர்மின்சுமை கொண்ட உலோக அயனி ஆகும்.
எடுத்துக்காட்டுகள்:
பொட்டாஷ்படிகாரம்[K2SO4-A12 (SO4)3 24.H2O] சோடியம்படிகாரம்(Na2SO4-A12 (SO4)3 24.H2O] அம்மோனியம் படிகாரம்[(NH4)2SO4A12(SO4)3 24.H2O), குரோம் படிகாரம் [K2SO4-Cr2 (SO4)3 24.H2O] பொதுவாக படிகாரங்கள் குளிர்ந்த நீரைவிட, வெந்நீரில் அதிகமாக கரையக்கூடியவை. கரைசல்களில் அவை அவற்றின் உட்கூறு அயனிகளின் பண்புகளை வெளிக்காட்டுகின்றன.
தயாரித்தல்:
அலுனைட் - படிகாரக் கல் என்பது இயற்கையில் காணப்படும் படிகமாகும், இதன் வாய்ப்பாடு K2SO4-A12 (SO4)3 4A1(OH)3- படிகாரக் கல்லை அதிகளவு கந்தக அமிலத்துடன் வினைப்படுத்தும்போது, அலுமினியம் ஹைட்ராக்சைடு முற்றிலும் அலுமினியம் சல்பேட்டாக மாற்றப்படுகிறது. இதனுடன் கணக்கிடப்பட்ட அளவு பொட்டாசியம் சல்பேட் சேர்த்து கரைசலை படிகமாக்கும் போது பொட்டாஷ் படிகாரம் கிடைக்கிறது. இது மறுபடிகமாக்கல் மூலம் தூய்மைப்படுத்தப்படுகிறது.
K2SO4.Al2(SO4)3 .4Al(OH)3 + 6H2SO4 → K2SO4 + 3Al2(SO4)3 + 12 H2O
K2SO4 + Al2(SO4)3 + 24 H2O → K2SO4.Al2(SO4)3.24 H2O
பண்புகள் :
பொட்டாஷ் படிகாரம் ஒரு வெண்ணிற படிகமாகும், இது நீரில் கரைகிறது ஆனால் ஆல்கஹாலில் கரைவதில்லை . இதன் நீர்க்கரைசலில் அலுமினியம் சல்பேட் நீராற்பகுப்படைவதால் கரைசல் அமிலத்தன்மை கொண்டதாக மாறுகிறது. பொட்டாஷ் படிகாரத்தை வெப்பப்படுத்தும் போது 365K வெப்பநிலையில் உருகுகிறது. 475 K வெப்பநிலையில் படிக நீரை இழந்து உருப்பெருக்கம் அடைகிறது. இது எரிக்கப்பட்ட படிகாரம் என்றழைக்கப்படுகிறது. இதை செஞ்சூட்டு நிலைக்கு வெப்பப்படுத்தும்போது சிதைந்து பொட்டாசியம் சல்பேட், அலுமினா மற்றும் சல்பர் ட்ரை ஆக்சைடு ஆகியவற்றை தருகிறது.
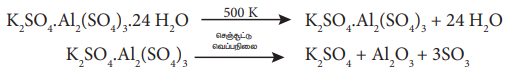
பொட்டாஷ் படிகாரத்தை, அம்மோனியம் ஹைட்ராக்சைடுடன் வினைப்படுத்தும்போது அலுமினியம் ஹைட்ராக்சைடு கிடைக்கிறது.
K2SO4 A12 (SO4)3 24H2O + 6NH4OH → K2SO4 + 3(NH4)2SO4 + 24H2O + 2A1(OH)3
படிகாரத்தின் பயன்கள்
1. இது நீர் சுத்திகரிப்பில் பயன்படுகிறது.
2. இது நீர் ஒட்டா ஆடைகள் தயாரித்தலிலும், ஜவுளித் துறையிலும் பயன்படுகிறது.
3. இது சாயமிடுதல், காகிதம் மற்றும் தோல் பதனிடும் தொழிற்சாலைகளில் பயன்படுகிறது.
4. இது இரத்தக் கசிவைத் தடுக்கும் "குறுதி தடுப்பான்" ஆக பயன்படுகிறது.