தனிமவரிசை அட்டவணை | வேதியியல் - இரண்டாம் வரிசை தனிமங்களின் முரண்பட்ட பண்புகள் | 11th Chemistry : UNIT 3 : Periodic Classification of Elements
11 வது வேதியியல் : அலகு 3 : தனிமங்களின் ஆவர்த்தன வகைப்பாடு
இரண்டாம் வரிசை தனிமங்களின் முரண்பட்ட பண்புகள்
இரண்டாம் வரிசை தனிமங்களின் முரண்பட்ட பண்புகள்
ஒரே தொகுதியில் உள்ள தனிமங்கள், ஒரே மாதிரியான இயற் மற்றும் வேதிப் பண்புகளைப் பெற்றுள்ளன. எனினும் ஒவ்வொரு தொகுதியிலும் உள்ள முதல் தனிமமானது அத்தனிமம் இடம்பெற்றுள்ள தொகுதியில் உள்ள பிற தனிமங்களின் பண்புகளிலிருந்து சில முரண்பட்ட பண்புகளைப் பெற்றிருக்கின்றன. உதாரணமாக, கார மற்றும் காரமண் உலோகங்கள் பொதுவாக அயனிச் சேர்மங்களை உருவாக்கும் தன்மையினைப் பெற்றுள்ளன. மாறாக, லித்தியம் மற்றும் பெரிலியம் ஆகியன அதிக அளவில் சகப்பிணைப்புச் சேர்மங்களை உருவாக்குகின்றன. இரண்டாம் வரிசையில் உள்ள தனிமங்கள் அவற்றின் இணைதிற கூட்டில் மொத்தம் நான்கு ஆர்பிட்டால்களை (2s மற்றும் 2p) மட்டும் பெற்றிருக்கின்றன. எனவே அவற்றின் அதிகபட்ச சகப்பிணைப்பு இணைதிறன் 4. ஆனால் அடுத்தடுத்த வரிசைகளில் உள்ள தனிமங்கள் தங்களது இணைதிற கூட்டில் அதிக ஆர்பிட்டால்களைப் பெற்றுள்ளன. எனவே உயர் இணைதிறன் மதிப்புகளைப் பெற்றுள்ளன. எடுத்துக்காட்டாக, போரான் BF4- ஐயும் மற்றும் அலுமினியம் AIF63-ஐயும் உருவாக்குகின்றன.
மூலைவிட்டத் தொடர்பு
தனிம வரிசை அட்டவணையில் மூலைவிட்டமாகச் செல்லும் போது இரண்டாம் மற்றும் மூன்றாம் வரிசையில் உள்ள தனிமங்கள் சில பண்புகளில் ஒத்துக் காணப்படுகின்றன. ஒரு தொகுதியில் காணப்படும் தனிமங்களுக்கிடையே நாம் காணும் பண்புகளைப் போன்று அதிக அளவில் ஒற்றுமைத் தன்மை காணப்படாவிட்டாலும் கூட, பின்வரும் தனிம இணைகளில் இப்பண்பு குறிப்பிடத்தக்க அளவில் உள்ளது.
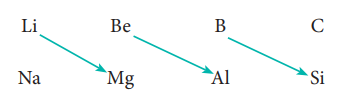
மூலைவிட்டத்தில் அமைந்துள்ள தனிமங்களின் பண்புகளுக்கிடையே காணப்படும் ஒற்றுமைத் தன்மை மூலை விட்டத் தொடர்பு என்றழைக்கப்படுகிறது.