11 வது வேதியியல் : அலகு 3 : தனிமங்களின் ஆவர்த்தன வகைப்பாடு
எலக்ட்ரான் அமைப்பின் அடிப்படையில் தனிமங்களை தொகுதிபடுத்துதல்
எலக்ட்ரான் அமைப்பின் அடிப்படையில் தனிமங்களை தொகுதிபடுத்துதல்
நவீன ஆவர்த்தன விதியின் அடிப்படையில் நவீன தனிமவரிசை அட்டவணையில் தனிமங்கள் 7-வரிசைகளிலும், 18-தொகுதிகளிலும் வைக்கப்பட்டுள்ளன. தனிமங்களை குறிப்பிட்ட இடத்தில் அமைத்தல் என்பது அதன் வெளிக்கூட்டு எலக்ட்ரான் அமைப்போடு நெருங்கிய தொடர்பு கொண்டது. தனிம வரிசை அட்டவணையின் தொடரிலும், தொகுதியிலும் எலக்ட்ரான் அமைப்பு எவ்வாறு மாறுபடுகின்றது என்பதை நாம் ஆய்ந்து அறிவோம்.
1. வரிசைகளில் எலக்ட்ரான் அமைப்பில் ஏற்படும் மாறுபாடு
ஒவ்வொரு வரிசையும் 'ns1' என்ற வெளிக்கூட்டு எலக்ட்ரான் அமைப்புடைய தனிமத்தில் துவங்கி 'ns2', np6’ என்ற வெளிக்கூட்டு எலக்ட்ரான் அமைப்புடைய தனிமத்துடன் நிறைவு பெறுகிறது என நாம் முன்னரே அறிவோம். இங்கு 'n' என்பது முதன்மைக் குவாண்டம் எண் ஆகும். முதல் வரிசையில், இணைதிற எலக்ட்ரான்கள் நிரப்பப்படுவது 1s ஆர்பிட்டாலில் துவங்குகிறது. இந்த ஆர்பிட்டாலில் அதிகபட்சமாக இரு எலக்ட்ரான்கள் மட்டுமே இடம் பெறமுடியும். எனவே முதல் வரிசையில் இரு தனிமங்கள், அதாவது ஹைட்ரஜன் மற்றும் ஹீலியம் ஆகிய இரண்டு தனிமங்கள் மட்டுமே இடம் பெறுகின்றன. இரண்டாவது வரிசையில் இணைதிற எலக்ட்ரான்கள் நிரப்பப்படுவது 2s ஆர்பிட்டாலில் துவங்கி பின்னர் மூன்று 2p ஆர்பிட்டால்களிலும் தொடர்கின்றன. இதில் லித்தியம் முதல் நியான் வரையிலான எட்டு தனிமங்கள் இடம் பெறுகின்றன.
மூன்றாவது வரிசையில் இணைதிற எலக்ட்ரான்கள் நிரப்பப்படுவது 3s ஆர்பிட்டாலில் துவங்கி பின்னர் 3p ஆர்பிட்டால்களிலும் தொடர்கின்றன. நான்காவது வரிசையில் இணைதிற எலக்ட்ரான்கள் முதலில் 4s ஆர்பிட்டாலிலும், பின்னர் 3d மற்றும் 4p ஆர்பிட்டால்களிலும் ஆஃபா தத்துவத்தின் அடிப்படையில் நிரப்பப்படுகின்றன. இதைப் போன்றே பிற வரிசைகளின் எலக்ட்ரான் அமைப்பினை நாம் விளக்க இயலும் (அட்டவணை 3.10)
அட்டவணை-3.10 வரிசைகளில் உள்ள தனிமங்களின் எலக்ட்ரான் அமைப்பு
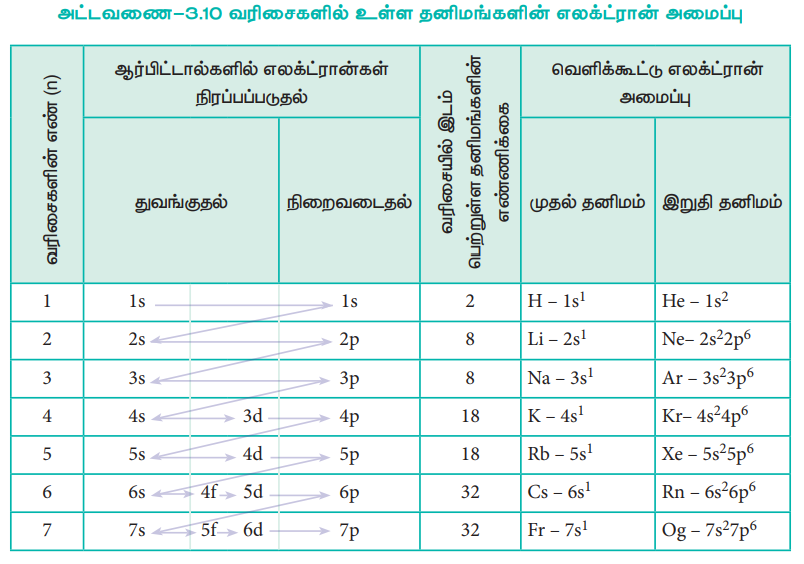
நான்காவது வரிசையில் 3d ஆர்பிட்டால்களில் இணைதிற எலக்ட்ரான்கள் நிரம்புதல் ஸ்கேன்டியத்திலிருந்து துவங்கி துத்தநாகத்தில் (zinc-ல்) நிறைவடைகிறது. இந்த 10 தனிமங்களையும் உள்ளடக்கிய வரிசை முதல் இடைநிலைத் தனிம வரிசை என அழைக்கப்படுகிறது. இதைப் போலவே அடுத்தடுத்த வரிசைகளில், 4d, 5d மற்றும் 6d ஆர்பிட்டால்களில் இணைதிற எலக்ட்ரான்கள் நிரப்பப்படுகின்றன. இவ்வரிசைகள் முறையே இரண்டாம், மூன்றாம் மற்றும் நான்காம் இடைநிலை வரிசைகள் என்றழைக்கப்படுகின்றன.
ஆறாவது வரிசையில், இணைதிற எலக்ட்ரான்கள் நிரப்பப்படுவது 6S ஆர்பிட்டாலில் துவங்கி பின்னர் 4f, 5d மற்றும் 6p ஆர்பிட்டால்களில் நிரப்பப்படுகின்றன. 4f ஆர்பிட்டால்கள் நிரப்பப்படுவது சீரியத்தில் (z = 58) துவங்கி லுட்டீசியத்தில் (z = 71) நிறைவடைகின்றது. இந்த 14 தனிமங்களையும் உள்ளடக்கிய வரிசை முதல் உள் இடைநிலைத்தனிம வரிசையாகும். இத்தனிமங்கள் லாந்தனைடுகள் என்றழைக்கப்படுகின்றன. இதைப்போலவே ஏழாவது வரிசையில் 5f ஆர்பிட்டால்கள் நிரப்பப்படுகின்றன. இந்த 14 தனிமங்களை உள்ளடக்கிய வரிசை ஆக்டினைடுகள் என்றழைக்கப்படுகின்றன. இந்த இரு வரிசைகளும் நவீன தனிமவரிசை அட்டவணையில் தனியே அடிப்பாகத்தில் வைக்கப்பட்டுள்ளன.
2. தொகுதிகளில் எலக்ட்ரான் அமைப்பில் ஏற்படும் மாறுபாடு
ஒரு தொகுதியில் உள்ள தனிமங்கள் அனைத்தும் அவற்றின் வெளிக்கூட்டில், ஒத்த எலக்ட்ரான் அமைப்பினைப் பெற்றுள்ளன. அட்டவணை (3.11)ல் பதினெட்டு தொகுதிகளுக்கான பொதுவான வெளிக்கூட்டு எலக்ட்ரான் அமைப்பு கொடுக்கப்பட்டுள்ளது. தனிமங்களின் கடைசி இணைதிற எலக்ட்ரான் சென்று சேரக்கூடிய ஆர்பிட்டாலின் அடிப்படையில் தனிமங்களை s, p, d மற்றும் f தொகுதி தனிமங்கள் என வகைப்படுத்தலாம்.
தொகுதி - 1 மற்றும் தொகுதி - 2 ல் உள்ள தனிமங்கள், s - தொகுதி தனிமங்கள் என்றழைக்கப்படுகின்றன. இவற்றின் கடைசி இணைதிற எலக்ட்ரான்கள் ns ஆர்பிட்டாலில் சென்று சேர்கிறது. தொகுதி - 1 ஐச் சேர்ந்த தனிமங்கள் கார உலோகங்கள் என்றும் தொகுதி - 2ஐச் சேர்ந்த தனிமங்கள் காரமண் உலோகங்கள் என்றும் அழைக்கப்படுகின்றன. இவைகள் குறைந்த கொதிநிலை, மற்றும் உருகு நிலையினைப் பெற்றிருப்பதுடன், குறைவான அயனியாக்கும் ஆற்றலையும் பெற்றுள்ள மென்மையான உலோகங்கள் ஆகும். இவைகள் அதிக வினைத்திறனைப் பெற்றிருக்கின்றன மேலும் அயனிச்சேர்மங்களை உருவாக்குகின்றன. இத்தனிமங்கள் அதிக எலக்ட்ரான் நேர்மின்தன்மையையும் மற்றும் தீச்சுடரில் நிறத்தினை ஏற்படுத்தும் தன்மையினையும் பெற்றிருக்கின்றன. இத்தனிமங்களின் பண்புகளைப் பற்றி அடுத்தடுத்த பாடப்பகுதிகளில் விரிவாக படிப்போம்.
தொகுதி - 13 முதல் 18 வரையிலான தனிமங்கள் p - தொகுதி தனிமங்கள் அல்லது பிரதிநிதித்துவ தனிமங்கள் என்றழைக்கப்படுகின்றன. இத்தனிமங்களின் பொதுவான வெளிக்கூட்டு எலக்ட்ரான் அமைப்பு ns2, np1-6 ஆகும். 16 மற்றும் 17ம் – தொகுதி தனிமங்கள் முறையே சால்கோஜன்கள் மற்றும் ஹாலஜன்கள் என்றழைக்கப்படுகின்றன. 18ம் தொகுதித் தனிமங்கள் முழுமையாக நிரப்பப்பட்ட இணைதிற கூட்டு எலக்ட்ரான் அமைப்பினை (ns2 np6) பெற்றுள்ளன. இவைகள் மந்த வாயுக்கள் (inert gases) அல்லது உயரிய வாயுக்கள் (noble gases) என அழைக்கப்படுகின்றன. p - தொகுதி தனிமங்கள் அதிகமான எதிர்க்குறி எலக்ட்ரான்கவர்தன்மை மதிப்புகளைப் பெற்றுள்ளன. s - தொகுதி தனிமங்களைக் காட்டிலும் இவற்றின் அயனியாக்கும் ஆற்றல் மதிப்பு அதிகம். இவைகள் பெரும்பாலும் சகப்பிணைப்புச் சேர்மங்களை உருவாக்குகின்றன. மேலும் இவைகள் உருவாக்கும் பல்வேறு சேர்மங்களில் ஒன்றுக்கும் மேற்பட்ட ஆக்சிஜனேற்ற நிலைகளைப் பெற்றுள்ளன.
தொகுதி-3 முதல் 12 வரையில் உள்ள தனிமங்கள் d தொகுதித் தனிமங்கள் அல்லது இடைநிலைத் தனிமங்கள் என்று அழைக்கப்படுகின்றன. இத்தனிமங்களின் பொதுவான இணைதிற கூட்டு எலக்ட்ரான் அமைப்பு ns1-2, (n-1) d1-10 ஆகும். இத்தனிமங்களும் ஒன்றிற்கும் மேற்பட்ட மாறுபடும் ஆக்சிஜனேற்ற நிலைகளைப் பெற்றுள்ளன. இவைகள் அயனிச் சேர்மங்கள், சகப்பிணைப்புச் சேர்மங்கள் மற்றும் ஈதல்சகப்பிணைப்புச் சேர்மங்களை உருவாக்கும் தன்மையினைப் பெற்றுள்ளன. மேலும் இவைகள் அணிக்கோவை இடைச்செருகல் சேர்மங்கள் (interstitial compounds) மற்றும் உலோகக் கலவைகளை உருவாக்குகின்றன. இவற்றின் உலோகக் கலவைகள் வினையூக்கிகளாகவும் செயல்படும் தன்மையினைப் பெற்றுள்ளன. இந்த தனிமங்கள் அதிக உருகுநிலையை பெற்றிருப்பதுடன் வெப்பம் மற்றும் மின்சாரத்தை நன்கு கடத்தும் கடத்திகளாகவும் செயல்படுகின்றன.
லாந்தனைடுகள் (4f1-14, 5d0-1, 6s2) மற்றும் ஆக்டினைடுகள் (5f0-14, 6d0-2, 7s2) ஆகியன f - தொகுதி தனிமங்கள் என்றழைக்கப்படுகின்றன. இத்தகைய தனிமங்கள் உலோகத் தன்மையினையும், அதிக உருக நிலையினையும் கொண்டுள்ளன. இவற்றின் சேர்மங்கள் பெரும்பாலும் நிறமுடையவை. இத்தனிமங்களும் மாறுபட்ட ஆக்சிஜனேற்ற நிலைகளைப் பெற்றுள்ளன.
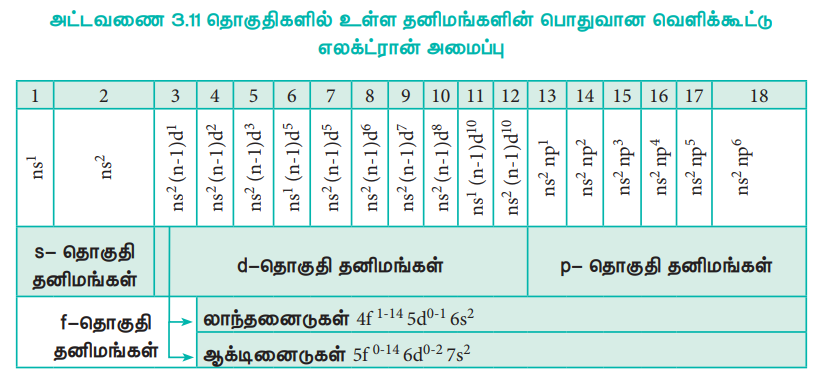
அட்டவணை 3.11 தொகுதிகளில் உள்ள தனிமங்களின் பொதுவான வெளிக்கூட்டு எலக்ட்ரான் அமைப்பு
தன்மதிப்பீடு
3) (n - 1) d2, ns2 (இங்கு n = 5) என்ற எலக்ட்ரான் அமைப்பினை நிறைவு செய்யும் தனிமமானது தனிமவரிசை அட்டவணையில் பெற்றுள்ள இடத்தினைக் கண்டறிக.
தீர்வு
• n = 5 எனவே இத்தனிமம் 5வது வரிசையை சார்ந்ததாகும். மேலும் இதன் வெளிக்கூட்டு எலக்ட்ரான் அமைப்பில் ns ஆர்பிட்டால் முழுவதும் நிரம்பி, (n−1) d ஆர்பிட்டாலில் இரண்டு எலக்ட்ரான்களைப் பெற்று உள்ளதால் 4வது தொகுதியை சேர்ந்த தனிமம் ஆகும். 5வது வரிசை, 4வது தொகுதியைச் சேர்ந்த அத்தனிமம் ஜிர்கோனியம் ஆகும்.