வேதிவினைகளின் வகைகள் - புத்தக வினாக்கள் விடைகள் | 10th Science : Chapter 10 : Types of Chemical Reactions
10வது அறிவியல் : அலகு 10 : வேதிவினைகளின் வகைகள்
புத்தக வினாக்கள் விடைகள்
வேதிவினைகளின் வகைகள்
I சரியான விடையைத் தேர்வு செய்க.
1. H2(g) + Cl2(g) → 2HCl(g) என்பது
அ) சிதைவுறுதல் வினை
ஆ) சேர்க்கை வினை
இ) ஒற்றை இடப்பெயர்ச்சி வினை
ஈ) இரட்டை இடப்பெயர்ச்சி வினை
2. ஒளிச்சிதைவு என்பது இதனால்
நடைபெறும் சிதைவு வினையாகும்
அ) வெப்பம்
ஆ) மின்னாற்றல்
இ) ஒளி
ஈ) எந்திர ஆற்றல்
3. கார்பன் மற்றும் ஆக்ஸிஜன்
இடையேயான ஒரு வினை பின்வருமாறு குறிக்கப்படுகிறது. C(s) + O2(g) → CO2(g) இது எவ்வகை வினையாக வகைப்படுத்தபடுகிறது.
i) சேர்க்கை வினை
ii) எரிதல் வினை
iii) சிதைவுறுதல் வினை
iv) மீளா வினை
அ) (i) மற்றும் (ii)
ஆ) (i) மற்றும் (iv)
இ) (i) (ii) மற்றும் (iii)
ஈ) (i) (ii) மற்றும் (iv)
4. Na2SO4(aq) + BaCl2(aq) → BaSO4(s) ↓ + 2 NaCl(aq)
என்ற வேதிச்சமன்பாடு பின்வருனவற்றுள் எவ்வகை வினையைக்
குறிக்கிறது
அ) நடுநிலையாக்கல் வினை
ஆ) எரிதல் வினை
இ) வீழ்படிவாதல் வினை
ஈ) ஒற்றை இடப்பெயர்ச்சி வினை
5. வேதிச் சமநிலை பற்றிய
பின்வரும் கூற்றுகளில் எவை சரியானவை?
i) இயக்கத்தன்மை உடையது
ii) சமநிலையில் முன்னோக்கு
மற்றும் பின்னோக்கு வினைகளில் வினைவேகம் சமம்
iii) மீளா வினைகள் வேதிச் சமநிலையை
அடைவதில்லை
iv) வினைபடு பொருள் மற்றும்
வினைவிளை பொருள்களில் செறிவு வேறுபடலாம்.
அ) (i), (ii) மற்றும் (iii)
ஆ) (i), (ii) மற்றும் (iv)
இ) (ii), (iii) மற்றும் (iv)
ஈ) (i), (iii) மற்றும் (iv)
6. X(s) + 2HCI(aq) → XCl2(aq) + H2(g) என்ற ஒற்றை
இடப்பெயர்ச்சி வினையில் X என்பது பின்வருவனவற்றுள் எதைக்
குறிக்கிறது
i) Zn
ii) Ag
iii) Cu
iv) Mg
அ) (i) மற்றும் (ii)
ஆ) (ii) மற்றும் (iii)
இ) (iii) மற்றும் (iv)
ஈ) (i) மற்றும் (iv)
7. பின்வருவனவற்றுள் எது “தனிமம்
+ தனிமம் → சேர்மம்” வகை அல்ல?
அ) C(s) + O2(g) → CO2(g)
ஆ) 2K(s) + Br2(1) → 2KBr(s)
இ) 2CO2(g) + O2(g) → 2CO2(g)
ஈ) 4Fe(s) + 3O2(g) → 2Fe2O3(s)
8. பின்வருவனவற்றுள் எது வீழ்படிவாதல் வினையை குறிக்கிறது?
அ) A(s) + B(s) → C(s) + D(s)
ஆ) A(s) + B(aq) → C(aq) + D(1)
இ) A(aq) + B(aq) → C(s) + D(aq)
ஈ) A(aq) + B(s) → C(aq) + D(1)
9. ஒரு கரைசலின் pH மதிப்பு 3 எனில், அதன் (OH-)
ஹைட்ராக்ஸைடு அயனி செறிவு என்ன?
அ) 1 × 10-3M
ஆ) 3M
இ) 1 × 10-11M
ஈ) 11M
10. தூளாக்கப்பட்ட CaCO3, கட்டியான CaCO3 விட தீவிரமாக வினைபுரிகிறது காரணம்
அ) அதிக புறப்பரப்பளவு
ஆ) அதிக அழுத்தம்
இ) அதிக செறிவினால்
ஈ) அதிக வெப்பநிலை
II. கோடிட்ட இடங்களை நிரப்புக.
1. அமிலம் மற்றும் காரத்திற்கு
இடையேயான வினை நடுநிலையாக்கல் வினை என்று அழைக்கப்படுகிறது.
2. ஹைட்ரோகுளோரிக் அமிலத்துடன்
லித்தியம் உலோகம் வினைபுரியும் போது ஹைட்ரஜன் வாயு வெளிவருகிறது
3. பனிக்கட்டி உருகுதல் செயலில்
நிகழும் சமநிலை இயற்பியல் சமநிலை என்று அழைக்கப்படுகிறது.
4. ஒரு பழச்சாறின் pH மதிப்பு 5.6 இதனுடன் நீர்த்த சுண்ணாம்பு
சேர்க்கும்போது இதன் pH மதிப்பு அதிகமாகிறது (அதிகமாகிறது / குறைகிறது)
5. 25°C வெப்பநிலையில் நீரின் அயனிப் பெருக்கத்தின் மதிப்பு 1.00 × 10-14 மோல்2 டெசி.மீ-6
6. மனித இரத்தத்தின் பொதுவான pH
மதிப்பு 7.4 (7.35 - 7.45)
7. மின்னாற்பகுப்பு என்பது சிதைவு வினை வகை வினையாகும்.
8. தொகுப்பு வினைகளில் உருவாகும்
வினை விளை பொருள்களின் எண்ணிக்கை ஒன்று
9. வேதி எரிமலை என்பது வேதிசிதைவுவினை வகை வினைக்கு எடுத்துகாட்டாகும்
10, ஹைடிரஜன் H+
அயனி நீரில் கரைவதால் உருவாகும் அயனி ஹைட்ரோனியம் அயனி என்று அழைக்கப்படுகிறது.
III. பொருத்துக:
வினையின் வகைகளை அடையாளம்
காண்
வினை வகை
1) NH4 OH(aq) + CH3
COOH(aq) → CH3 COONH4(aq) + H2O(I)
– ஒற்றை இடப்பெயர்ச்சி வினை
2) Zn(s) + CuSO4(aq) → ZnSO4(aq) + Cu(s) - எரிதல் வினை
3) ZnCO3(s) வெப்பம் → ZnO(s) + CO2(g) - நடுநிலையாக்கல்
வினை
4) C2H4(g) + 4O2(g)
→ 2CO2(g) + 2H2O(g) + வெப்பம்
- வெப்பச்சிதைவு வினை
விடை:
1) NH4 OH(aq) + CH3 COOH(aq)
→ CH3 COONH4(aq)
+ H2O(I) - எரிதல் வினை
2) Zn(s) + CuSO4(aq) → ZnSO4(aq) + Cu(s) - வெப்பச்சிதைவு
வினை
3) ZnCO3(s) வெப்பம் → ZnO(s) + CO2(g) - ஒற்றை
இடப்பெயர்ச்சி வினை
4) C2H4(g) + 4O2(g) → 2CO2(g) + 2H2O(g)
+ வெப்பம் - நடுநிலையாக்கல்
வினை
IV. சரியா தவறா? தவறு எனில் கூற்றினை திருத்துக.
1. சில்வர் உலோகம் நைட்ரிக்
அமிலத்தில் ஹைட்ரஜன் வாயுவை இடப்பெயர்ச்சி செய்யவல்லது.
விடை: தவறு
சரியான விடை: சோடியம் உலோகம்
நைட்ரிக் அமிலத்தில் ஹைட்ரஜன் வாயுவை இடப்பெயர்ச்சி செய்யவல்லது.
2. SO3, CO2, NO2
போன்ற வாயுக்கள் கரைந்துள்ள மழைநீரின் pH மதிப்பு
7-யை விட குறைவாக இருக்கும்.
விடை: சரி
3. ஒரு மீள்வினையின் சமநிலையில்
வினைவிளை மற்றும் வினைபடு பொருள்களின் செறிவு சமமாக இருக்கும்.
விடை: சரி
4. ஒரு மீள்வினையின் ஏதேனும் ஒரு
வினைவிளை பொருளை அவ்வப்பொழுது நீக்கும் பொழுது அவ்வினையின் விளைச்சல்
அதிகரிக்கிறது.
விடை: சரி
5. pH தாளை ஒரு கரைசலில்
நனைக்கும் பொழுது மஞ்சளாக மாறுகிறது. எனவே அக்கரைசல் காரத்தன்மை கொண்டது.
விடை: தவறு
சரியான விடை: PH தாளை ஒரு
கரைசலில் நனைக்கும் பொழுது மஞ்சளாக மாறுகிறது எனவே அக்கரைசல் அமிலத்தன்மை கொண்டது.
V. குறு வினாக்கள்:
1. பொட்டாசியம் குளோரைடு
நீர்க்கரைசலை சில்வர் நைட்ரேட் நீர்க்கரைசலுடன் சேர்க்கும் பொழுது வெண்மை நிற
வீழ்படிவு உண்டாகிறது. இவ்வினையின் வேதிச் சமன்பாட்டை தருக.
KCl(aq) + AgNO3(aq) → AgCl(s) ↓ + KNO3(aq)
AgCl வெள்ளை வீழ்படிவாக நீர்கரைசலான
KNO3 - ல் கிடைக்கிறது
2. வெப்பநிலையை உயர்த்தும்
பொழுது ஒரு வினையின் வேகம் அதிகரிக்கிறது ஏன்?
வெப்பம் அதிகரிக்கும் பொழுது
வினைபடுபொருள்களின் பிணைப்புகள் எளிதில் உடைந்து அதிக வினைபடு பொருள்களை அயனிகளாக
மாற்றி வினையின் வேகத்தை அதிகரிக்கிறது.
3. சேர்க்கை அல்லது கூடுகை வினை
வரையறு வெப்ப உமிழ் சேர்க்கை வினைக்கு எடுத்துகாட்டு தருக.
இரண்டு (அ) அதற்கு மேற்பட்ட வினைபடு பொருள்கள்
இணைந்து ஒரு சேர்மம் உருவாகும் வினை சேர்க்கை வினை (அ) கூடுகை வினை ஆகும்
S(5) + O2(g) → SO2(g)
திட கந்தகம் ஆக்சிஜனுடன் வினைபுரிந்து கந்தக டை
ஆக்ஸைடாக மாறும்பொழுது வெப்பம் உமிழப்படுகிறது. ஏனெனில் புதிய மூலக்கூறு உருவாகும்
பொழுது பிணைப்பு உருவாகிறது. அப்பொழுது ஆற்றல் வெளிப்படுகிறது.
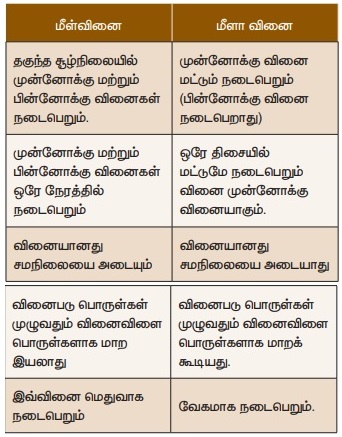
4. மீள் மற்றும் மீளா வினைகளை
வேறுபடுத்துக.
மீள் வினை
அ) தகுந்த சூழ்நிலையில் முன்னோக்கு மற்றும்
பின்னோக்கு வினைகள் நடைபெறும்.
ஆ) முன்னோக்கு மற்றும் பின்னோக்கு வினைகள் ஒரே
நேரத்தில் நடைபெறும்.
இ) வினையானது சமநிலை அடையும்.
ஈ) வினைபடு பொருள்கள் முழுவதும் வினைவிளை
பொருள்களாக மாற இயலாது.
உ) இவ்வினை மெதுவாக நடைபெறும்.
மீளா வினை
அ) முன்னோக்கு வினை மட்டுமே நடைபெறும்.
ஆ) ஒரே திசையில் மட்டுமே நடைபெறும் வினை
முன்னோக்கு வினையாகும்.
இ) வினையானது சமநிலை அடையாது.
ஈ) வினைபடு பொருள்கள்
முழுவதும் வினைவிளை பொருள்களாக மாற கூடியது.
உ) வேகமாக நடைபெறும்.
X. நெடு வினாக்கள் :
1. வெப்பச்சிதைவு வினைகள் என்பது
யாவை?
விடை:
* ஒரு சேர்மம் வெப்பத்தை உட்கொண்டு சிதைவுற்று இரண்டு (அ)
அதற்கு மேற்பட்ட எளிய மூலக்கூறுகளாக சிதைவுறும் வினை வெப்பச் சிதைவு வினை
எனப்படும்.
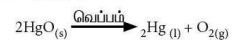
* மெர்குரி II ஆக்ஸைடு வெப்பத்தினால் சிதைவுற்று மெர்குரி மற்றும்
ஆக்சிஜன் வாயுவாக மாறுகிறது. இவ்வினை சேர்மத்திலிருந்து தனிமம் / தனிமம்
சிதைவடைவதல் என்ற வகையைச் சார்ந்தது.
2HgO(s) வெப்பம் →
2Hg(l) + O2(g)
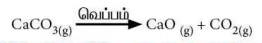
* கால்சியம் கார்பனேட்டை வெப்பப்படுத்தும்போது
சிதைவுற்று கால்சியம் மற்றும் கார்பன் - டை - ஆக்ஸைடாக மாறுகிறது.
* இவ்வினை சேர்மத்திலிருந்து சேர்மம் / சேர்மம்
என்ற வகையைச் சார்ந்தது.
2. இரட்டை இடப்பெயர்ச்சி
வினையின் வகைகளை தகுந்த எடுத்துகாட்டுடன் விளக்குக.
விடை:
இரண்டு சேர்மங்கள் வினைபுரியும் பொழுது
அவற்றின் அயனிகள் பரிமாறிக் கொள்ளப்படுமானால் அவ்வினை இரட்டை இடப்பெயர்ச்சி வினை
எனப்படுகிறது.
அவை இரு வகைப்படும்
i. வீழ்படிவாக்கல் வினை
ii. நடுநிலையாக்கல் வினை
வீழ்படிவாக்கல் வினை
* இரு சேர்மங்களின் நீர்க்கரைசல்களை கலக்கும்
பொழுது, அவை வினைபுரிந்து நீரில்
கரையாத ஒரு விளைபொருளும், நீரில் கரையும் ஒரு விளை பொருளும்
தோன்றினால் அவ்வினை வீழ்படிவாக்கல் வினை எனப்படுகிறது.
* பொட்டாசியம் அயோடைடு லெட் நைட்ரேட்டுடன்
வினைபுரிந்து மஞ்சள் நிற லெட் அயோடைடு சேர்மத்தை வீழ்படிவாக தருகிறது.
Pb (NO3)2(aq) + 2 KI(aq)
→ Pbl2(s) + 2KNO3(sq)
நடுநிலையாக்கல் வினை
இதில் அமிலமும், காரமும் வினைபுரிந்து உப்பையும் நீரையும் தந்து, அமிலத்தன்மையும், காரத்தன்மையும், நடுநிலையாக்கப்படுவதால் இது நடுநிலையாக்கல் வினை எனப்படுகிறது.
சோடியம் ஹைட்ராக்ஸைடு ஹைட்ரோ குளோரிக்
அமிலத்துடன் வினைபுரிந்து, சோடியம் குளோரைடு என்ற நடுநிலையான உப்பு நீரில் கரைந்து கிடைக்கிறது.
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l)
3. ஒரு வினையின் வினை வேகத்தை
பாதிக்கும் காரணிகளை விளக்குக.
விடை:
i) வினைபடு பொருள்களின் தன்மை
சோடியம் ஹைட்ரோகுளோரிக் அமிலத்தைவிட, அசிட்டிக் அமிலத்துடன் மெதுவாக
வினைபுரிகிறது. ஏனென்றால் அசிட்டிக் அமிலம், ஹைட்ரோகுளோரிக்
அமிலத்துடன் வினைதிறன் குறைந்தது. எனவே வினைபடுபொருளின் இயல்பு வினைவேகத்தை
பாதிக்கிறது.
2Na(s) + 2HCl(aq) → 2NaCl(aq) + H2(g) வேகமாக
2Na(s) + 2CH3COOH(aq)
→ 2CH3COONa(aq) + H2(g)
மெதுவாக
ii) வினைபடு பொருள்களின் செறிவு
குறிப்பிட்ட கன அளவு கொண்ட கரைசலில் கரைந்துள்ள
கரைபொருளின் அளவே செறிவு ஆகும். செறிவு அதிகமாக இருக்கும் போது குறிப்பிட்ட கன
அளவில் துகள்களின் எண்ணிக்கை அதிகமாக இருப்பதால், வினையின் வேகமும் அதிகரிக்கும்.
துத்தநாக துகள்கள் 1M HCI ஐ விட 2M HCI ல் வேகமாக வினைபுரியும்
i. வெப்பநிலை
வெப்பநிலை அதிகரிக்கும்போது வினைபடுபொருள்களின்
பிணைப்புகள் எளிதில் உடைந்து வினையின் வேகம் அதிகரிக்கிறது.
அறை வெப்பநிலையில் கால்சியம் கார்பனேட் மெதுவாக
வினைபுரியும். ஆனால் வெப்பப்படுத்தும்போது வினையின் வேகம் அதிகரிக்கும்.
ii. அழுத்தம்
வாயுநிலையிலுள்ள வினைபடுபொருள்களில் அழுத்தம்
அதிகரிக்கும் போது வினையின் வேகம் அதிகரிக்கும். ஏனெனில் அழுத்தத்தை
அதிகரிக்கும்போது வினைபடு பொருள்களின் துகள்கள் மிக அருகே வந்து அடிக்கடி மோதலில்
ஈடுபடுகின்றன.
iii. வினையூக்கி
* வினையூக்கி என்பது வினையில் நேரடியாக
ஈடுபடாமல், வினையின்
வேகத்தை அதிகரிக்கும்.
* பொட்டாசியம் குளோரேட்டை சூடுபடுத்தும் போது ஆக்ஸிஜன்
குறைவாக வெளிவருகிறது. ஆனால் மாங்கனீசு - டை - ஆக்ஸைடை வினைபடு பொருளுடன் சேர்த்த
பிறகு ஆக்ஸிஜனின் வெளியேறும் வேகம் அதிகரிக்கிறது.
iv. வினைபடு பொருள்களின் புறப்பரப்பளவு
* வேதிவினையில் கட்டியான வினைபடுபொருள்களை விட, தூளாக்கப்பட்ட வினைபடுபொருள்களே
விரைவாக வினைபுரியும்.
* கட்டியான கால்சியம் கார்பனேட்டை விட
தூளாக்கப்பட்ட கால்சியம் கார்பனேட் ஹைட்ரோகுளோரிக் அமிலத்துடன் வேகமாக
வினைபுரிகிறது. ஏனெனில் தூளாக்கும் பொழுது புறப்பரப்பளவு அதிகரிக்கிறது.
4. அன்றாட வாழ்வில் pH எவ்வாறு முக்கிய பங்கு வகிக்கிறது?
விடை:
i. விலங்குகள் pH சாந்துள்ள
உணர்வு
நமது உடல் 7.0 முதல் 7.8 வரை உள்ள pH எல்லையை சார்ந்து வேலை செய்கிறது. நம் உடலில் உள்ள திரவங்கள் வெவ்வெறு pH
மதிப்புகளை கொண்டவை. எடுத்துகாட்டாக மனித இரத்தத்தின் PH மதிப்பு 7.35 லிருந்து 7.45
ஆகும். இந்த மதிப்பிலிருந்து குறைந்தாலோ (அ) அதிகரித்தாலோ, அது
நோயை உண்டாக்கும்.
ii. மனித செரிமான மண்டலத்தில் pH மதிப்பு
நமது இரைப்பை ஹைட்ரோ குளோரிக் அமிலத்தை
சுரக்கிறது. இது இரைப்பையை பாதிக்காமல் உணவை செரிக்க உதவுகிறது. சரியான செரிமானம்
இல்லாதபோது இரைப்பையானது கூடுதலான அமிலத்தை சுரந்து வலியையும், எரிச்சலையும் ஏற்படுத்துகிறது.
இத்திரவத்தின் தோராயமான pH மதிப்பு 2.0
ஆகும்
iii. மண்ணின் pH மதிப்பு
சிட்ரிக் அமிலம் கொண்ட பழங்கள் சற்று
காரத்தன்மை உள்ள மண்ணிலும், நெல் அமிலத்தன்மை கொண்ட மண்ணிலும், கரும்பு
நடுநிலைத்தன்மை கொண்ட மண்ணிலும் வளரும்.
iv. மழைநீரின் pH மதிப்பு
மழைநீரின் pH மதிப்பு ஏறக்குறைய 7 ஆகும். இது
நடுநிலைத்தன்மை கொண்டது, ஆனால் சல்பர் - டை - ஆக்ஸைடு,
நைட்ரஜன் ஆக்ஸைடு போன்ற மாசுக்கள் மழைநீரில் கரைந்து அதன் PH
மதிப்பை 7-ல் இருந்து குறைக்கிறது. இது அமில
மழை எனப்படுகிறது. இந்த அமில மழைநீர் ஆறுகளில் சேரும்பொழுது அவற்றின் pH குறைந்து, நீர்வாழ் உயிர்களின் வாழ்வு
பாதிக்கப்படுகிறது.
5. வேதிச் சமநிலை என்றால் என்ன?
அதன் பண்புகள் யாவை?
விடை:
வேதிச்சமநிலை என்பது ஒரு மீள்வேதிவினையின் வினைபடுபொருள்
மற்றும் வினைவிளை பொருளின் செறிவில் எந்த மாற்றமும் நிகழாத நிலை ஆகும்.
முன்னோக்கு வினையின் வேகம் = பின்னோக்கு
வினையின் வேகம்
சமநிலையின் பண்புகள்:
* வேதிச்சமநிலையில் முன்னோக்கு வினையின் வேகமும், பின்னோக்கு வினையின் வேகமும்,
சமம்.
* நேரத்தை பொருத்து அழுத்தம், செறிவு, நிறம்,
அடர்த்தி, பாகுநிலை போன்றவை மாறாது.
* வேதிச்சமநிலை என்பது ஒரு இயங்குச் சமநிலை
ஏனெனில் முன்னோக்கு வினையும், பின்னோக்கு வினையும் தொடர்ந்து நிலையாக நடந்து கொண்டிருக்கும்.
* இயற்பியல் சமநிலையில், அனைத்து நிலைமைகளும் மாறாத கன
அளவைப் பெறுகின்றன.
XI. உயர் சிந்தனைக்கான வினாக்கள் : (HOTS)
1. 'A' என்ற திண்மச் சேர்மத்தை
வெப்பப்படுத்தும்பொழுது சிதைந்து 'B' மற்றும் 'C' என்ற வாயுவைத் தருகிறது. 'C' என்ற வாயுவை நீரில்
செலுத்தும்போது அமிலத்தன்மையாக மாறுகிறது. A,B, மற்றும் 'C’
- ஐ கண்டறிக.
'C’ யை நீரில் செலுத்தும் போது
அமிலத்தன்மையாக மாறுகிறது. எனவே 'C' என்பது அலோக ஆக்சைடாக
இருக்க வேண்டும். அதாவது CO2. 'A' என்ற சேர்மம் கால்சியம் கார்பனேட்டாக இருக்க
வேண்டும். கால்சியம் கார்பனேட் சிதைவுற்று கால்சியம் ஆக்ஸைடு மற்றும் கார்பன் - டை
- ஆக்ஸைடை தருகிறது.
CaCO3(s) → CaO(s) + CO2(g)
A B
C
A : CaCO3 : கால்சியம் கார்பனேட்
B : CaO : கால்சியம் ஆக்ஸைடு
C : CO2 : கார்பன் - டை – ஆக்ஸைடு
2. காப்பர் சல்பேட் கரைசலை
கலக்குவதற்கு நிக்கல் கரண்டியை பயன்படுத்தலாமா? உனது கூற்றை
நியாயப்படுத்துக.
பயன்படுத்த கூடாது, ஏனெனில் நிக்கல், காப்பரை விட அதிக வினைதிறன் கொண்டது. எனவே நிக்கல் காப்பரை இடப்பெயர்ச்சி
செய்து நிக்கல் சல்பேட்டையும், காப்பரையும் தரும்.
XII. கணக்கீடுகள் :
1. எலுமிச்சை சாறின் pH மதிப்பு 2 எனில் அதன் ஹைட்ரஜன் அயனியின் செறிவின்
மதிப்பு என்ன?
ஹைட்ரஜன் அயனியின் செறிவு H+ = 10-PH M
எலுமிச்சை சாறின் ஹைட்ரஜன் அயனியின் செறிவு =10-2M
எலுமிச்சை சாற்றில் ஹைட்ரஜன் அயனியின் செறிவு =
0.01 M
எலுமிச்சை சாற்றில் ஹைட்ரஜன் அயனியின் செறிவு =
0.01 M
2. 1.0 × 10-4 மோலார்
செறிவுள்ள HNO3 கரைசலின் pH மதிப்பை கணக்கிடுக.
நீரில் HNO3 பிரியும் முறை
HNO3(I) → H+(aq) + NO-3(aq)
கரைசலில் ஒரு மோல் நைட்ரிக் அமிலம், ஒரு H+ அயனியை தருகிறது. எனவே 1.0 × 10-4 மோல்
நைட்ரிக் அமிலம் 1.0 × 10-4 மோல் H+
அயனியை தருகிறது.
[H+] = 1.0 × 10-4 மோல் லிட்டர்-1
pH = -log10 [H+]
= - (-4) log10 × 10-4
= 4 × 1
pH = 4
1.0 × 10-4 மோலார்
செறிவுள்ள HNO3 கரைசலின் pH மதிப்பு 4
3. 1.0 × 10-5 மோலார்
செறிவுள்ள KOH கரைசலின் pH மதிப்பை
காண்க.
KOH நீரில் பிரியும் முறை
KOH(aq) → K+(aq) + OH-(aq)
ஒரு மோல் KOH ஒரு OH- அயனியை
தருகிறது எனவே 1.0 x 10-5 மோலார் செறிவுள்ள KOH
1.0 × 10-5OH- அயனியை தரும்.
[OH-] = 1.0 × 10-5 மோல் லிட்டர்-1
POH = -log10[OH-]
POH = -log10 1.0 × 10-5
= - (-5) log1010
= 5 × 1
POH = 5
PH = 14 - POH pH + pOH = 14
pH = 14 – 5
pH = 9
1.0 × 10-5 மோலார்
செறிவுள்ள KOH கரைசலின் pH மதிப்பு 9
4. ஒரு கரைசலின் ஹைட்ராக்ஸைடு
அயனிச் செறிவு 1.0 x 10-11 மோல் எனில் அதன் pH
மதிப்பு என்ன?
[OH-] = 1.0 × 10-11 மோல்
POH = - log10[OH-]
= -log10 1.0 × 10-11
= - (-11) log1010
= 11 × 1
POH = 11
pH = 14 – POH pH + pOH = 14
pH = 14 – 11
pH = 3
ஒரு கரைசலில் ஹைட்ராக்ஸைடு அயனிச் செறிவு 1.0 x 10-11 மோல்
எனில் அதன் pH மதிப்பு 3
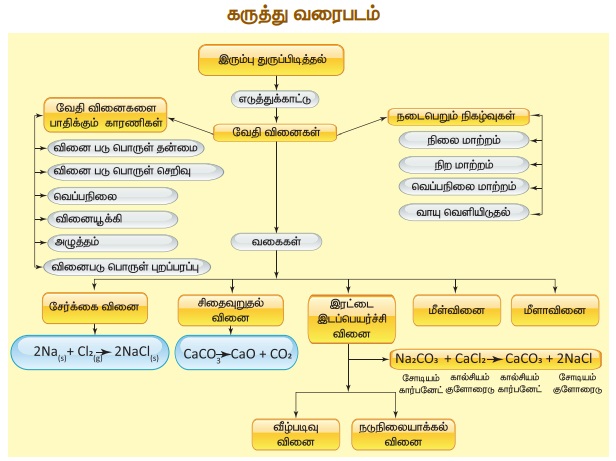
வேதிவினைகளின் வகைகள்
I சரியான விடையைத் தேர்வு செய்க.
1. H2(g) + Cl2(g) → 2HCl(g) என்பது
அ) சிதைவுறுதல் வினை
ஆ) சேர்க்கை வினை
இ) ஒற்றை இடப்பெயர்ச்சி வினை
ஈ) இரட்டை இடப்பெயர்ச்சி வினை
2. ஒளிச்சிதைவு என்பது இதனால்
நடைபெறும் சிதைவு வினையாகும்
அ) வெப்பம்
ஆ) மின்னாற்றல்
இ) ஒளி
ஈ) எந்திர ஆற்றல்
3. கார்பன் மற்றும் ஆக்ஸிஜன்
இடையேயான ஒரு வினை பின்வருமாறு குறிக்கப்படுகிறது. C(s) + O2(g) → CO2(g) இது எவ்வகை வினையாக வகைப்படுத்தபடுகிறது.
i) சேர்க்கை வினை
ii) எரிதல் வினை
iii) சிதைவுறுதல் வினை
iv) மீளா வினை
அ) (i) மற்றும் (ii)
ஆ) (i) மற்றும் (iv)
இ) (i) (ii) மற்றும் (iii)
ஈ) (i) (ii) மற்றும் (iv)
4. Na2SO4(aq) + BaCl2(aq) → BaSO4(s) ↓ + 2 NaCl(aq)
என்ற வேதிச்சமன்பாடு பின்வருனவற்றுள் எவ்வகை வினையைக்
குறிக்கிறது
அ) நடுநிலையாக்கல் வினை
ஆ) எரிதல் வினை
இ) வீழ்படிவாதல் வினை
ஈ) ஒற்றை இடப்பெயர்ச்சி வினை
5. வேதிச் சமநிலை பற்றிய
பின்வரும் கூற்றுகளில் எவை சரியானவை?
i) இயக்கத்தன்மை உடையது
ii) சமநிலையில் முன்னோக்கு
மற்றும் பின்னோக்கு வினைகளில் வினைவேகம் சமம்
iii) மீளா வினைகள் வேதிச் சமநிலையை
அடைவதில்லை
iv) வினைபடு பொருள் மற்றும்
வினைவிளை பொருள்களில் செறிவு வேறுபடலாம்.
அ) (i), (ii) மற்றும் (iii)
ஆ) (i), (ii) மற்றும் (iv)
இ) (ii), (iii) மற்றும் (iv)
ஈ) (i), (iii) மற்றும் (iv)
6. X(s) + 2HCI(aq) → XCl2(aq) + H2(g) என்ற ஒற்றை
இடப்பெயர்ச்சி வினையில் X என்பது பின்வருவனவற்றுள் எதைக்
குறிக்கிறது
i) Zn
ii) Ag
iii) Cu
iv) Mg
அ) (i) மற்றும் (ii)
ஆ) (ii) மற்றும் (iii)
இ) (iii) மற்றும் (iv)
ஈ) (i) மற்றும் (iv)
7. பின்வருவனவற்றுள் எது “தனிமம்
+ தனிமம் → சேர்மம்” வகை அல்ல?
அ) C(s) + O2(g) → CO2(g)
ஆ) 2K(s) + Br2(1) → 2KBr(s)
இ) 2CO2(g) + O2(g) → 2CO2(g)
ஈ) 4Fe(s) + 3O2(g) → 2Fe2O3(s)
8. பின்வருவனவற்றுள் எது வீழ்படிவாதல் வினையை குறிக்கிறது?
அ) A(s) + B(s) → C(s) + D(s)
ஆ) A(s) + B(aq) → C(aq) + D(1)
இ) A(aq) + B(aq) → C(s) + D(aq)
ஈ) A(aq) + B(s) → C(aq) + D(1)
9. ஒரு கரைசலின் pH மதிப்பு 3 எனில், அதன் (OH-)
ஹைட்ராக்ஸைடு அயனி செறிவு என்ன?
அ) 1 × 10-3M
ஆ) 3M
இ) 1 × 10-11M
ஈ) 11M
10. தூளாக்கப்பட்ட CaCO3, கட்டியான CaCO3 விட தீவிரமாக வினைபுரிகிறது காரணம்
அ) அதிக புறப்பரப்பளவு
ஆ) அதிக அழுத்தம்
இ) அதிக செறிவினால்
ஈ) அதிக வெப்பநிலை
II. கோடிட்ட இடங்களை நிரப்புக.
1. அமிலம் மற்றும் காரத்திற்கு
இடையேயான வினை நடுநிலையாக்கல் வினை என்று அழைக்கப்படுகிறது.
2. ஹைட்ரோகுளோரிக் அமிலத்துடன்
லித்தியம் உலோகம் வினைபுரியும் போது ஹைட்ரஜன் வாயு வெளிவருகிறது
3. பனிக்கட்டி உருகுதல் செயலில்
நிகழும் சமநிலை இயற்பியல் சமநிலை என்று அழைக்கப்படுகிறது.
4. ஒரு பழச்சாறின் pH மதிப்பு 5.6 இதனுடன் நீர்த்த சுண்ணாம்பு
சேர்க்கும்போது இதன் pH மதிப்பு அதிகமாகிறது (அதிகமாகிறது / குறைகிறது)
5. 25°C வெப்பநிலையில் நீரின் அயனிப் பெருக்கத்தின் மதிப்பு 1.00 × 10-14 மோல்2 டெசி.மீ-6
6. மனித இரத்தத்தின் பொதுவான pH
மதிப்பு 7.4 (7.35 - 7.45)
7. மின்னாற்பகுப்பு என்பது சிதைவு வினை வகை வினையாகும்.
8. தொகுப்பு வினைகளில் உருவாகும்
வினை விளை பொருள்களின் எண்ணிக்கை ஒன்று
9. வேதி எரிமலை என்பது வேதிசிதைவுவினை வகை வினைக்கு எடுத்துகாட்டாகும்
10, ஹைடிரஜன் H+
அயனி நீரில் கரைவதால் உருவாகும் அயனி ஹைட்ரோனியம் அயனி என்று அழைக்கப்படுகிறது.
III. பொருத்துக:
வினையின் வகைகளை அடையாளம்
காண்
வினை வகை
1) NH4 OH(aq) + CH3
COOH(aq) → CH3 COONH4(aq) + H2O(I)
– ஒற்றை இடப்பெயர்ச்சி வினை
2) Zn(s) + CuSO4(aq) → ZnSO4(aq) + Cu(s) - எரிதல் வினை
3) ZnCO3(s) வெப்பம் → ZnO(s) + CO2(g) - நடுநிலையாக்கல்
வினை
4) C2H4(g) + 4O2(g)
→ 2CO2(g) + 2H2O(g) + வெப்பம்
- வெப்பச்சிதைவு வினை
விடை:
1) NH4 OH(aq) + CH3 COOH(aq)
→ CH3 COONH4(aq)
+ H2O(I) - எரிதல் வினை
2) Zn(s) + CuSO4(aq) → ZnSO4(aq) + Cu(s) - வெப்பச்சிதைவு
வினை
3) ZnCO3(s) வெப்பம் → ZnO(s) + CO2(g) - ஒற்றை
இடப்பெயர்ச்சி வினை
4) C2H4(g) + 4O2(g) → 2CO2(g) + 2H2O(g)
+ வெப்பம் - நடுநிலையாக்கல்
வினை
IV. சரியா தவறா? தவறு எனில் கூற்றினை திருத்துக.
1. சில்வர் உலோகம் நைட்ரிக்
அமிலத்தில் ஹைட்ரஜன் வாயுவை இடப்பெயர்ச்சி செய்யவல்லது.
விடை: தவறு
சரியான விடை: சோடியம் உலோகம்
நைட்ரிக் அமிலத்தில் ஹைட்ரஜன் வாயுவை இடப்பெயர்ச்சி செய்யவல்லது.
2. SO3, CO2, NO2
போன்ற வாயுக்கள் கரைந்துள்ள மழைநீரின் pH மதிப்பு
7-யை விட குறைவாக இருக்கும்.
விடை: சரி
3. ஒரு மீள்வினையின் சமநிலையில்
வினைவிளை மற்றும் வினைபடு பொருள்களின் செறிவு சமமாக இருக்கும்.
விடை: சரி
4. ஒரு மீள்வினையின் ஏதேனும் ஒரு
வினைவிளை பொருளை அவ்வப்பொழுது நீக்கும் பொழுது அவ்வினையின் விளைச்சல்
அதிகரிக்கிறது.
விடை: சரி
5. pH தாளை ஒரு கரைசலில்
நனைக்கும் பொழுது மஞ்சளாக மாறுகிறது. எனவே அக்கரைசல் காரத்தன்மை கொண்டது.
விடை: தவறு
சரியான விடை: PH தாளை ஒரு
கரைசலில் நனைக்கும் பொழுது மஞ்சளாக மாறுகிறது எனவே அக்கரைசல் அமிலத்தன்மை கொண்டது.
V. குறு வினாக்கள்:
1. பொட்டாசியம் குளோரைடு
நீர்க்கரைசலை சில்வர் நைட்ரேட் நீர்க்கரைசலுடன் சேர்க்கும் பொழுது வெண்மை நிற
வீழ்படிவு உண்டாகிறது. இவ்வினையின் வேதிச் சமன்பாட்டை தருக.
KCl(aq) + AgNO3(aq) → AgCl(s) ↓ + KNO3(aq)
AgCl வெள்ளை வீழ்படிவாக நீர்கரைசலான
KNO3 - ல் கிடைக்கிறது
2. வெப்பநிலையை உயர்த்தும்
பொழுது ஒரு வினையின் வேகம் அதிகரிக்கிறது ஏன்?
வெப்பம் அதிகரிக்கும் பொழுது
வினைபடுபொருள்களின் பிணைப்புகள் எளிதில் உடைந்து அதிக வினைபடு பொருள்களை அயனிகளாக
மாற்றி வினையின் வேகத்தை அதிகரிக்கிறது.
3. சேர்க்கை அல்லது கூடுகை வினை
வரையறு வெப்ப உமிழ் சேர்க்கை வினைக்கு எடுத்துகாட்டு தருக.
இரண்டு (அ) அதற்கு மேற்பட்ட வினைபடு பொருள்கள்
இணைந்து ஒரு சேர்மம் உருவாகும் வினை சேர்க்கை வினை (அ) கூடுகை வினை ஆகும்
S(5) + O2(g) → SO2(g)
திட கந்தகம் ஆக்சிஜனுடன் வினைபுரிந்து கந்தக டை
ஆக்ஸைடாக மாறும்பொழுது வெப்பம் உமிழப்படுகிறது. ஏனெனில் புதிய மூலக்கூறு உருவாகும்
பொழுது பிணைப்பு உருவாகிறது. அப்பொழுது ஆற்றல் வெளிப்படுகிறது.
4. மீள் மற்றும் மீளா வினைகளை
வேறுபடுத்துக.
மீள் வினை
அ) தகுந்த சூழ்நிலையில் முன்னோக்கு மற்றும்
பின்னோக்கு வினைகள் நடைபெறும்.
ஆ) முன்னோக்கு மற்றும் பின்னோக்கு வினைகள் ஒரே
நேரத்தில் நடைபெறும்.
இ) வினையானது சமநிலை அடையும்.
ஈ) வினைபடு பொருள்கள் முழுவதும் வினைவிளை
பொருள்களாக மாற இயலாது.
உ) இவ்வினை மெதுவாக நடைபெறும்.
மீளா வினை
அ) முன்னோக்கு வினை மட்டுமே நடைபெறும்.
ஆ) ஒரே திசையில் மட்டுமே நடைபெறும் வினை
முன்னோக்கு வினையாகும்.
இ) வினையானது சமநிலை அடையாது.
ஈ) வினைபடு பொருள்கள்
முழுவதும் வினைவிளை பொருள்களாக மாற கூடியது.
உ) வேகமாக நடைபெறும்.

X. நெடு வினாக்கள் :
1. வெப்பச்சிதைவு வினைகள் என்பது
யாவை?
விடை:
* ஒரு சேர்மம் வெப்பத்தை உட்கொண்டு சிதைவுற்று இரண்டு (அ)
அதற்கு மேற்பட்ட எளிய மூலக்கூறுகளாக சிதைவுறும் வினை வெப்பச் சிதைவு வினை
எனப்படும்.
* மெர்குரி II ஆக்ஸைடு வெப்பத்தினால் சிதைவுற்று மெர்குரி மற்றும்
ஆக்சிஜன் வாயுவாக மாறுகிறது. இவ்வினை சேர்மத்திலிருந்து தனிமம் / தனிமம்
சிதைவடைவதல் என்ற வகையைச் சார்ந்தது.
2HgO(s) வெப்பம் → 2Hg(l) + O2(g)

* கால்சியம் கார்பனேட்டை வெப்பப்படுத்தும்போது
சிதைவுற்று கால்சியம் மற்றும் கார்பன் - டை - ஆக்ஸைடாக மாறுகிறது.
* இவ்வினை சேர்மத்திலிருந்து சேர்மம் / சேர்மம்
என்ற வகையைச் சார்ந்தது.

2. இரட்டை இடப்பெயர்ச்சி
வினையின் வகைகளை தகுந்த எடுத்துகாட்டுடன் விளக்குக.
விடை:
இரண்டு சேர்மங்கள் வினைபுரியும் பொழுது
அவற்றின் அயனிகள் பரிமாறிக் கொள்ளப்படுமானால் அவ்வினை இரட்டை இடப்பெயர்ச்சி வினை
எனப்படுகிறது.
அவை இரு வகைப்படும்
i. வீழ்படிவாக்கல் வினை
ii. நடுநிலையாக்கல் வினை
வீழ்படிவாக்கல் வினை
* இரு சேர்மங்களின் நீர்க்கரைசல்களை கலக்கும்
பொழுது, அவை வினைபுரிந்து நீரில்
கரையாத ஒரு விளைபொருளும், நீரில் கரையும் ஒரு விளை பொருளும்
தோன்றினால் அவ்வினை வீழ்படிவாக்கல் வினை எனப்படுகிறது.
* பொட்டாசியம் அயோடைடு லெட் நைட்ரேட்டுடன்
வினைபுரிந்து மஞ்சள் நிற லெட் அயோடைடு சேர்மத்தை வீழ்படிவாக தருகிறது.
Pb (NO3)2(aq) + 2 KI(aq)
→ Pbl2(s) + 2KNO3(sq)
நடுநிலையாக்கல் வினை
இதில் அமிலமும், காரமும் வினைபுரிந்து உப்பையும் நீரையும் தந்து, அமிலத்தன்மையும், காரத்தன்மையும், நடுநிலையாக்கப்படுவதால் இது நடுநிலையாக்கல் வினை எனப்படுகிறது.
சோடியம் ஹைட்ராக்ஸைடு ஹைட்ரோ குளோரிக்
அமிலத்துடன் வினைபுரிந்து, சோடியம் குளோரைடு என்ற நடுநிலையான உப்பு நீரில் கரைந்து கிடைக்கிறது.
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l)
3. ஒரு வினையின் வினை வேகத்தை
பாதிக்கும் காரணிகளை விளக்குக.
விடை:
i) வினைபடு பொருள்களின் தன்மை
சோடியம் ஹைட்ரோகுளோரிக் அமிலத்தைவிட, அசிட்டிக் அமிலத்துடன் மெதுவாக
வினைபுரிகிறது. ஏனென்றால் அசிட்டிக் அமிலம், ஹைட்ரோகுளோரிக்
அமிலத்துடன் வினைதிறன் குறைந்தது. எனவே வினைபடுபொருளின் இயல்பு வினைவேகத்தை
பாதிக்கிறது.
2Na(s) + 2HCl(aq) → 2NaCl(aq) + H2(g) வேகமாக
2Na(s) + 2CH3COOH(aq)
→ 2CH3COONa(aq) + H2(g)
மெதுவாக
ii) வினைபடு பொருள்களின் செறிவு
குறிப்பிட்ட கன அளவு கொண்ட கரைசலில் கரைந்துள்ள
கரைபொருளின் அளவே செறிவு ஆகும். செறிவு அதிகமாக இருக்கும் போது குறிப்பிட்ட கன
அளவில் துகள்களின் எண்ணிக்கை அதிகமாக இருப்பதால், வினையின் வேகமும் அதிகரிக்கும்.
துத்தநாக துகள்கள் 1M HCI ஐ விட 2M HCI ல் வேகமாக வினைபுரியும்
i. வெப்பநிலை
வெப்பநிலை அதிகரிக்கும்போது வினைபடுபொருள்களின்
பிணைப்புகள் எளிதில் உடைந்து வினையின் வேகம் அதிகரிக்கிறது.
அறை வெப்பநிலையில் கால்சியம் கார்பனேட் மெதுவாக
வினைபுரியும். ஆனால் வெப்பப்படுத்தும்போது வினையின் வேகம் அதிகரிக்கும்.
ii. அழுத்தம்
வாயுநிலையிலுள்ள வினைபடுபொருள்களில் அழுத்தம்
அதிகரிக்கும் போது வினையின் வேகம் அதிகரிக்கும். ஏனெனில் அழுத்தத்தை
அதிகரிக்கும்போது வினைபடு பொருள்களின் துகள்கள் மிக அருகே வந்து அடிக்கடி மோதலில்
ஈடுபடுகின்றன.
iii. வினையூக்கி
* வினையூக்கி என்பது வினையில் நேரடியாக
ஈடுபடாமல், வினையின்
வேகத்தை அதிகரிக்கும்.
* பொட்டாசியம் குளோரேட்டை சூடுபடுத்தும் போது ஆக்ஸிஜன்
குறைவாக வெளிவருகிறது. ஆனால் மாங்கனீசு - டை - ஆக்ஸைடை வினைபடு பொருளுடன் சேர்த்த
பிறகு ஆக்ஸிஜனின் வெளியேறும் வேகம் அதிகரிக்கிறது.
iv. வினைபடு பொருள்களின் புறப்பரப்பளவு
* வேதிவினையில் கட்டியான வினைபடுபொருள்களை விட, தூளாக்கப்பட்ட வினைபடுபொருள்களே
விரைவாக வினைபுரியும்.
* கட்டியான கால்சியம் கார்பனேட்டை விட
தூளாக்கப்பட்ட கால்சியம் கார்பனேட் ஹைட்ரோகுளோரிக் அமிலத்துடன் வேகமாக
வினைபுரிகிறது. ஏனெனில் தூளாக்கும் பொழுது புறப்பரப்பளவு அதிகரிக்கிறது.
4. அன்றாட வாழ்வில் pH எவ்வாறு முக்கிய பங்கு வகிக்கிறது?
விடை:
i. விலங்குகள் pH சாந்துள்ள
உணர்வு
நமது உடல் 7.0 முதல் 7.8 வரை உள்ள pH எல்லையை சார்ந்து வேலை செய்கிறது. நம் உடலில் உள்ள திரவங்கள் வெவ்வெறு pH
மதிப்புகளை கொண்டவை. எடுத்துகாட்டாக மனித இரத்தத்தின் PH மதிப்பு 7.35 லிருந்து 7.45
ஆகும். இந்த மதிப்பிலிருந்து குறைந்தாலோ (அ) அதிகரித்தாலோ, அது
நோயை உண்டாக்கும்.
ii. மனித செரிமான மண்டலத்தில் pH மதிப்பு
நமது இரைப்பை ஹைட்ரோ குளோரிக் அமிலத்தை
சுரக்கிறது. இது இரைப்பையை பாதிக்காமல் உணவை செரிக்க உதவுகிறது. சரியான செரிமானம்
இல்லாதபோது இரைப்பையானது கூடுதலான அமிலத்தை சுரந்து வலியையும், எரிச்சலையும் ஏற்படுத்துகிறது.
இத்திரவத்தின் தோராயமான pH மதிப்பு 2.0
ஆகும்
iii. மண்ணின் pH மதிப்பு
சிட்ரிக் அமிலம் கொண்ட பழங்கள் சற்று
காரத்தன்மை உள்ள மண்ணிலும், நெல் அமிலத்தன்மை கொண்ட மண்ணிலும், கரும்பு
நடுநிலைத்தன்மை கொண்ட மண்ணிலும் வளரும்.
iv. மழைநீரின் pH மதிப்பு
மழைநீரின் pH மதிப்பு ஏறக்குறைய 7 ஆகும். இது
நடுநிலைத்தன்மை கொண்டது, ஆனால் சல்பர் - டை - ஆக்ஸைடு,
நைட்ரஜன் ஆக்ஸைடு போன்ற மாசுக்கள் மழைநீரில் கரைந்து அதன் PH
மதிப்பை 7-ல் இருந்து குறைக்கிறது. இது அமில
மழை எனப்படுகிறது. இந்த அமில மழைநீர் ஆறுகளில் சேரும்பொழுது அவற்றின் pH குறைந்து, நீர்வாழ் உயிர்களின் வாழ்வு
பாதிக்கப்படுகிறது.
5. வேதிச் சமநிலை என்றால் என்ன?
அதன் பண்புகள் யாவை?
விடை:
வேதிச்சமநிலை என்பது ஒரு மீள்வேதிவினையின் வினைபடுபொருள்
மற்றும் வினைவிளை பொருளின் செறிவில் எந்த மாற்றமும் நிகழாத நிலை ஆகும்.
முன்னோக்கு வினையின் வேகம் = பின்னோக்கு
வினையின் வேகம்
சமநிலையின் பண்புகள்:
* வேதிச்சமநிலையில் முன்னோக்கு வினையின் வேகமும், பின்னோக்கு வினையின் வேகமும்,
சமம்.
* நேரத்தை பொருத்து அழுத்தம், செறிவு, நிறம்,
அடர்த்தி, பாகுநிலை போன்றவை மாறாது.
* வேதிச்சமநிலை என்பது ஒரு இயங்குச் சமநிலை
ஏனெனில் முன்னோக்கு வினையும், பின்னோக்கு வினையும் தொடர்ந்து நிலையாக நடந்து கொண்டிருக்கும்.
* இயற்பியல் சமநிலையில், அனைத்து நிலைமைகளும் மாறாத கன
அளவைப் பெறுகின்றன.
XI. உயர் சிந்தனைக்கான வினாக்கள் : (HOTS)
1. 'A' என்ற திண்மச் சேர்மத்தை
வெப்பப்படுத்தும்பொழுது சிதைந்து 'B' மற்றும் 'C' என்ற வாயுவைத் தருகிறது. 'C' என்ற வாயுவை நீரில்
செலுத்தும்போது அமிலத்தன்மையாக மாறுகிறது. A,B, மற்றும் 'C’
- ஐ கண்டறிக.
'C’ யை நீரில் செலுத்தும் போது
அமிலத்தன்மையாக மாறுகிறது. எனவே 'C' என்பது அலோக ஆக்சைடாக
இருக்க வேண்டும். அதாவது CO2. 'A' என்ற சேர்மம் கால்சியம் கார்பனேட்டாக இருக்க
வேண்டும். கால்சியம் கார்பனேட் சிதைவுற்று கால்சியம் ஆக்ஸைடு மற்றும் கார்பன் - டை
- ஆக்ஸைடை தருகிறது.
CaCO3(s) → CaO(s) + CO2(g)
A B
C
A : CaCO3 : கால்சியம் கார்பனேட்
B : CaO : கால்சியம் ஆக்ஸைடு
C : CO2 : கார்பன் - டை – ஆக்ஸைடு
2. காப்பர் சல்பேட் கரைசலை
கலக்குவதற்கு நிக்கல் கரண்டியை பயன்படுத்தலாமா? உனது கூற்றை
நியாயப்படுத்துக.
பயன்படுத்த கூடாது, ஏனெனில் நிக்கல், காப்பரை விட அதிக வினைதிறன் கொண்டது. எனவே நிக்கல் காப்பரை இடப்பெயர்ச்சி
செய்து நிக்கல் சல்பேட்டையும், காப்பரையும் தரும்.
XII. கணக்கீடுகள் :
1. எலுமிச்சை சாறின் pH மதிப்பு 2 எனில் அதன் ஹைட்ரஜன் அயனியின் செறிவின்
மதிப்பு என்ன?
ஹைட்ரஜன் அயனியின் செறிவு H+ = 10-PH M
எலுமிச்சை சாறின் ஹைட்ரஜன் அயனியின் செறிவு =10-2M
எலுமிச்சை சாற்றில் ஹைட்ரஜன் அயனியின் செறிவு =
0.01 M
எலுமிச்சை சாற்றில் ஹைட்ரஜன் அயனியின் செறிவு =
0.01 M
2. 1.0 × 10-4 மோலார்
செறிவுள்ள HNO3 கரைசலின் pH மதிப்பை கணக்கிடுக.
நீரில் HNO3 பிரியும் முறை
HNO3(I) → H+(aq) + NO-3(aq)
கரைசலில் ஒரு மோல் நைட்ரிக் அமிலம், ஒரு H+ அயனியை தருகிறது. எனவே 1.0 × 10-4 மோல்
நைட்ரிக் அமிலம் 1.0 × 10-4 மோல் H+
அயனியை தருகிறது.
[H+] = 1.0 × 10-4 மோல் லிட்டர்-1
pH = -log10 [H+]
= - (-4) log10 × 10-4
= 4 × 1
pH = 4
1.0 × 10-4 மோலார்
செறிவுள்ள HNO3 கரைசலின் pH மதிப்பு 4
3. 1.0 × 10-5 மோலார்
செறிவுள்ள KOH கரைசலின் pH மதிப்பை
காண்க.
KOH நீரில் பிரியும் முறை
KOH(aq) → K+(aq) + OH-(aq)
ஒரு மோல் KOH ஒரு OH- அயனியை
தருகிறது எனவே 1.0 x 10-5 மோலார் செறிவுள்ள KOH
1.0 × 10-5OH- அயனியை தரும்.
[OH-] = 1.0 × 10-5 மோல் லிட்டர்-1
POH = -log10[OH-]
POH = -log10 1.0 × 10-5
= - (-5) log1010
= 5 × 1
POH = 5
PH = 14 - POH pH + pOH = 14
pH = 14 – 5
pH = 9
1.0 × 10-5 மோலார்
செறிவுள்ள KOH கரைசலின் pH மதிப்பு 9
4. ஒரு கரைசலின் ஹைட்ராக்ஸைடு
அயனிச் செறிவு 1.0 x 10-11 மோல் எனில் அதன் pH
மதிப்பு என்ன?
[OH-] = 1.0 × 10-11 மோல்
POH = - log10[OH-]
= -log10 1.0 × 10-11
= - (-11) log1010
= 11 × 1
POH = 11
pH = 14 – POH pH + pOH = 14
pH = 14 – 11
pH = 3
ஒரு கரைசலில் ஹைட்ராக்ஸைடு அயனிச் செறிவு 1.0 x 10-11 மோல்
எனில் அதன் pH மதிப்பு 3
