கலவினைகளின் வெப்ப இயக்கவியல் | மின் வேதியியல் - நெர்ன்ஸ்ட் சமன்பாடு | 12th Chemistry : UNIT 9 : Electro Chemistry
12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 9 : மின் வேதியியல்
நெர்ன்ஸ்ட் சமன்பாடு
நெர்ன்ஸ்ட் சமன்பாடு
நெர்ன்ஸ்ட் சமன்பாடு என்பது மின்கல மின்னழுத்தம் மற்றும் மின்வேதி வினையில் ஈடுபடும் கூறுகளின் செறிவு ஆகியவற்றை தொடர்புபடுத்தும் சமன்பாடாகும். பின்வரும் ஒட்டுமொத்த ஆக்ஸிஜனேற்ற ஒடுக்க வினை நிகழும் ஒரு மின்வேதிக் கலனை கருதுவோம்,
xA + yB ↔ lC + mD
மேற்காண் வினைக்கான வினைக்குணகம் (Q) மதிப்பு கீழே கொடுக்கப்பட்டுள்ளது
Q = [C]Ɩ [D]m / [A]x [B]y ......(9.28)
நாம் முன்னரே கற்றறிந்தபடி,
∆G = ∆G° + RT lnQ .....(9.29)
கிப்ஸ் கட்டிலா ஆற்றலை மின்கல emf உடன் பின்வருமாறு தொடர்பு படுத்த முடியும். (சமன்பாடுகள் (9.24) மற்றும் (9.25)]
∆G = - nFEcell ; ∆G° = - nFE°cell
இந்த மதிப்புகளையும், சமன்பாடு (9.28) லிருந்து Q மதிப்பையும் சமன்பாடு (9.29) ல் பிரதியிட
(9.29) ⇒ - nFEcell = - nFEocell + RT ln [C]Ɩ [D]m / [A]x [B]y ......(9.30)
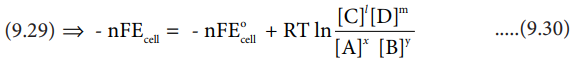
சமன்பாடு (9.30) முழுவதையும் (-nF) ஆல் வகுக்க
(9.25) ⇒ Ecell = Eocell - RT / nF ln [C]Ɩ [D]m / [A]x [B]y
(or) Ecell = Eocell – 2.303RT/nF log [C]Ɩ [D]m / [A]x [B]y ......(9.31)
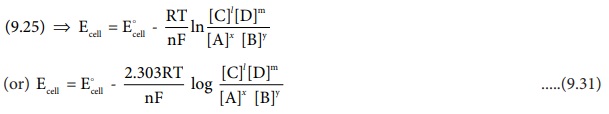
மேற்காண் சமன்பாடு (9.31) ஆனது நெர்ன்ஸ்ட் சமன்பாடு என்றழைக்கப்படுகிறது. 25°C (298K), வெப்பநிலையில் சமன்பாடு (9.31) ஐ பின்வருமாறு எழுதலாம்,

25°C வெப்பநிலையில் நெர்ன்ஸ்ட் சமன்பாட்டை பயன்படுத்தி பின்வரும் மின்கலத்தின் emf மதிப்பை நாம் கணக்கிடுவோம்.
Cu (s) | Cu2+ (0.25 aq, M) | | Fe3+ (0.005 aq M) | Fe2+ (0.1 aq M) | Pt (s)
Given : (Eo) Fe3+│Fe2+ = 0.77V and (Eo) Cu2+ │Cu = 0.34 V
நிகழும் அரைகல வினைகள்
Cu (s) → Cu2+ (aq) + 2e- ..... (1)
2 Fe3+ → (aq) + 2e- → 2Fe2+ (aq) ..... (2)
ஒட்டுமொத்த வினை
Cu (s) + 2 Fe3+ (aq) → Cu2+ (aq) + 2Fe2+ (aq), and n = 2
25°C வெப்பநிலையில் நெர்ன்ஸ்ட் சமன்பாட்டை பயன்படுத்த
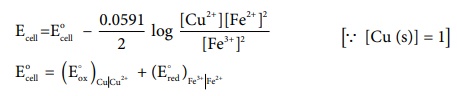
Cu2+ │ Cu பின் திட்ட ஒடுக்க மின்னழுத்த மதிப்பு 0.34 V
∙ (Eoox) Cu│Cu3+ = -0.34V
(Eored) Fe3+ │ Fe2+ = 0.77V
∙ Eocell = - 0.34 + 0.77
Eocell = 0.43V

∙ Ecell =0.43 - 0.0591 / 2 × log (0.25) (0.1)2/ (0.005)2
=0.43 - 0.0591 / 2 × 2
=0.43 - 0.0591
= 0.3709V.
= log (0.25) (0.1)2 / (0.005)2
= log 25 × 10-2 × 1 × 10-2 / 25 × 10-6
= log 10-2
= 2 log10 10
= 2.
தன் மதிப்பீடு
டேனியல் மின்கலத்தில் நிகழும் மின்வேதிக் கலவினை
Zn (s) + Cu2+ (aq) → Zn2+ (aq)+Cu (s)
நேர்மின்முனைப் பகுதியில் அயனிச் செறிவை 10 மடங்கு அதிகரிக்கும்போது மின்கல மின்னழுத்தத்தில் ஏற்படும் மாற்றம் என்ன?