மின் வேதியியல் - தன்மதிப்பீடு - தீர்வுகள் | 12th Chemistry : UNIT 9 : Electro Chemistry
12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 9 : மின் வேதியியல்
தன்மதிப்பீடு - தீர்வுகள்
III. தன்மதிப்பீடு
1. 25°C வெப்பநிலையில் 0.01 M செறிவுடைய நீர்த்த KCl கரைசலின் மோலார் கடத்துத்திறனை கணக்கிடுக. 25°C வெப்பநிலையில் KCl கரைசலின் நியம கடத்துத்திறன் மதிப்பு 14.114 × 10-2 Sm-1
M = 0.01M K = 14.114 × 10-2 Sm-1 ∧m = ?
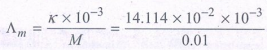
= 14.114 × 10-3
∧m =1.4114 × 10-2 Sm2 mol-1
2. 25°C ல் பின்வரும் மின்கலத்தின் emf மதிப்பு 0.34V காப்பர் மின்முனையின் ஓடுக்க மின்னழுத்த மதிப்பை கணக்கிடுக.
Pt (s) |H2 (g, 1 atm) |H+ (aq, 1 M) ||Cu2+. (aq, 1 M) | Cu (s)
Eoகலம் = 0.34 V (Eoஒடுக்)Cu2+|Cu= ?
(Eo ஆக்சி)H2| H+ =0 V
Eoகலம் = (Eo ஆக்சி)H2| H++ (Eoஒடுக்)Cu2+|Cu
0.34 = 0 + (Eoஒடுக்)Cu2+|Cu
(Eoஒடுக்)Cu2+|Cu = 0.34 V
3. ஜிங்க் மற்றும் காப்பர் மின்முனைகளின் கணக்கிடப் பட்ட emf மதிப்புகளைப் பயன்படுத்தி, 25°C ல் பின்வரும் மின்கலத்தின் emf மதிப்பை காண்க.
Zn (s) |zn2+ (aq, 1 M) ||Cu2+ (aq, 1 M)| Cu (s)
Eoகலம் = ? (Eo ஆக்சி)Zn (s) |zn2+ = 0.76 V ; (Eoஒடுக்)Cu2+|Cu = 0.34 V
Zn (s) |Zn2+ (aq, l M)|| Cu 2+ (aq, 1M| Cu (s)
Eoகலம் = (Eo ஆக்சி)Zn (s) |zn2+ + (Eoஒடுக்)Cu2+|Cu
= 0.76 + 0.34
Eoகலம் = + 1.1V
4. பின்வரும் கால்வானிக் மின்கலத்தில் நிகழும் ஒட்டு மொத்த ஆக்ஸிஜனேற்ற ஒடுக்க வினையை எழுதுக.
Pt (s) |Fe2+ (aq), Fe3+ (aq) || |MnO4- (aq),
H+ (aq), Mn2+ (aq) |Pt (s)
Fe2+ → Fe3+ + e (ஆக்சிஜனேற்றம்) ---------- (1)
MnO4- + 8H+ + 5e → Mn2+ + 4H2Ol ஒடுக்கம் ---(2)
(1) × 5 5Fe2+ → 5Fe3+ + 5e ------- (3)
(2) + (3) 5
Fe2+ + MnO4- +8 H+ → 5Fe3++ Mn2+ + 4 H2O(l)
5. டேனியல் மின்கலத்தில் நிகழும் மின்வேதிக் கலவினை
Zn (s) + Cu2+ (aq) → Zn2+ (aq) + Cu (s)
நேர்மின்முனைப் பகுதியில் அயனிச் செறிவை 10 மடங்கு அதிகரிக்கும்போது மின்கல மின்னழுத் தத்தில் ஏற்படும் மாற்றம் என்ன?
Zn (s) + Cu2+ (aq) → Zn2+ (aq) + Cu (s)
நேர்மின்வாய் Zn(s) – Zn+2aq + 2e- (ஆக்சிஜனேற்றம்)
எதிர்மின்வாய் Cu2+(aq) + 2e- Cu(s) (ஒடுக்கம்)
n = 2

எதிர்மின்வாய் பகுதி செறிவு = நேர்மின்வாய்பகுதி செறிவு
[Cu2+] = [Zn2+] = 1M
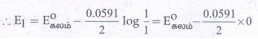
E1 = Eoகலம்
நேர்மின் முனைப் பகுதியின் அயனிச் செறிவு 10 மடங்கு அதிகரிக்கும்போது
[Zn2+] = 10 M[Cu2+] =1M
E2 = Eoகலம் - (0.0591 / 2 ) log (10 / 1)
E2 = Eoகலம் -0.02955 × 1
மின்கல மின்னழுத்தம் 0.02955 V குறைகிறது.
6. 0.15 ஆம்பியர் மின்னோட்டத்தை கொண்டு, ஒரு உலோக உப்புக் கரைசலானது 15 நிமிடங்களுக்கு நீராற்பகுக்கப்படும்போது, எதிர்மின்முனையில் விடுவிக்கப்பட்ட உலோகத்தின் நிறை 0.783 கிராம் எனில், அந்த உலோகத்தின் சமான நிறையை கணக்கிடுக.
t = 15 நிமிடங்க ள் = 15 × 60 = 900 sec
I = 0.15 ஆம்பியர்
m = 0.783 கி
Z = ? e =?
m = ZIt
ஃ Z = m/It = 0.783/(0.15 × 900) = 5.8 ×10-3
Z = சமமானநிறை / 96500
ஃ சமமானநிறை = Z × 96500
= 5.8 × 10-3
× 96500
சமமானநிறை = 559.7